Students get through AP Inter 2nd Year Chemistry Important Questions Lesson 6(a) 15వ గ్రూపు మూలకాలు which are most likely to be asked in the exam.
AP Inter 2nd Year Chemistry Important Questions Lesson 6(a) 15వ గ్రూపు మూలకాలు
Very Short Answer Questions (అతిస్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
నైట్రోజన్ యొక్క చర్యాశీలత ఫాస్పరస్కు భిన్నంగా ఉంటుంది. ఎందువలన?
జవాబు:
నైట్రోజన్ ద్విపరమాణుక అణువు (N2) గా ఉంటుంది. రెండు N- పరమాణువుల మధ్య త్రిబంధం ఉండుట వలన అధిక బంధ విచ్చేధన శక్తి (941.4kJ mol-1) ఉంటుంది.అందువలన మూలక స్థితిలో నైట్రోజన్ చర్యలో పాల్గొనకుండా జడత్వంను కలిగియుంటుంది
తెలుపు లేదా పసుపు ఫాస్పరస్ చతుర్ధ (టెట్రా) పరమాణుక అణువు (P4)గా ఉంటుంది. P-P మధ్య ఏక బంధం ఉండుట వలన, N≡N బంధం కంటే తక్కువ బంధ విచ్ఛేదన శక్తి (213 kJmol-1) ఉంటుంది. అందువలన ఫాస్ఫరస్ నైట్రోజన్ కంటే అత్యధిక చర్యాశీలతను కలిగి ఉంటుంది.
ప్రశ్న 2.
ప్రయోగశాలలో నైట్రోజన్ ను ఎలా తయారు చేస్తారు. ఈ చర్యలో ఇమిడి ఉన్న రసాయన సమీకరణమును వ్రాయుము.
జవాబు:
సమమోలార్ అమ్మోనియం క్లోరైడ్ మరియు సోడియం నైట్రైట్ జల ద్రావణాలను వేడి చేసి ప్రయోగశాలలో నైట్రోజన్ ను తయారు చేస్తారు.
NH4Cl(aq) + NaNO2(aq) → NH4NO2(aq) + NaCl(aq)
ద్విస్థానభ్రంశ చర్యలో ఏర్పడిన అమ్మోనియం నైట్రైట్ అస్థిరమైనది. కావున ఇది వియోగం చెంది నైట్రోజన్ వాయువును ఇస్తుంది.
![]()
ప్రశ్న 3.
నైట్రోజన్ ద్విపరమాణుక అణువుగాను మరియు ఫాస్ఫరస్ P4గాను ఉంటాయి. ఎందువలన? [TS 15]
జవాబు:
నైట్రోజన్ తక్కువ పరమాణు పరిమాణము మరియు అధిక ఋణవిద్యుదాత్మకత వలన Pπ-Pπ బహు బంధాలను ఏర్పరుస్తుంది. అందువలన రెండు నైట్రోజన్ పరమాణువుల మధ్య త్రిబంధం కలిగి నైట్రోజన్ ద్విపరమాణుక అణువుగా ఉంటుంది.
అధిక పరమాణు పరిమాణం మరియు అల్ప ఋణ విద్యుదాత్మకత వలన ఫాస్ఫరస్ తానంతట తానుగా Pπ-Pπ బంధాలను ఏర్పరచుకోలేదు.
అందువలన ఫాస్ఫరస్ P-P ఏకబంధాలను ఏర్పర్చుకొని చతుర్ముఖీయ P4 అణువుగా ఉంటుంది.
ప్రశ్న 4.
ఫాస్ఫరస్ కంటే నైట్రోజన్ తక్కువ కాటనేషన్ ధర్మాలను ప్రదర్శిస్తుంది. ఎందువలన?
జవాబు:
కాటనేషన్ ధర్మం మూలకం-మూలకం యొక్క బంధ బలం పై ఆధారపడుతుంది. N-N (159 kJmol-1) బంధ బలం, P-P (213 kJ mol-1) బంధ బలం కంటే చాలా తక్కువ. అందువలన ఫాస్ఫరస్ కంటే నైట్రోజన్ తక్కువ కాటనేషన్ ధర్మాలను ప్రదర్శిస్తుంది.
ప్రశ్న 5.
నైట్రోజన్ అణువు అత్యధికంగా స్థిరమైనది. ఎందువలన? [IPE ’14]
జవాబు:
N2 లో రెండు N పరమాణువులు బాగా బలమైన త్రికసమయోజనీయ బంధాలతో బంధించబడి ఉంటాయి. అందువలన బంధ విచ్ఛేధన శక్తి అధికంగా ఉంటుంది. ఈ ఫలితంగా గది ఉష్ణోగ్రత వద్ద N2 కు తక్కువ చర్యాశీలతను మరియు అధిక స్థిరత్వం కలిగి ఉంటుంది.
![]()
ప్రశ్న 6.
+3 ఆక్సీకరణ స్థితిలో ఉన్న బిస్మత్ సమ్మేళనాలు అత్యంత స్థిరంగా ఉంటాయి. ఎందువలన?
జవాబు:
జడజంట ప్రభావం కారణంగా గ్రూపులో క్రిందకు పోయే కొలది +5 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం తగ్గుతుంది. మరియు +3 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం పెరుగుతుంది. అందువలన అందువలన +3 ఆక్సీకరణ స్థితిలో ఉన్న బిస్మత్ సమ్మేళనాలు, +5 ఆక్సీకరణ స్థితిలో ఉన్న సమ్మేళనాల కంటే అత్యంత స్థిరమైనవి.
ప్రశ్న 7.
రూపాంతరత అనగానేమి? ఫాస్ఫరస్ యొక్క భిన్న రూపాంతరాలను వివరింపుము. [TS 16]
జవాబు:
ఒక మూలకం రెండు గాని అంతకంటే ఎక్కువ గాని భౌతిక రూపాలలో ఉండి, ఇంచుమించుగా ఒకే రసాయన ధర్మాలను కలిగి, వేరువేరు భౌతిక ధర్మాలను ప్రదర్శించే ప్రక్రియను రూపాంతరత అంటారు.
ఫాస్ఫరస్ యొక్క రూపాంతరాలు :
a) తెల్ల (లేదా) పసుపు – P
b) ఎర్ర – P
c) స్కార్లెట్ – P
d) ఉదా రంగు – P
e) α – నల్ల ఫాస్ఫరస్ మరియు β – నల్ల ఫాస్ఫరస్
ప్రశ్న 8.
నైట్రోజన్ జడ స్వభావాన్ని ఏ విధంగా వివరిస్తారు?
జవాబు:
N≡N బంధం యొక్క బంధన శక్తి అత్యధికంగా ఉండుట వలన గది ఉష్ణోగ్రత డైనైట్రోజన్ జడస్వభావాన్ని కలిగి ఉంటుంది.
ప్రశ్న 9.
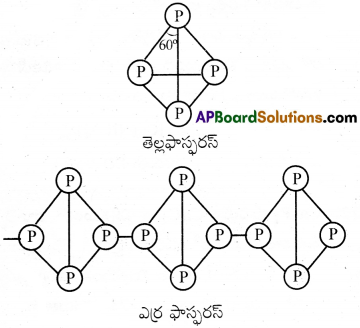
తెల్ల ఫాస్ఫరస్ మరియు ఎర్ర ఫాస్ఫరస్ల నిర్మాణాల్లోని భిన్నత్వాన్ని వివరించండి.
జవాబు:
తెల్లఫాస్ఫరస్ విచ్ఛిన టెట్రా హైడ్రాల్ P4 అణువులను కలిగియుంటుంది.కాని ఎర్ర ఫాస్ఫరస్ లోని టెట్రా హైడ్రాల్ P4 లు ఒక దానిలో ఒకటి సమయోజనీయ బంధాలను ఏర్పరచుకుని శృంఖాలను కలిగి ఉంటుంది.
ప్రశ్న 10.
ఎర్ర ఫాస్ఫరస్ నుండి – నల్ల ఫాస్ఫరస్ ను ఏ విధంగా తయారు చేస్తారు?
జవాబు:
ఎర్ర ఫాస్ఫరస్ ను మూసి ఉన్న గొట్టంలో 803K వద్ద వేడి చేయగా α-నల్ల ఫాస్ఫరస్ ఏర్పడుతుంది.
ప్రశ్న 11.
తెల్లని ఫాస్ఫరస్ మరియు ఎర్ర ఫాస్ఫరస్ ధర్మాల్లోని బేధాలను వ్రాయండి.
జవాబు:
తెల్లని ఫాస్ఫరస్:
- ఇది మృదువైన మరియు వెల్లులి లాంటి వాసన కలిగిన ఘనపదార్థము
- ఇది విషపూరితమైనది.
- ఇది నీటిలో కరుగదు కాని కార్బన్ డై సల్ఫైడ్లో కరుగుతుంది.
- ఇది గాలిలో ఆయత్నికృతంగా, స్వచ్చంగా మండుతుంది.
- ఘన మరియు భాష్ప స్థితిలో ఇది P4 అణువుగా ఉంటుంది.
తెల్లని ఫాస్ఫరస్:
- ఇది కఠినమైన మరియు స్ఫటిక ఘనపదార్థం. దీనికి వాసన లేదు.
- ఇది విషపూరితమైనది కాదు.
- ఇది నీటిలోను మరియు కార్బన్ డై సల్ఫైడ్ రెండింటిలోను కరుగదు.
- ఇది తక్కువ చర్యాశీలతను కలిగి ఉంటుంది.
- ఇది టెట్రా హైడ్రాల్ P4 యూనిట్లతో శృంఖలాలుగా ఉంటుంది.
![]()
ప్రశ్న 12.
“జడ జంట ప్రభావం” అనగానేమి? [ TS 22]
జవాబు:
వేలన్సీ స్థాయిలోని ns ఎలక్ట్రాన్లను కేంద్రకం బాగా బలంగా ఆకర్షించుట వలన ఇవి రసాయన చర్యలో పాల్గొనవు. దీనినే “జడజంట ప్రభావం” అంటారు. ఈ ధర్మంనకు కారణం d మరియు f ఆర్బిటాల్లకు గల తక్కువ పరిరక్షణ ప్రభావం.
ప్రశ్న 13.
NH3 బలమైన క్షారం, BiH3 బలహీన క్షారం ఎందువలన? వివరింపుము.
జవాబు:
Bi కంటే N చాలా చిన్నది. అందువలన దాని బంధంలో పాల్గొనని ఎలక్ట్రాన్ల లు తక్కువ ప్రదేశంలో కేంద్రీకృతమై ఉంటాయి.
అందువల్ల ‘N’ పరమాణువు మీద ఉన్న బంధగతం కాని ఎలక్ట్రాన్ సాంద్రత, Bi పరమాణువు మీద ఉన్న ఎలక్ట్రాన్ సాంద్రత కంటే ఎక్కువ. దీని ఫలితంగా NH3 లోని N కు ఎలక్ట్రాన్ జంటను దానం చేసే ప్రవృతి BiH3 లోని Bi కంటే ఎక్కువ. అందువలన BiH3 కంటే NH3 బలమైన క్షారం.
ప్రశ్న 14.
15వ గ్రూపు మూలకాల హైడ్రేడ్లను క్షారబలం పెరిగే క్రమంలోను మరియు క్షయకరణ స్వభావం తగ్గే క్రమంలో అమర్చండి.
జవాబు:
పెరిగే క్రమం (క్షార బలం పెరుగును):
BiH3 < SbH3 < AsH3 < PH3 < NH3
క్షయకరణం స్వభావం తగ్గే క్రమం:
BiH3 > SbH3 > AsH3 > PH3 > NH3
ప్రశ్న 15.
NH3 కంటే PH3 బలహీనమైన క్షారం వివరింపుము.
జవాబు:
N కంటే P కు ఎక్కువ పరమాణు పరిమాణం ఉంటుంది. అందువలన Nతో పోలిస్తే ‘P’ లోని బంధంలో పాల్గోనని ఎలక్ట్రాన్ జంట ఎక్కువ ప్రదేశంలో కేంద్రీకృతమై ఉంటుంది. అందువలన ‘P’ పరమాణువులోని ఎలక్ట్రాన్ సాంద్రత నైట్రోజన్ పరమాణువులోని ఎలక్ట్రాన్ సాంద్రత కంటే చాలా తక్కువ అందువలన PH3, NH3 కంటే చాలా బలహీనమైన క్షారం.
ప్రశ్న 16.
15 వగ్రూపు మూలకాల్లోని ఒక హైడ్రైడ్ నీటిలో కరిగి క్షార ద్రావణాన్ని ఏర్పరచింది. ఈ ద్రావణం AgCl అవక్షేపాన్ని కరిగించింది. ఆహైడ్రైడ్ పేరును, ఈ చర్యలో ఇమిడి ఉన్న రసాయన సమీకరణంను వ్రాయండి.
జవాబు:
NH3 నీటిలో కరిగి క్షార ద్రావణంను ఏర్పర్చును. ఈ ద్రావణం సంక్లిష్ట లవణంను ఏర్పరచుట వలన ఇది AgCl అవక్షేపంలో కరుగును.

ప్రశ్న 17.
CO2 యొక్క జడ వాతావరణం సమక్షంలో తెల్ల ఫాస్ఫరస్ ను గాఢ NaOH ద్రావణంతో కలిపి వేడి చేసిన ఏమి జరుగుతుంది? [AP-15,19]
జవాబు:
CO2 యొక్క జడ వాతావరణ సమక్షంలో తెల్ల ఫాస్ఫరస్ ను గాఢ NaOH ద్రావణంతో కలిపి వేడి చేసిన ఫాస్ఫిన్ వాయువు వెలువడుతుంది.
P4 + 3NaOH + 3H2O → 3NaH2PO2 + PH3 ↑
![]()
ప్రశ్న 18.
NH3 హైడ్రోజన్ బంధాలను ఏర్పరుస్తుంది. కాని PH3 ఏర్పరచదు. ఎందువల్ల? [TS-15]
జవాబు:
N(3.0) యొక్క ఋణవిద్యుదాత్మకత H(2.1) కంటే అత్యధికం మరియు అధిక దృవశీలత గలN-H బంధం వలన NH3 అంతరణుక H-బంధాలను ఏర్పరుస్తుంది. P మరియు H రెండింటి యొక్క బుణవిద్యుదాత్మకత (2.1). అందువలన P-H బంధంనకు దృవశీలత ఉండదు. కావున PH, H- బంధాలను ఏర్పర్చలేదు.
ప్రశ్న 19.
HNH బంధ కోణం HPH, HAsH మరియు HSbH కోణాల కంటే ఎక్కువ. ఎందువల్ల?
జవాబు:
N నుండి Sb కి పోయేకొలది ఋణవిద్యుదాత్మకత తగ్గుతుంది. బంధక ఎలక్ట్రాన్ జంటలు కేంద్రక పరమాణువుకు దూరంగా జరిగి ఉండును. అనగా పక్క పక్కన గల బంధక జంటల మధ్య వికర్షణబలాలు తగ్గుతాయి. కనుక NH3 నుండి SbH3 కి బంధకోణం తగ్గుతుంది.
ప్రశ్న 20.
కాల్షియం ఫాస్ఫైడ్, భార జలంతో ఏవిధంగా చర్య జరుపుతుంది?
జవాబు:
కాల్షియం ఫాస్ఫైడ్, భారజలంతో చర్య జరిపి PD3 ను ఏర్పరుస్తుంది.

ప్రశ్న 21.
అమ్మోనియా మంచి సంక్లిష్ట కారకం అని ఒక ఉదాహరణతో వివరించండి. [IPE ’14]
జవాబు:
అమ్మోనియా అణువులోని నైట్రోజన్ మీద ఉన్న ఒంటరి జంట ఎలక్ట్రాన్ల వలన NH3 లూయిస్ క్షారంగా పని చేస్తుంది. ఇది ఎలక్ట్రాన్లను దానం చేసి లోహ అయాన్తో సంక్లిష్ట అయానన్ను ఏర్పరుస్తుంది.
ఈ ధర్మం వలన అమ్మోనియా మంచి సంక్లిష్ట కారకంగా పని చేస్తుంది. ఇది లోహ అయాన్ను కనుగొనుటకు ఉపయోగపడుతుంది.
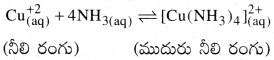
ప్రశ్న 22.
Ca3P2 మరియు CaC2 ల మిశ్రమంను హూల్మే సంకేతాల తయారీలో ఉపయోగిస్తారు. వివరింపుము.
జవాబు:
Ca3P2 మరియు CaC2 ల మిశ్రమంను కలిగి ఉన్న పాత్రకు రంధ్రం చేసి సముద్రంలోకి విసురుతారు. కాల్షియం ఫాస్ఫైడ్ సముద్ర జలంతో చర్య జరిపి PH3 ఫాస్ఫిన్ ను విడుదల చేస్తుంది. [AP 16]
Ca3P2 + 6H2O → 3Ca(OH)2 + PH3
కాల్షియం కార్బైడ్ నీటితో చర్య జరిపి ఎసిటిలిన్ వాయువును విడుదల చేస్తుంది.
CaC2 + 2H2O → Ca(OH)2 + C2H2
విడుదలైన ఫాస్ఫీన్ మంటను అందుకొని, ఎసిటిలీన్ ను మండిస్తుంది. ఈ మండుతున్న వాయువులు, సముద్ర తీరానికి చేరే ఓడలకు సంకేతాల వలె పని చేయును.
ప్రశ్న 23.
నైట్రేట్ అయాన్ యొక్క జేగురు రంగు వలయ పరీక్షలో ఏ రసాయన సమ్మేళనం ఏర్పడుతుంది. [AP 18]
జవాబు:
[Fe(H2O)5NO]+2.
ప్రశ్న 24.
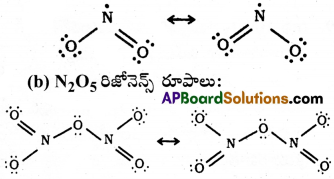
NO2 మరియు N2O5 ల రిజోనెన్స్ నిర్మాణాలను వ్రాయండి.
జవాబు:
(a) NO2 రిజోనెన్స్ రూపాలు:
ప్రశ్న 25.
R3P = O ఉంటుంది కాని R3N = O సాధ్యంకాదు. ఎందువల్ల? (R = అల్కైల్)
జవాబు:
d- ఆర్బిటాల్ లేక పోవుట వలన నైట్రోజన్ pπ-dπ బహు బంధాలను ఏర్పర్చలేదు.
దీని ఫలితంగా నైట్రోజన్ సమయోజకతను నాలుగు మించి విస్తరించలేదు కనుక R3N = O ఉండదు. కాని ఫాస్ఫరస్ నందు d- ఆర్బిటాల్ ఉండుటచే అది pπ-dπ బంధాలను ఏర్పర్చుట ద్వారా దాని సమయోజకతను నాలుగు కన్నా ఎక్కువకు విస్తరించుకోగలదు. కనుక ఫాస్ఫరస్ సమయోజకత ఐదు కలిగిన R3P = O ను ఏర్పర్చును.
![]()
ప్రశ్న 26.
నైట్రిక్ ఆక్సైడు (NO) ఏ విధంగా తయారు చేస్తారు?
జవాబు:
అమ్మోనియాను ఆక్సిజన్ వాతావరణంలో ఉత్ప్రేరకం సమక్షంలో ఆక్సీకరించగా నైట్రిక్ ఆక్సైడ్ ఏర్పడును.
![]()
ప్రశ్న 27.
నైట్రోజన్ యొక్క సాధారణ ఆక్సైడ్ మరియు మిశ్రమం ఆక్సైడ్లకు ఒక్కో ఉదాహరణనిమ్ము.
జవాబు:
సాధారణ ఆక్సైడ్ : NO
మిశ్రమం ఆక్సైడ్ : N2O3
ప్రశ్న 28.
NO వాయుస్థితిలో పారా అయస్కాంత ధర్మంను చూపిస్తుంది. కాని ద్రవ మరియు ఘనస్థితిలో డయా అయస్కాంత ధర్మంను చూపిస్తుంది. ఎందువల్ల?
జవాబు:
ఒంటరి ఎలక్ట్రాన్లు ఉండుట వలన వాయుస్థితిలో NO పారా అయస్కాంత ధర్మంను చూపిస్తుంది. కాని ద్రవ మరియు ఘనస్థితిలో N2O2 అను ద్విఅణుకంను ఏర్పర్చుట వలన ఇది డయాస్కాంత ధర్మంను చూపిస్తుంది.

ప్రశ్న 29.
(a) ఫాస్ఫరస్ యొక్క ఆమ్ల ఆక్సైడ్ (b) నైట్రోజన్ యొక్క తటస్థ ఆక్సైడ్లకు ఉదాహరణను ఇవ్వండి. [TS – 18][AP17]
జవాబు:
(a) ఫాస్ఫరస్ యొక్క ఆమ్ల ఆక్సైడ్ P2O5 (ఫాస్ఫరస్ పెంటాక్సైడ్)
(b) నైట్రోజన్ యొక్క తటస్థ ఆక్సైడ్ NO (నైట్రిక్ ఆక్సైడ్.)
ప్రశ్న 30.
ఈ క్రింది వానిని వివరింపుము.
(a) ఎర్ర ఫాస్ఫరస్ క్షారం చర్య
(b) PCl3, H3PO3ల మధ్య చర్య
జవాబు:
a) ఎర్ర ఫాస్ఫరస్తో క్షారం చర్య నొందదు.
b) PCl3, H3PO3తో చర్య జరిపి పైరోఫాస్ఫరస్ ఆమ్లంను ఏర్పరుస్తుంది.
5H3PO3 + PCl3 → 3H4P2O5 + 3HCl
ప్రశ్న 31.
(a) CH3COOH (b) C2H OH (c) నీరు లతో PCl3 ఏ విధంగా చర్య జరుపుతుంది.
జవాబు:
(a) PCl3, CH3COOH తో చర్యనొంది ఎసిటైల్ క్లోరైడ్ను ఏర్పరస్తుంది.
3CH3COOH + PCl3 → 3CH3COCl + H3PO3
(b) PCl3, C2H5OH తో చర్యనొంది ఈథైల్ క్లోరైడ్ను ఏర్పరుస్తుంది.
3CH2H3OH + PCl3 → 3C2H5Cl + H3PO3
(c) PCl3 నీటితో వేగంగా చర్యనొంది ఫాస్ఫరస్ ఆమ్లంను ఏర్పరుస్తుంది.
PCl3 + 3H2O → H3PO3 + 3HCl
ప్రశ్న 32.
PCl3 ఆక్సీకరణిగాను మరియు క్షయకరణిగాను పని చేయగలదు. వివరణ ఇవ్వండి.
జవాబు:
PCl3 లో ఫాస్ఫరస్ ఆక్సీకరణ స్థితి +3 ఇది గరిష్ట ఆక్సీకరణ స్థితి +5 కు మరియు కనిష్ట ఆక్సీకరణ స్థితి -3. కు మధ్య ఉంటుంది. అందువలన ఇది ఆక్సీకరణి గాను మరియు క్షయకరణిగాను పని చేస్తుంది.
ఆక్సీకరణిగా పనిచేసినప్పుడు
12Ag + 4PCl3 → 12AgCl + P4
క్షయకరణిగా పని చేసినపుడు
SO3 + PCl3 → POCl3 + SO2
![]()
ప్రశ్న 33.
ఈ క్రింది వానిలో వేటిని ఏర్పరచటం సాధ్యంకాదు?
PCl3, AsCl3, SbCl3, NCl5, BiCl5, PH5
జవాబు:
నైట్రోజన్లో ఖాళీ d- ఆర్బిటాల్లు లేక పోవుట వలన ఇది పెంటాహాలైడ్లను ఏర్పర్చలేదు. కావున NCl5ను ఏర్పరచటం సాధ్యంకాదు.
జడజంట ప్రభావము వలన BiCl5 ఏర్పడదు. ఫాస్ఫరస్లోని d- ఆర్బిటాల్ మరియు H లో 1s ఆర్బిటాల్ల అతిపాత అవధి తక్కువగా ఉండుట వలన PH5 ఏర్పడదు.
ప్రశ్న 34.
SbCl5 లేక SbCl3 లలో దేనికి అధిక సంయోజకత కలదు?
జవాబు:
SbCl5 లో అధిక ఆక్సీకరణ స్థితి +5 ఉండుట వలన SbCl3 మరియు SbCl5 లలో SbCl5 కు అధిక సంయోజకత ఉంటుంది.
ప్రశ్న 35.
PCl5 ఘనస్థితిలో ఫాస్పరస్ యొక్క ఆక్సీకరణ స్థితులను వ్రాయుము.
జవాబు:
ఇది ఘనస్థితిలో అయానిక ఘన పదార్థంగా ఉంటుంది. అనగా [PCl4]+ లో ‘P’ ఆక్సీకరణ స్థితి +5
[PCl6]– లో ‘P’ ఆక్సీకరణ స్థితి +5
∴ ఘనPCl5 లో ఫాస్ఫరస్ ఆక్సీకరణ స్థితి +5
ప్రశ్న 36.
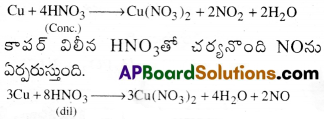
కాపర్ లోహము HNO3తో చర్య నొందినపుడు భిన్న రకాల ఉత్పనాలను ఏవిధంగా ఏర్పరుస్తుందో వివరింపుము.
జవాబు:
కాపర్ లోహము గాఢ HNO3 తో చర్యనొంది NO2ను ఏర్పరుస్తుంది.
ప్రశ్న 37.
నైట్రిక్ ఆమ్లంలోని నైట్రోజన్ ఆక్సీకరణ స్థితికి సమానమైన ఆక్సీకరణ స్థితి ఉన్న నైట్రోజన్ ఆక్సైడ్ ఏది?
జవాబు:
N2O5లో నైట్రోజన్ యొక్క ఆక్సీకరణ సంఖ్య +5. ఇది HNO3లోని కు N ఆక్సీకరణ స్థితికి సమానం.
ప్రశ్న 38.
నైట్రిక్ ఆమ్లం తయారీలో జరిగే రసాయన చర్యలను వ్రాయండి.
జవాబు:
అధిక పరిమాణంలో HNO3 ని ప్రధానంగా ఆస్వాల్డ్ విధానంలో తయారు చేస్తారు. ఇందులో ఇమిడి ఉన్న రసాయన చర్యలు.

ప్రశ్న 39.
గాఢ HNO3 సమక్షంలో ఇనుము (ఐరన్) క్రియారహితంగా ఉంటుంది. ఎందువల్ల?
జవాబు:
ఐరన్, క్రోమియం, నికెల్ మరియు అల్యూమినియం వంటి లోహాలను గాఢ HNO3 ముంచినపుడు, అవి వాటికి ఉన్న సాధారణ చర్యాశీలతను కోల్పోయి క్రియారహితంగా మారుతాయి. ఇందుకు కారణం లోహాల ఉపరితలంపై లోహ ఆక్సైడ్ అనే పలుచని రక్షణ పొర ఏర్పడుట.ఇది తరువాత చర్యను నిరోధిస్తుంది.
3Fe + 8HNO3 → FeO.Fe2O3 + 8NO2 + 4H2O
ప్రశ్న 40.
(a) నైట్రిక్ ఆమ్లం మరియు (b) అమ్మోనియాల ఉపయోగాలను వ్రాయండి.
జవాబు:
a) దీనిని NH4NO3 వంటి ఎరువును తయారు చేయుటకు మరియు నైట్రేట్ కలిగిన విస్ఫోటకాలు మరియు మంటను ఏర్పర్చే సాధనాలను తయారు చేయుటకు ఉపయోగిస్తారు. దీనిని నైట్రోగ్లిసరిన్, నైట్రోటోలిన్ మరియు కర్బన నైట్రో సమ్మేళనాలను తయారు చేయుటకు ఉపయోగిస్తారు. దీనిని స్టెయిన్ లెస్ స్టీలు శుభ్రపర్చుటకు మరియు లోహాలను ఎచింగ్ చేయుటకు ఉపయోగిస్తారు. దీనిని రాకేట్ ఇంధనాలకు ఆక్సీకరణిగా ఉపయోగిస్తారు.
b) దీనిని అనేక నైట్రోజన్ కలిగియున్న ఎరువుల తయారీకి మరియు HNO3 వంటి నైట్రోజన్ కలిగిన ఇనార్గానిక్ సమ్మేళనాలను తయారు చేయుటకు ఉపయోగిస్తారు.
ప్రశ్న 41.
ఈక్రింది వానిలో ఫాస్ఫరస్ ఆక్సీకరణ స్థితులను తెల్పండి
(i) H3PO3
(ii) PCl3
(iii) Ca3P2
(iv) Na3PO4
(v) POF3
జవాబు:
(i) H3PO3 = +3
(ii) PCl3 = +3
(iii) Ca3P2 = -3
(iv) Na3PO4 = +5
(v) POF3 = +5
ప్రశ్న 42.
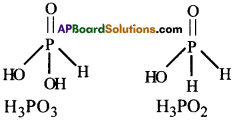
H3PO3 ద్విప్రోటిక్ ఆమ్లం కాని H3PO2 మాత్రం ఏకాప్రోటిక్ ఆమ్లం ఎందువల్ల?
జవాబు:
H3PO3 లో రెండు -OH గ్రూపులు ఉన్నాయి. కావున ఇది ద్విప్రోటిక్ ఆమ్లం. కాని H3PO2లో ఒకే ఒక్క -OH గ్రూపు ఉన్నది. అందువలన ఇది ఏక క్షారామ్లం.
ప్రశ్న 43.
H3PO3 యొక్క అననుపాత చర్యను తెల్పండి.
జవాబు:
ఆర్థోఫాస్ఫరస్ ఆమ్లంను వేడి చేసినపుడు అనుపాత చర్య నొంది ఆర్థోఫాస్ఫరిక్ ఆమ్లం మరియు ఫాస్ఫిన్లను ఏర్పరుస్తుంది.
![]()
ప్రశ్న 44.
H3PO2 ఒక మంచి క్షయకరణి అని ఉదాహరణతో వివరింపుము.
జవాబు:
P-H బంధాలను కలిగిన ఆమ్లం బలమైన క్షయకరణిగా పని చేస్తుంది.
హైపోఫాస్ఫరస్ ఆమ్లం (H3PO2) లో రెండు P-H బంధాలు ఉండుట వలన ఇది బలమైన క్షయకరణిగా పనిచేస్తుంది. ఉదాహరణకు ఇది AgNO3 ను లోహ సిల్వర్గా మరియు HgCl2 ను Hgగా క్షయకరిస్తుంది.
4AgNO3 + H3PO2 + 2H2O → 4Ag↓ + H3PO4 + 4HNO3
2HgCl2 + H3PO2 + 2H2O → 2Hg↓ + H3PO4 + 4HCl
![]()
ప్రశ్న 45.
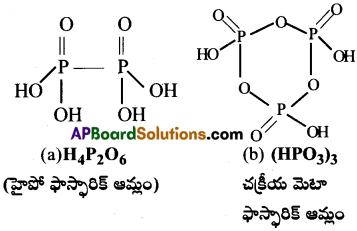
క్రింది వాటి నిర్మాణాలను గీయండి.
(a) హైపో ఫాస్ఫారిక్ ఆమ్లం
(b) చక్రీయ మెటా ఫాస్ఫారిక్ ఆమ్లం
జవాబు:
ప్రశ్న 46.
NH3 కంటే PH కి తక్కువ బాష్పీభవన స్థానము ఉంటుంది ఎందుకు? [TS 16,18]
జవాబు:
NH3 వలే ద్రవ స్థితిలో PH3 లోని పరమాణువులు హైడ్రోజన్ బంధం ద్వారా జతకూడవు. అందువల్ల NH3 కంటే PH3కి తక్కువ బాష్పీభవన స్థానము ఉంటుంది.
Short Answer Questions (స్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
15వ గ్రూపు మూలకాల సాధారణ అభిలాక్షణిక ధర్మాలను వాటి ఎలక్ట్రాన్ విన్యాసం, ఆక్సీకరణస్థితి, పరమాణు పరిమాణం, ఆయానీకరణ ఎంథాల్ని మరియు ఋణ విద్యుదాత్మకతల పరంగా చర్చించండి.
జవాబు:
ఎలక్ట్రాన్ విన్యాసం :
15వ గ్రూపు మూలకాలు సాధారణ ఎలక్ట్రాన్ విన్యాసం ns²np³. ఈ మూలకాలలో పూర్తిగా నిండిన S-ఆర్బిటాల్ మరియు సగం నిండిన – ఆర్బిటాల్ ఉండుటవలన వీటికి అదనపు స్థిరమైన ఎలక్ట్రాన్ విన్యాసం వస్తుంది.
ఆక్సీకరణ స్థితులు :
ఈ గ్రూపు మూలకాలు సాధారణ -3, +3 మరియు +5 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తాయి. గ్రూపులో క్రిందికి పోయే కొలది పరమాణు పరిమాణం మరియు లోహ స్వభావం పెరుగుట వలన -3 ఆక్సీకరణ స్థితిని ప్రదర్శించే ప్రవృత్తి తగ్గుతుంది. -3 ఆక్సీకరణస్థితి ఉన్న ఏ సమ్మేళనాన్ని Bi ఏర్పరచలేదు.
గ్రూపులో క్రిందికి పోయే కొలది +5 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం తగ్గుతుంది. అంతే కాకుండా గ్రుపూలో క్రిందికి పోయే కొలది +3 ఆక్సీకరణ స్థితి యొక్క స్థిరం పెరుగుతుంది. (కారణం జడ జంట ప్రభావం) నైట్రోజన్, ఆక్సిజన్తో చర్య నొందినపుడు +1,+2,+3, +4 మరియు +5 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తుంది. ఫాస్ఫరస్ కొన్ని ఆక్సో ఆమ్లాలలో +1 మరియు +4 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తుంది.
పరమాణు పరిమాణము :
గ్రూపులో పై నుండి క్రిందికి సమయోజనీయ మరియు ఆయానిక వ్యాసార్థాలు పెరుగుతాయి. నైట్రోజన్ నుండి ఫాస్ఫరస్కు గుర్తించదగినంత పరమాణు పరిమాణం పెరుగుతుంది. ఆర్సెనిక్ నుండి బిస్మత్కు పరమాణు పరిమాణం కొద్దిగా పెరుగుతుంది. ఇందుకు కారణం పెద్ద పరమాణువులలో పూర్తిగా నిండిన ‘d’ మరియు ‘f’ ఆర్బిటాళ్ళు ఉండటం.
ఆయానీకరణ ఎంథాల్పీ :
గ్రూపులో క్రిందికి పోయే కొలదిఆయానీకరణ ఎంథాల్పి తగ్గుతుంది. ఇందుకు ప్రధాన కారణం క్రమంగా వాటి పరమాణు పరిమాణం పెరుగటయే.
15వ గ్రూపు మూలకాల యొక్క అయానీకరణ ఎంథాల్పీ అదే పిరియడ్లోని 14వ గ్రూపు మూలకాల మరియు 16వ గ్రూపు మూలకాల అయానీకరణ ఎంథాల్పీ కంటే ఎక్కువ.
వరుస అయానీకరణ శక్తులు క్రమం ఈ క్రింది విధంగా ఉంటుంది. ∆iH1 > ∆iH2 > ∆iH3.
ఋణవిద్యుదాత్మకత :
గ్రూపులలో క్రిందికి పోయే కొలది పరమాణు పరిమాణం పెరుగుదలతో పాటు ఋణ విద్యుదాత్మకత విలువలు తగ్గుతాయి.
ప్రశ్న 2.
15వ గ్రూపు మూలకాల రసాయన చర్యశీలత తీరును చర్చించండి.
జవాబు:
15వ గ్రూపు మూలకాల రసాయన చర్యాశీలత తీరు:
1) ఆక్సీకరణ సంఖ్యలు :
ఈ గ్రూపు మూలకాలు సాధారణంగా −3, +3 మరియు +5 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తాయి. గ్రూపులో క్రిందికి పోయే కొలది –3 ఆక్సీకరణ స్థితిని ప్రదర్శించే ప్రవృత్తి తగ్గుతుంది. –3 ఆక్సీకరణ స్థితి ఉన్న ఏ సమ్మేళనాన్ని బిస్మత్ ఏర్పర్చలేదు.
గ్రూపులో పై నుండి క్రిందికి పోయే కొలది +5 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం తగ్గుతుంది కాని +3 ఆక్సీకరణ స్థితి యొక్క స్థిరత్వం పెరుగుతుంది. (కారణం జడజంట ప్రభావము) నైట్రోజన్, ఆక్సిజన్తో చర్య నొందినపుడు +1,+2,+3, +4 మరియు +5 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తుంది. కొన్ని ఆక్సో ఆమ్లాల్లో ఫాస్ఫరస్ +1 మరియు +4 ఆక్సీకరణ స్థితులను ఏర్పరుస్తుంది.
2) హైడ్రోజన్ చర్య :
ఈ మూలకాలు EH3 అనే ఫార్ములాగల సమయోజనీయ హైడ్రైడ్లను ఏర్పరుస్తాయి.(ఇచ్చట E = N,P, As, Sb)
a) గ్రూపులలో క్రిందికి పోయేకొలది హైడ్రైడ్ ఉష్టీయ స్థిరత్వం తగ్గుతుంది.
b) గ్రూపులో క్రిందికి పోయే కొలది హైడ్రైడ్ క్షయకరణ స్వభావం పెరుగుతుంది.
c) గ్రూపులో క్రిందికి పోయే కొలది క్షార స్వభావం తగ్గుతుంది.
d) హైడ్రోజన్ బంధాల కారణంగా NH3 యొక్క భాష్పీభవన స్థానం PH3 కంటే ఎక్కువ. మిగిలిన హైడ్రైడ్ భాష్పీభవన స్థానాలు PH3 నుండి పెరుగుతాయి.
నైట్రోజన్ లాంటి తేలికైన మూలకాలు E2H4 ఫార్ములా గల హైడ్రైడ్లను ఏర్పరుస్తాయి.
ఉదా: N2H4.
3) హాలోజన్లతో చర్య :
ఈ గ్రూపు మూలకాలు అన్ని (N, P, As, Sb, Bi) హలైడ్లను ఏర్పరుస్తాయి.
a) ట్రై హాలైడ్ల సాధారణ ఫార్ములా EX3.(NBr3 మరియు NI3 కాకుండా) మిగిలినవి అన్ని పిరమిడ్ ఆకారంలో స్థిరత్వంను కలిగి ఉంటాయి. ఇవి నీటిలో జల విశ్లేషణ చెందుతాయి.
b) పెంటా హాలైడ్ల సాధారణ ఫార్ములా (EX5) P, As మరియు Sbలు మాత్రమే వీటిని ఏర్పరుస్తాయి. కాని N ఏర్పర్చదు. ఈ హాలైడ్లు sp³d సంకరీకరణంతో ట్రైగోనల్ బై పిరమిడల్ నిర్మాణంలో ఉంటాయి.
4) ఆక్సిజన్ తో చర్య :
ఈ గ్రూపు మూలకాలు E2O3 మరియు E2O5 అను ఆక్సైడ్లను ఏర్పరుస్తాయి.
ఉదా : P2O3 మరియు P2O5.
కాని నైట్రోజన్ కు pπ-pπ బహు బంధాలను ఏర్పర్చే సామర్థ్యం ఉండుట వలన ఇది +1 నుండి +5 ఆక్సీకరణ స్థితులు గల అనేక ఆక్సైడ్లను ఏర్పరుస్తుంది.
ఉదా : N2O, NO, N2O3, NO2, N2O4, N2O5 E2O5 ఆక్సైడ్లు E2O3 ఆక్సైడ్ కంటే బలమైన ఆమ్లాలు. గ్రూపులో క్రిందికి పోయే కొలది ఆమ్ల స్వభావం తగ్గుతుంది.
ప్రశ్న 3.
ఈ క్రింది వానితో P4 ఏ విధంగా చర్య జరుపుతుంది?
(a) SOCl2 (b) SO2Cl2?
జవాబు:
(a) SOCl2 తో చర్య :
P4 + 8SOCl2 → 4PCl3 + 4SO2 + 2S2Cl2
(b) SO2Cl2 తో చర్య :
P4 + 10SO2Cl2 → 4PCl5 + 10SO2
ప్రశ్న 4.
15వ గ్రూపులోని నైట్రోజన్ యొక్క అసంగత ధర్మాన్ని వివరించండి.
జవాబు:
15వ గ్రూపు మూలకాలలో నైట్రోజన్ మిగిలిన మూలకాలన్నింటి కంటే అసంగత ప్రవర్తన కలిగి ఉంటుంది. ఈ భేదానికి గల కొన్ని ముఖ్యమైన కారణాలు ఈ క్రింది ఇవ్వబడినవి.
i) విభిన్నమైన అల్ప పరిమాణం
ii) అధిక ఋణవిద్యుదాత్మకత
iii) అధిక అయనీకరణ ఎంథాల్పీ
iv) వేలన్సీ స్థాయిలో d-ఆర్బిటాల్లు లేకపోవుట.
కొన్ని అసంగత ధర్మాలు:
- నైట్రోజన్ pπ-pπ బంధాలను ఏర్పరుస్తుంది. మిగిలినవి ఏర్పర్చవు.
- నైట్రోజన్ యొక్క కాటనేషన్ ధర్మం ఫాస్ఫరస్ కంటే తక్కువ.
- నైట్రోజన్ జడత్వంగా ఉండి మూలక స్థితిలో చర్యలలో పాల్గొనదు.
- నైట్రోజన్ గరిష్ట సంయోజకత 4 ను ప్రదర్శిస్తుంది.
కాని మిగిలిన మూలకాలు వాటి సంయోజకతను 6 కు విస్తరించుకుంటాయి. - అధిక ఋణవిద్యుదాత్మకత కారణంగా నైట్రోజన్ ఈ గ్రూపు మూలకాలన్నింటి కంటే అత్యంత అలోహము.
- నైట్రోజన్ యొక్క హైడ్రైడ్ (NH3) స్థిరమైనది కాని మిగిలిన మూలకాల హైడ్రైడ్లు అస్థిరమైనవి.
![]()
ప్రశ్న 5.
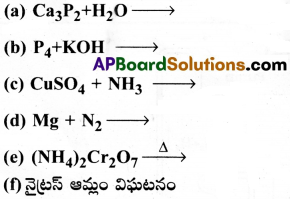
క్రింది చర్యలను పూర్తి చేయండి.
జవాబు:
a) Ca3P2 + 6H2O → 3Ca(OH)2 + 2PH3 ↑
b) P4 + 3H2O + 3KOH → PH3 ↑ + 3KH2PO2
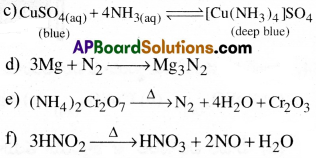
ప్రశ్న 6.
క్రింది వాటితో PCI ఏ విధంగా చర్య జరుపుతుంది? [AP 20]
(a) నీరు (b) C2H5OH (c) CH3COOH (d) Ag
జవాబు:
a) PCl5 + H2O → POCl3 + 2HCl
PCl5 + 4H2O → H3PO4 + 5HCl
b) C2H5OH + PCl5 → C2H5Cl + POCl3 + HCl
c) CH3COOH + PCl5 → CH3COCl + POCl3 + HCl
d) PCl5 + 2Ag → 2AgCl + PCl3
ప్రశ్న 7.
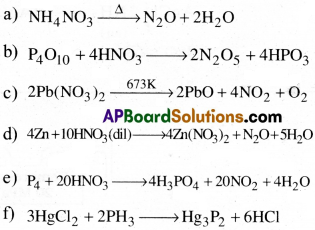
క్రింది చర్యలను పూర్తిచేయండి:
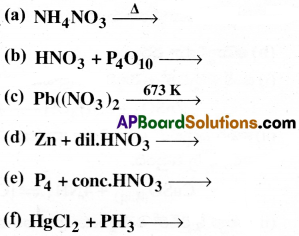
జవాబు:
Long Answer Questions (దీర్ఘ సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
హేబర్ విధానంలో అమ్మోనియాను ఎలా తయారు చేస్తారు? అమ్మోనియా ఈ క్రింది వానితో జరుపు చర్యలను వివరింపుము. [AP 15,18,19][TS 17,20]
![]()
జవాబు:
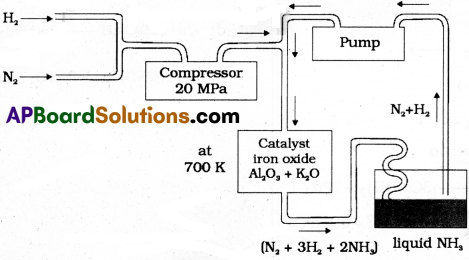
(a) హేబర్ విధానంలో అమ్మోనియా తయారీ విధానం:
- హేబర్ విధానం లీచాల్లియర్ నియమం పై ఆధారపడును.
- హేబరు విధానంలో అధిక మొత్తంలో అమ్మోనియా తయారీకి 1:3 నిష్పత్తిలో N2 మరియు H2 ల మిశ్రమంను ఉపయోగిస్తారు.
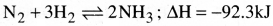
- ఇది ఒక ద్విగత చర్య. పురోగామి చర్య ఉష్ణమోచక చర్య. ఘనపరిమాణం తగ్గు దిశలో చర్య జరుగుతుంది.
- లీచాల్లీయర్ నియమం ప్రకారం అధిక మొత్తంలో అమ్మోనియా దిగుబడికి అల్ప ఉష్ణోగ్రత మరియు అధిక పీడనాలు అవసరము. కాని తక్కువ ఉష్ణోగ్రత వద్ద చర్య చాలా నెమ్మదిగా జరుగును.
- అనువైన పరిస్థితులు: (a) ఉష్ణోగ్రత: 725-775K (b) పీడనం: 200-300 atm
- ఉత్ప్రేరకం: ఐరన్ ఆక్సైడ్కు కొద్దిగా K2O మరియు Al2O3 కలిపిన మిశ్రమం.
- విధానం: శుద్ధమైన పొడి N2 మరియు H2 ల మిశ్రమమును 300 అట్మా.ల పీడనం వద్ద సంపీడ్యం చెందించి. ఆ మిశ్రమంను 725-775K వద్ద వేడి చేసి ఉత్ప్రేరకం మీదగా పంపుతాయి. అప్పుడు అమ్మోనియా ఏర్పడుతుంది. ఏర్పడిన అమ్మోనియాను ద్రవరూపంలోనికి మార్చి చర్యా మిశ్రమం నుంచి వేరుచేస్తారు.
(b) అమ్మోనియా చర్యలు:
(i) జింక్ సల్ఫేట్తో అమ్మోనియా ద్రావణం చర్య జరిపి జింక్ హైడ్రాక్సైడ్ అనే తెల్లని అవక్షేపాన్ని ఇస్తుంది.
ZnSO4 + 2NH4OH → Zn(OH)2 + (NH4)2SO4 (అమ్మోనియం సల్ఫేట్)
(ii) కాపర్ సల్ఫేట్తో అమ్మోనియా ద్రావణం చర్య జరిపి టెట్రా అమైన్ కాపర్ (II) సల్ఫేట్ అనే ముదరు నీలిరంగు సంక్లిష్టాన్ని ఇస్తుంది.
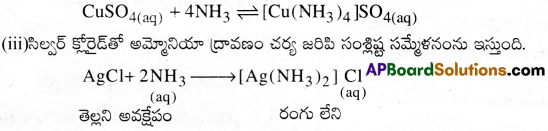
![]()
ప్రశ్న 2.
ఆస్ట్రాల్ద్ విధానంలో నైట్రికామ్లంను ఏలా తయారు చేస్తారు? ఇది ఈ క్రింది వాటితో HNO3 ఏలా చర్య జరుపుతుంది.
(a) కాపర్ (b) Zn (c) S8 (d) P4 [TS 19,22][AP 17]
జవాబు:
(a) ఆస్ట్రాల్ద్ విధానంలో నైట్రికామ్లం తయారీ మూడు దశలలో జరుగును: [AP 22]
దశ-1 : NH3 వాతావరణంలోని ఆక్సీజన్తో ఉత్ప్రేరక ఆక్సీకరణం చెందుతుంది.

నత్రికామ్లంను మూడు దశలలో గాఢత చెందిస్తారు.
- 68% HNO3 వచ్చు వరకు స్వేదనం చేస్తారు.
- గాఢ. H2SO4 ను కలిపి స్వేదనం చేయగా 98% HNO3 లభిస్తుంది.
- 98% HNO3 ను శీతలీకరణ మిశ్రమంలో చల్లబరిస్తే 100% శుద్ధ HNO3 స్ఫటికాలు వేరవుతాయి.
(b) నత్రికామ్లం చర్యలు:
i) (a) కాపర్ సజల నైట్రిక్ ఆమ్లంతో చర్య జరిపి నైట్రిక్ ఆక్సైడ్ను ఇస్తుంది.
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
(b) కాపర్తో గాఢ నైట్రిక్ ఆమ్లంతో చర్య జరిపి నైట్రోజన్ డై ఆక్సైడ్ను ఇస్తుంది.
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
ii) (a)సజల నైట్రిక్ ఆమ్లం జింక్ తో చర్య జరిపి N2O ను ఇస్తుంది.
4Zn + 10HNO3 → 4Zn(NO3)2 + 5H2O + N2O
(b) జింక్ గాఢ నైట్రిక్ ఆమ్లంతో చర్య జరిపి నైట్రోజన్ డై ఆక్సైడ్ను ఇస్తుంది.
Zn + 4HNO3 → Zn(NO3)2 + 2H2O + 2NO2
iii) నైట్రిక్ ఆమ్లం సల్ఫర్ను సల్ఫ్యురిక్ ఆమ్లంగా ఆక్సీకరిస్తుంది.
S8 + 48HNO3 → 8H2SO4 + 48NO2 + 16H2O
iv) నైట్రిక్ ఆమ్లం ఫాస్ఫరస్ ను ఫాస్ఫారిక్ ఆమ్లంగా ఆక్సీకరిస్తుంది.
P4 + 20HNO3 → 4H3PO4 + 20NO2 + 4H2O
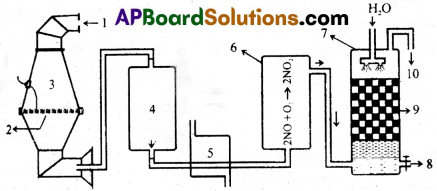
ఆస్ట్వాల్డ్ విధానంలో నైట్రికామ్లం తయారీ విధానం
- అమ్మోనియా, ఆక్సిజన్ మిశ్రమం
- ప్లాటినం వల
- ఉత్ప్రేరకం గది
- అల్యూమినియం లేదా క్రోమియం స్టీల్ పాత్ర (cooling tower)
- బాయిలర్
- ఆక్సీకరణ గది
- శోషణ టవర్
- 61% HNO3
- ఇటుకల చకర్ల గదులు
- O2 తో కలిసి ఉన్న చర్య నొందని NO