Students get through AP Inter 2nd Year Chemistry Important Questions Lesson 6(b) 16వ గ్రూపు మూలకాలు which are most likely to be asked in the exam.
AP Inter 2nd Year Chemistry Important Questions Lesson 6(b) 16వ గ్రూపు మూలకాలు
Very Short Answer Questions (అతిస్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
డై ఆక్సిజన్ వాయువు, కాని సల్ఫర్ ఘన పదార్థం. ఎందువలన?
జవాబు:
అల్ప పరమాణు పరిమాణం మరియు అధిక ఋణవిద్యుదాత్మకత వలన ఆక్సిజన్ pπ-pπ బహు బంధాలను ఏర్పర్చుకుంటుంది. దీని ఫలితంగా ఆక్సిజన్ ద్విపరమాణుక అణువుగా ఉంటుంది. ఈ అణువులు వాండర్ బలాలుచే బంధితమై ఉంటాయి. కావున గది ఉష్ణోగ్రత వద్ద (O2) వాయువుగా ఉంటుంది.
అధిక పరమాణు పరిమాణం మరియు అల్ప ఋణవిద్యుదాత్మకత కారణంగా సల్ఫర్ pπ-pπ బహు బంధాలను ఏర్పర్చలేదు. ఇది కేవలం S-S ఏకా బంధాలను మాత్రమే ఏర్పరుస్తుంది. అధిక కాటనేషన్ ధర్మం కారణంగా S8 అణువుగా ఉంటుంది. కావున గది ఉష్ణోగ్రత వద్ద సల్ఫర్ ఘన పదార్థంగా ఉంటుంది.
ప్రశ్న 2.
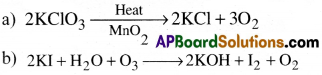
(a) KClO3 ను MnO3 తో వేడి చేసినపుడు
(b) O3 ని KI ద్రావణంలోకి పంపించినపుడు ఏమి జరుగుతుంది?
జవాబు:
ప్రశ్న 3.
ద్విస్వభావ మరియు తటస్థ ఆక్సైడ్లకు ఒక్కో దానికి రెండేసి ఉదాహరణలను ఇవ్వండి.
జవాబు:
ద్వి స్వభావ ఆక్సైడ్లు : TeO2,PoO2
తటస్థ ఆక్సైడ్లు : N2O, NO
ప్రశ్న 4.
సాధారణంగా ఆక్సిజన్ -2 ఆక్సీకరణ స్థితిని మాత్రమే ప్రదర్శిస్తుంది. కాని ఈ గ్రూపులో మిగిలిన మూలకాలు +2,+4, +6 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తాయి. వివరించండి.
జవాబు:
ఆక్సిజన్కు అధిక ఋణవిద్యుదాత్మకత ఉండుట వలన ఇది ఋణ ఆక్సీకరణ స్థితి -2 ను మాత్రమే ప్రదర్శిస్తుంది. (OF2 లో మాత్రమే దీనికి +2 ఆక్సీకరణ స్థితి ఉంటుంది).
ఈ గ్రూపులో మిగిలిన మూలకాలకు అల్పఋణ విద్యుదాత్మకత మరియు ఖాళీ d-ఆర్బిటాల్లు అందుబాటులో ఉండుట వలన ఇవి +2, +4 మరియు +6 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తాయి.
ప్రశ్న 5.
ఆక్సిజన్ –2 ఆక్సీకరణ స్థితి కాకుండా భిన్న ఆక్సీకరణ స్థితిని ప్రదర్శించే ఏవైన రెండు సమ్మేళనాలను తెల్పండి. ఆ సమ్మేళనాలలో ఆక్సిజన్ యొక్క ఆక్సీకరణ స్థితిని తెల్పండి.
జవాబు:
O2F2 లో ఆక్సిజన్ యొక్క ఆక్సీకరణ స్థితి +1
OF2 లో ఆక్సిజన్ యొక్క ఆక్సీకరణ స్థితి +2
![]()
ప్రశ్న 6.
ఆక్సిజన్ యొక్క అణుఫార్ములా O2 గా ఉంటే సల్ఫర్ యొక్క అణుఫార్ములా S8గా ఉంటుంది. వివరించండి.
జవాబు:
అల్ప పరమాణు పరిమాణం మరియు అధిక ఋణ విద్యుదాత్మకత కారణంగా ఆక్సిజన్ pπ-pπ బహు బంధాలను ఏర్పర్చుకుంటుంది. దీని ఫలితంగా ఆక్సిజన్ ద్విపరమాణుక అణువు (O2) గా ఉంటుంది.
అధిక పరమాణు పరిమాణం మరియు అల్ప బుణ విద్యుదాత్మకత కారణంగా సల్ఫర్ pπ-pπ బహు బంధాలను ఏర్పర్చుకోలేదు. ఇది కేవలం S-S ఏక బంధాలను మాత్రమే ఏర్పరుస్తుంది. అంతేకాకుండా సల్ఫర్కు ఉన్న అధిక కాటనేషన్ సామర్థ్యం కారణంగా ఇది అష్టపరమాణుక (S8) అణువుగా ఉంటుంది. ఇది మడతలు వలయ నిర్మాణంను కలిగి ఉంటుంది.
ప్రశ్న 7.
H2O ద్రవం, కాని H2S వాయువు. వివరించండి. [IPE ’14]
జవాబు:
H2O అణువుల మధ్య హైడ్రోజన్ బంధాలు ఉంటాయి. అందువల్ల H2O సహచరిత ద్రవంగా ఉంటుంది.
H2S అణువుల మధ్య హైడ్రోజన్ బంధాలు లేకపోవుట వలన గది ఉష్ణోగ్రత వద్ద H2S వాయువు. అధిక పరమాణు పరిమాణం మరియు అల్పఋణ విద్యుదాత్మకత కారణంగా సల్ఫర్ పరమాణు H2S తో హైడ్రోజన్ బంధాలను ఏర్పర్చదు.
ప్రశ్న 8.
H2O కి తటస్థ స్వభావం ఉంటే H2S కి ఆమ్ల స్వభావం ఉంటుంది. వివరింపుము.
జవాబు:
O పరమాణువు కంటే S- పరమాణువు యొక్క పరిమాణం అధికం. అందువల్ల O-H బంధం కంటే S-H బంధం బలహీనమైనది. ఈ కారణంగా జల ద్రావణంలో H2S విఘటనం చెంది H+ అయాన్లను ఇస్తుంది. కావున H2S కి ఆమ్ల స్వభావం ఉంటుంది.
ప్రశ్న 9.
భూపటలంపై అత్యంత సమృద్ధిగా లభించే మూలకం యొక్క పేరు.
జవాబు:
భూపటలంపై అత్యంత సమృద్ధిగా లభించే మూలకం ఆక్సిజన్.
ప్రశ్న 10.
16వ గ్రూపు మూలకాల్లో అత్యధిక కాటనేషన్ ఉన్న మూలకం ఏది?
జవాబు:
బలమైన S-S బంధం ఉండుట వలన 16వ గ్రూపు మూలకాల్లో సల్ఫర్ అత్యధిక కాటనేషన్ ధర్మాన్ని కలిగి ఉంటుంది.
ప్రశ్న 11.
చాల్కోజన్ హైడ్రైడ్లలో అత్యంత బలమైన ఆమ్లం మరియు అత్యంత స్థిరమైన హైడ్రైడ్లు ఏవి?
జవాబు:
అత్యంత ఆమ్ల హైడ్రైడ్ : H2Te(హైడ్రోజన్ టెల్లూరైడ్)
అత్యంత స్థిరమైన హైడ్రైడ్ : H2O (హైడ్రోజన్ మోనాక్సైడ్)
![]()
ప్రశ్న 12.
ఈ క్రింది వానిలో సల్ఫర్ యొక్క సంకరీకరణాన్ని తెల్పండి. [AP 20]
(a) SO2 (b) SO3 (c) SF4 (d) SF6
జవాబు:
(a) SO2 – sp²
(b) SO3 – sp²
(c) SF4 – sp³d
(d) SF6 – sp³d²
ప్రశ్న 13.
సల్ఫర్ యొక్క ఏవైన రెండు ఆక్సోఆమ్లాల పేర్లను, వాటి ఫార్ములాలను వ్రాయండి. వాటిలో సల్ఫర్ ఆక్సీకరణ స్థితిని తెల్పండి.
జవాబు:
(i) సల్ఫ్యూరస్ ఆమ్లం
ఫార్ములా : H2SO3 ఆక్సీకరణ స్థితి : +4
(ii) సల్ఫ్యూరిక్ ఆమ్లం
ఫార్ములా : H2SO4 ఆక్సీకరణ స్థితి: +6
ప్రశ్న 14.
SF4 మరియు SF6 ల నిర్మాణాలను వివరింపుము.
జవాబు:
SF4 లో సల్ఫర్ sp³d సంకరీకరణంలో పాల్గొంటుంది. మరియు ట్రైగోనల్ బైపిరమిడల్ ఆకృతిని కలిగి ఈక్విటోరియల్ స్థానం నుందు ఒక ఒంటరి ఎలక్ట్రాన్ జంటను కలిగి ఉంటుంది. దీనినే సి-సా నిర్మాణం అంటారు.
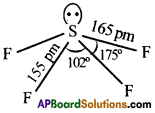
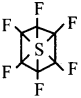
SF6 లో సల్ఫర్ sp³d² సంకరీకరణంను ప్రదర్శించి అష్టముఖి నిర్మాణంను కలిగి ఉంటుంది.
ప్రశ్న 15.
క్రింది ఒక్కొక్కదానికి రెండేసి ఉదాహరణలివ్వండి.
(a) తటస్థ ఆక్సైడ్
(b) పెరాక్సైడ్
(c) సూపర్ ఆక్సైడ్
జవాబు:
(a) తటస్థ ఆక్సైడ్ : NO, N2O, CO, H2O
(b) పెరాక్సైడ్ : H2O2, BaO2, Na2O2
(c) సూపర్ ఆక్సైడ్ : KO2, RbO2, CsO2.
ప్రశ్న 16.
“టెయిలింగ్ ఆఫ్ మెర్క్యురీ ” అనగా నేమి? దీనిని ఎలా తొలగిస్తారు. [AP15,17] [TS 15,18,22]
జవాబు:
ఓజోన్ సమక్షంలో మెర్క్యురీ Hg2O ను ఏర్పరుస్తుంది. దీని కారణంగా మెర్క్యురీ తన లోహ కాంతిని, ద్రవ మట్టాన్ని కోల్పోయి, గాజుగొట్టం గోడలకు అంటుకోవ డాన్ని “టెయిలింగ్ ఆఫ్ మెర్క్యురీ అంటారు. దీనిని నీటితో కడిగితే అది కోల్పోయిన లోహ కాంతిని, ద్రవ మట్టాన్ని మళ్ళీ తిరిగి పొందుతుంది.
![]()
ప్రశ్న 17.
ఓజోన్ వాయువును పరిమాణాత్మకంగా నిర్ణయించే సూత్రమును వ్రాయుము.
జవాబు:
ఓజోన్ను అధిక KI జల ద్రావణంనకు కలుపగా I2 విడుదలగును.దీనిని ప్రమాణ Na2S2O3 ద్రావణంతో పిండి(స్టార్చ్)ని సూచిక ఉపయోగించి అంశమాపనం చేస్తారు. హైపో ద్రావణం నుండి I2 ను మరియు I2 నుండి ఓజోన్ లెక్కిస్తారు.
ప్రశ్న 18.
ఓజోన్ నిర్మాణాన్ని వ్రాయండి.
జవాబు:
ఓజోన్ అణువులో కేంద్రక పరమాణువు ఆక్సిజన్ sp² సంకరీకరణంను పొంది ఒక ఒంటరి ఎలక్ట్రాన్ జంటను కలిగి ఉండును. దీని ఫలితంగా ఓజోన్ కోణీయ నిర్మాణంతో 117° బంధకోణంను కలిగి ఉండును. నిజానికి ఇది ఈ రెండు రెజోనెన్స్ నిర్మాణంల సంకర రూపం.
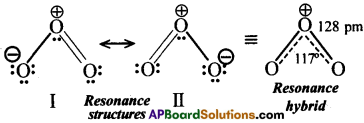
ప్రశ్న 19.
SO2 ని ఆంటిక్లోర్గా ఉపయోగిస్తారు. వివరించండి.
జవాబు:
బట్టల నుండి విరంజనం తరువాత క్లోరిన్ను తొలగించుటకు SO2 ను ఆంటిక్లోర్గా ఉపయోగిస్తారు. Cl2 ను తొలగించే చర్యలో ఇది క్లోరిన్ ను HCl గా క్షయకరించ [AP22][TS 19]
Cl2 + SO2 + 2H2O → 2HCl + H2SO4
ప్రశ్న 20.
ఓజోన్ ను ఏవిధంగా గుర్తిస్తారు?
జవాబు:
- స్టార్చ్ అయొడైడ్ కాగితంను ఓజోన్ నీలి రంగు లోనికి మారుస్తుంది.
- ఓజోన్ సమక్షంలో మెర్క్యురి ద్రవ మట్టాన్ని కోల్పోయి గాజును అంటుకొంటుంది.
- ఓజోన్ క్షారయుత బెంజిడిన్ ద్రావణంను జేగురుగా మారుస్తుంది.
ప్రశ్న 21.
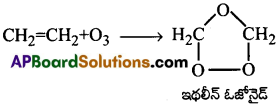
ఇథిలీన్ ఓజోన్ ఏ విధంగా చర్యనొందును?
జవాబు:
CCl4 వంటి జడ ద్రావణి సమక్షంలో 195K వద్ద ఓజోన్ వాయువును CH2 = CH2 లోనికి పంపిన, ఓజోనైడ్ ఏర్పడుతుంది.
ప్రశ్న 22.
O3 మరియు O2లలో ఏది పరాయస్కాంత పదార్థం?
జవాబు:
O3 మరియు O2లలో O2 పరాయస్కాంత పదార్థం.
ప్రశ్న 23.
O3, O2 లలో ఏది మంచి ఆక్సీకరణి. ఎందువల్ల?
జవాబు:
విఘటనం చెందినపుడు ఓజోన్ తేలికగా నవజాత ఆక్సిజన్ను విడుదల చేస్తుంది. అందువలన O3 మరియు O2 లలో O3 మంచి ఆక్సీకరణి కారకం.
O3 → O2 + (0)
![]()
ప్రశ్న 24.
O3 మరియు H2SO4 కు ఒక్కొక్కదానికి ఏవైనా రెండు ఉపయోగాలను వ్రాయండి.
జవాబు:
ఓజోన్ (O3) యొక్క ఉపయోగాలు:
- ఓజోన్ ను క్రిమిసంహారిణి గాను, సంక్రమణ వ్యాధుల నిరోధిగాను ఉపయోగిస్తారు.
- నీటిని శుభ్రపర్చుటకు ఉపయోగిస్తారు.
H2SO4 యొక్క ఉపయోగాలు:
- H2SO4ను పెట్రోలియం శుద్ధి చేయుటకు ఉపయోగిస్తారు.
- దీనిని డిటర్జెంట్ల తయారీ పరిశ్రమలో ఉపయోగిస్తారు.
ప్రశ్న 25.
సల్ఫర్ యొక్క ఏ రూపము పరాయస్కాంత ధర్మాన్ని ప్రదర్శిస్తుంది?
జవాబు:
అధిక ఉష్ణోగ్రతలు (దాదాపు 1000K) వద్ద సల్ఫర్ S2 అణువుగా ఉండును. ఇది O2 వలె పరాయస్కాంత ధర్మాన్ని ప్రదర్శిస్తుంది.
ప్రశ్న 26.
SO2 ఉనికిని ఏవిధంగా గుర్తిస్తారు?
జవాబు:
ఆమీకృత KMnO4 ద్రావణం యొక్క పింక్ వర్ణంను SO2 వివర్ణం చేయును.
2KMnO4 + 5SO2 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
ప్రశ్న 27.
16వ గ్రూపు మూలకాలను ఎందువలన చాల్కోజన్లు అని పిలుస్తారు?
జవాబు:
16 వ గ్రూపులో మొదటి నాలుగు మూలకాలు (O, S, Se, Te)ను చాల్కోజన్లు అంటారు. కారణం ఇవి లోహ ధాతువులను ఏర్పర్చే మూలకాలు.
ప్రశ్న 28.
చాల్కోజన్లలో వేటికి అత్యధిక ఋణవిద్యుదాత్మకత మరియు వేటికి అత్యధిక ఎలక్ట్రాన్ ఎఫినిటి ఉంటుంది?
జవాబు:
చాల్కోజన్లలో అత్యధిక ఋణ విద్యుదాత్మకత మూలకం ఆక్సిజన్. అధిక ఎలక్ట్రాన్ ఎఫినిటి మూలకం సల్ఫర్.
ప్రశ్న 29.
16వ గ్రూపు మూలకాల హైడ్రైడ్లలో వేటికి అత్యధిక భాష్పీభవన స్థానం మరియు అత్యల్ప ఆమ్ల స్వభావం ఉంటుంది?
జవాబు:
బలమైన అంతరణుక హైడ్రోజన్ బంధాల వలన H2Oకు అత్యధిక బాష్పీభవన స్థానం కలదు. O-H బంధ ధైర్ఘ్యం తక్కువగా ఉండటం వలన H2O బలహీనమైన ఆమ్లం.
Short Answer Questions (స్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
O, S, Se, Te మరియు Po మూలకాల స్థానాలను ఆవర్తన పట్టికలో ఎలక్ట్రాన్ విన్యాసం, ఆక్సీకరణ స్థితులు మరియు హైడ్రైడ్లను ఏర్పరచే సమర్థత ఆధారంగా ఏవిధంగా నిర్ధేశించారు.
జవాబు:
i) ఎలక్ట్రాన్ విన్యాసం :
ఈ మూలకాలన్నియు ఒకే సాధారణ బాహ్య ఎలక్ట్రాన్ విన్యాసం ns²-np4ను కలిగి ఉండుట కారణంగా వీటిని 16వ గ్రూపులో చేర్చుట సమంజసమే.
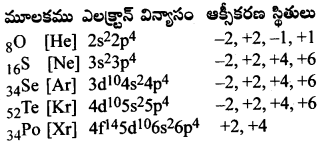
ii) ఆక్సీకరణ స్థితులు :
మనం గమనించిన విధంగా 16వ గ్రూపు మూలకాలన్నింటి యొక్క సాధారణ ఆక్సీకరణ స్థితి -2 కాకుండా S, Se మరియు Te లు +4 మరియు +6 ఆక్సీకరణ స్థితులను ప్రదర్శిస్తాయి. ‘d’ ఆర్బిటాల్లు లేని కారణంగా ఆక్సిజన్ +4 మరియు +6 ఆక్సీకరణ స్థితులను ప్రదర్శించదు.
పైన వివరించిన విధంగా ఈ మూలకాల కనిష్ట మరియు గరిష్ట ఆక్సీకరణ స్థితులను ఆధారంగా వీటిని 16వ గ్రూపులో ఉంచటం సమంజసం.
iii) హైడ్రైడ్లను ఏర్పర్చుట :
ఈ గ్రూపు మూలకాలన్ని EH2 అను సాధారణ ఫార్ములా గల హైడ్రైడ్లను ఏర్పరుస్తాయి. అనగా H2O, H2S, H2Se, H2,Te మరియు H2P0. కనుక ఈ మూలకాలను ఒకే గ్రూపు అనగా 16వ గ్రూపులో ఉంచటం సమంజసమే.
![]()
ప్రశ్న 2.
H2SO4ను స్పర్శ (కాంటాక్ట్) విధానంలో ఏవిధంగా తయారు చేస్తారు. [TS-15,16]
జవాబు:
స్పర్శ విధానం దశలు:
i) SO2 ఉత్పత్తి :
చూర్ణ స్థితిలో ఉన్న సల్ఫరన్ను గాలి సమక్షంలో మండించుట ద్వారా (లేక) సల్ఫర్ అధికంగా కలిగిన ధాతువును భర్జనం చేయుట దీనిని తయారు చేస్తారు.
S8 + 😯2 → 8SO2
4FeS2 + 11O2 → 2Fe2O3 + 8SO2.
ii) సల్ఫర్ డై ఆక్సైడ్, సల్ఫర్ ట్రై ఆక్సైడ్గా ఆక్సీకరణం చెందుట:
![]()
స్పర్శ విధానంలో ఇది ప్రధానమైన దశ.
SO3 అధిక దిగుబడికి అవసరమైన పరిస్థితులు
ఉష్ణోగ్రత = 400 – 450°C
పీడనం = 1.5 to 2 atm
ఉత్ప్రేరకం = Pt, ఆస్బెస్టాస్ లేదా V2O5.
iii) SO3 ని H2SO4గా మార్చుట :
SO3 ని గాఢ H2SO4లోకి అధిశోషణంగావిస్తే ఓలియమ్ (లేదా) ఫైరో సల్ఫ్యూరిక్ ఆమ్లం లభిస్తుంది.
SO3 + H2SO4(గాఢ) → H2S2O7 (ఓలియమ్)
SO3ని నీటిలోకి అధిశోషణం చేయకూడదు. కారణం SO3 మరియు నీటి మధ్య చర్య అధిక ఉష్ణమోచక చర్య మరియు SO3 నీటితో ఆమ్ల బిందువులు గల పొగ మంచును ఏర్పర్చుకొనును. కొన్ని సందర్భాలలో ఈ ప్రక్రియను చేయుట చాలా కష్టతరం.
iv) ఓలియమ్ను విలీనం చేసి H2SO4 ను ఏర్పర్చుట :
ఓలియమ్ను లెక్కించిన పరిమాణంలో సజలం చేసి కావలసిన గాఢతలలో H2SO4 ను పొందుతారు.
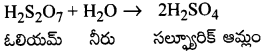
ప్రశ్న 3.
ఓజోన్ను ఎలా తయారు చేస్తారు? ఈ క్రింది వానితో ఓజోన్ ఎలా చర్యనొందునో తెల్పుము? [AP-16]
(a) PbS (b) KI (c) Hg (d) Ag
జవాబు:
నిశ్శబ్ద విద్యుదుత్సర్గం ద్వారా అనార్ధ్ర ఆక్సిజన్ ను ప్రవాహంలా పంపినట్లైతే ఆక్సిజన్ ఓజోన్గా (10%) మార్పు చెందుతుంది.
ఏర్పడిన ఉత్పన్నాన్ని ఓజోనైజ్డ్ ఆక్సిజన్ అంటారు.
3O2 → 2O3; ∆H(298K) = +142 kJ mol-1.
ఆక్సిజన్ నుండి ఓజోన్ ఏర్పడే చర్య ఉష్ణగ్రాహక ప్రక్రియ. కాబట్టి ఆక్సిజన్ వియోగాన్ని నివారించుటకు నిశ్శబ్ద విద్యుదుత్సర్గాన్ని తప్పనిసరిగా ఉపయోగిస్తారు.
a) PbS + 4O3 → PbSO4 + 4O2
b) 2KI(aq) +H2O(l) + O3(g) → 2KOH(aq) + I2(s) + O2(g)
c) 2Hg + O3 → Hg2O + O2
d) 2Ag + O3 → Ag2O + O2
ప్రశ్న 4.
సల్ఫర్ రూపాంతరతను గురించి లఘు వ్యాఖ్య వ్రాయుము.
జవాబు:
- సల్ఫర్ ఏర్పరిచే అనేక రూపాంతరాలలో పసుపు రాంబిక్ సల్ఫర్ (α-సల్ఫర్) మరియు మోనోక్లినిక్ సల్ఫర్(β- సల్ఫర్) లు అతి ముఖ్యమైనవి.
- గది ఉష్ణోగ్రత వద్ద స్థిరంగా ఉండే రాంబిక్ సల్ఫర్ను 369K కంటే హెచ్చు ఉష్ణోగ్రతకు వేడి చేస్తే అది మోనోక్లినిక్ సల్ఫర్గా పరివర్తనం చెందుతుంది.
- మరొక ముఖ్యమైన రూపాంతరము వలయ-S6 (ఎంజెల్ సల్ఫర్ లేదా E-సల్ఫర్). ఇది ఆరు పరమాణువుల కుర్చీ వలయ ఆకారంలో ఉండును.
ప్రశ్న 5.
SO2 ఈ క్రింది వాటితో ఏవిధంగా చర్య జరుపుతుంది. [TS 22]
(a) Na2SO3 (b) Cl2 (c) Fe+3 అయాన్లు (d) KMnO4
జవాబు:
a) Na2SO3(aq) + SO2(g) + H2O(l) → 2NaHSO3(aq)
b) SO2 + Cl2 → SO2Cl2
c) SO2 + Fe2(SO4)3 + 2H2O → 2FeSO4 + 2H2SO4
d) 2KMnO4 + 5SO2 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
![]()
ప్రశ్న 6.
మూలక సల్ఫర్ నుంచి ప్రారంభించి H2SO4 ని ఎలా తయారు చేస్తారు?
జవాబు:

ప్రశ్న 7.
SO-24 మరియు SO3 ల నిర్మాణాలను వర్ణించండి.
జవాబు:
సల్ఫేట్ అయాన్ నందు సల్ఫర్ sp³ సంకరీకరణంలో పాల్గొనును. కనుక ఇది చతుర్ముఖీయ ఆకారం కలిగి ఉండును. సల్ఫేట్ అయాన్లో అన్ని S-O బంధ దూరాలు సమానం. కనుక సల్ఫేట్ అయాన్ ఈ క్రింది రెజోనెన్స్ రూపాల సంకర నిర్మాణం.
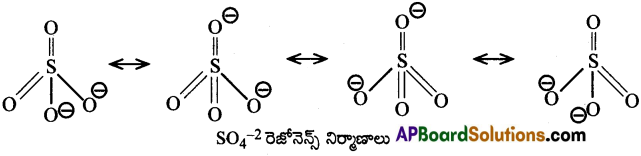
SO3 అణువులో సల్ఫర్ sp² సంకరీకరణంలో పాల్గొంటుంది. సల్ఫర్లోని మూడు sp²-ఆర్బిటాల్లు మూడు ఆక్సిజన్ పరమాణువులలోని p-ఆర్బిటాల్లతో అతిపాతం జరిపి మూడు సిగ్మా S-O బంధాలు ఏర్పర్చును. ఇప్పుడు సల్ఫర్ వద్ద ఒక శుద్ధ p ఆర్బిటాల్, రెండు d-ఆర్బిటాల్ను కలిగి ఉంటుంది. ఇవి మూడు ఆక్సిజన్ పరమాణువులోని p-ఆర్బిటాళ్ళలలో అతిపాతం జరిపి మూడు π-బంధాలను ఏర్పర్చును. అన్ని S-O బంధ దూరాలు సమానం. కనుక SO3 మూడు రెజోనెన్స్ నిర్మాణాలలో ఉండును. గది ఉష్ణోగ్రత వద్ద వాయుస్థితిలోని SO3 అణువు సమతల త్రిభుజాకారంలో ఉండును.
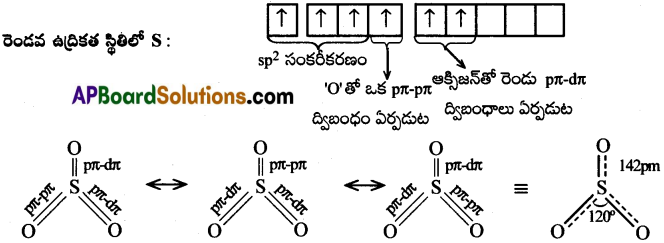
ప్రశ్న 8.
సల్ఫర్ యొక్క ఏ ఆక్సైడ్ ఆక్సీకరణిగాను మరియు క్షయకరణిగాను పనిచేస్తుంది? ఒక్కొదానికి ఒక ఉదాహరణనిమ్ము?
జవాబు:
తేమ సమక్షంలో SO2 మంచి క్షయకరణిగా పనిచేస్తుంది.
Cl2 + SO2 + 2H2O → 2HCl + H2SO4
2Fe+3 + SO2 + 2H2O → 2Fe+2 + SO2 + 4H+
SO2 ప్రధానంగా బలమైన క్షయకరణ కారకాలతో చర్య నొందినపుడు బలహీనమైన ఆక్సీకరణిగా పనిచేస్తుంది.
2H2S + SO2 → 2H2O + 3S
2SnCl2 + SO2 + 4HCl → 2SnCl4 + 2H2O + S
ప్రశ్న 9.
H2SO4 స్పర్శ విధానంలో SO2 నుండి SO3 ఏర్పడటానికి అనుకూలమైన పరిస్థితులను వివరింపుము
జవాబు:
సల్ఫ్యూరిక్ ఆమ్లం తయారీలో SO2, O2తో V2O5 (ఉత్ప్రేరకం) సమక్షంలో ఉత్ప్రేరక ఆక్సీకరణం చెంది SO్కని ఇస్తుంది. ఇది ప్రధానమైన దశ.
![]()
ఈ చర్య ఉష్ణమోచక చర్య, ద్విగత చర్య మరియు పురోగామి చర్య. దీని వలన ఘనపరిమాణంను తగ్గించే దిశ. SO3 అధిక దిగుబడికి అల్ప ఉష్ణోగ్రత మరియు అధిక పీడనాలు అనువైన పరిస్థితులు. కాని అల్ప ఉష్ణోగ్రత వద్ద చర్యా వేగం చాలా నెమ్మదిగా ఉంటుంది. కావున ప్రయోగంను 2 బార్ల పీడనం మరియు 720 K ఉష్ణోగ్రత వద్ద జరుపుతారు.
ప్రశ్న 10.
ఈ క్రింది చర్యలను పూర్తి చేయండి.

జవాబు:
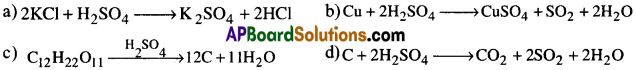
ప్రశ్న 11.
అమ్మోనియాను తడిలేకుండా చేయడానికి దేనిని ఉపయోగిస్తారు?
జవాబు:
పొడి లైమ్ CaO ను పంపుట ద్వారా NH3 ను తడిలేకుండా (పొడిగా) చేస్తారు.
![]()
ప్రశ్న 12.
అమ్మోనియాను తడి లేకుండా మార్చుటకు గాఢ H2SO4, P4O10 మరియు అనార్ద్ర CaCl2 లను ఉపయోగించరు ఎందుకు?
జవాబు:
అమ్మోనియా వీటితో చర్య నొంది (NH4) SO4; (NH4)3PO4 మరియు CaCl2.8NH3లను ఏర్పరుస్తుంది. కావున అమ్మోనియాను తడి లేకుండా చేయడానికి వీటిని ఉపయోగించరు.
Long Answer Questions (దీర్ఘ సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
స్పర్శ (కాంటాక్ట్) విధానంలో సల్ఫ్యూరిక్ ఆమ్లం తయారు చేయుటను వివరింపుము. [TS -18]
జవాబు:
స్పర్శ (కాంటాక్ట్) విధానంలో సల్ఫ్యూరిక్ ఆమ్లం తయారీ మూడు దశలలో జరుగును:
1) SO2ఉత్పత్తి :
చూర్ణ స్థితిలో ఉన్న సల్ఫర్ను గాలి సమక్షంలో మండించుట ద్వారా దీనిని తయారు చేస్తారు.
S+ O2 → SO2
4FeS2 + 11O2 → 2Fe2O3 + 8SO2.
2) SO3 ఏర్పడుట:
- సల్ఫర్ డై ఆక్సైడ్, V2O5 ఉత్ప్రేరకం సమక్షంలో ఆక్సీకరణం చెంది సల్ఫర్ ట్రై ఆక్సైడ్ ఏర్పడును.
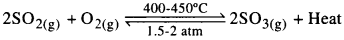
- ఇది ఒక ద్విగత చర్య. పురోగామి చర్య ఉష్ణమోచక చర్య. ఘనపరిమాణం తగ్గు దిశలో చర్య జరుగుతుంది.
- లీషాల్లీయర్ నియమం ప్రకారం అధిక మొత్తంలో SO3 దిగుబడికి అల్ప ఉష్ణోగ్రత మరియు అధిక పీడనాలు అవసరము. కాని తక్కువ ఉష్ణోగ్రత వద్ద చర్య చాలా నెమ్మదిగా జరుగును.
iv) అనువైన పరిస్థితులు :
(a) ఉష్ణోగ్రత; 720K (b) పీడనం : 1.5 నుండి 2 atm
v) ఉత్ప్రేరకం :
V2O5(లేదా) Pt
3) SO3 ని H2SO4గా మార్చుట:
SO3 ని గాఢ H2SO4 లోకి అధిశోషణంగావిస్తే ఓలియమ్ (లేదా) ఫైరో సల్ఫ్యూరిక్ ఆమ్లం లభిస్తుంది.
SO3 + H2SO4(గాఢ) → H2S2O7 (ఓలియమ్)
ఓలియమ్ను లెక్కించిన పరిమాణంలో సజలం చేసి కావలసిన గాఢతలలో H2SO4 ను పొందుతారు.
H2S2O7 + H2O → 2H2SO4
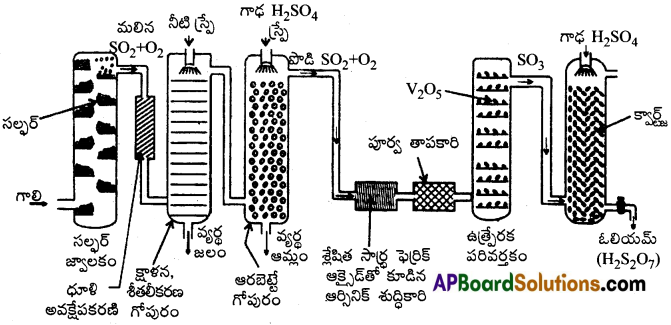
![]()
ప్రశ్న 2.
ఆక్సిజన్ నుండి ఓజోన్ను ఎలా తయారు చేస్తారు. ఈ క్రింది వాటితో దాని చర్యలను వివరింపుము
(a) C2H4 (b) KI (c) Hg (d) PbS [AP 22][IPE ’14][AP,TS 16,17,18,19,20]
జవాబు:
I) ఓజోన్ తయారీ :
నిశ్శబ్ద విద్యుదుత్సర్గం ద్వారా అనార్ధ్ర ఆక్సిజన్ ను ప్రవాహంలా పంపినట్లైతే ఆక్సిజన్ ఓజోన్గా (10%) మార్పు చెందుతుంది. ఏర్పడిన ఉత్పన్నాన్ని ఓజోనైజ్డ్ ఆక్సిజన్ అంటారు.
3O2 → 2O3; ∆H = +142 kJ mol-1.
ఈ విధానాన్ని ఓజోనైజర్లో చేస్తారు.
II) ఓజోన్ చర్యలు:
a) ఓజోన్ ఇథిలీన్తో చర్య జరిపి ఇథిలీన్ ఓజొనైడ్ను ఏర్పరుస్తుంది.
దీనిని Zn సమక్షంలో జలవిశ్లేషణ గావించిన ఫార్మాల్డిహైడ్ను ఏర్పరుస్తుంది.
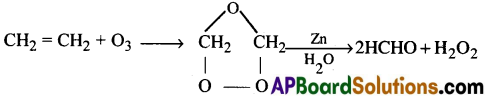
b) ఓజోన్ పొటాషియం అయోడైడ్ను అయోడిన్గా ఆక్సీకరిస్తుంది.
2KI + H2O + O3 → 2KOH + I2 + O2
c) ఓజోన్ మెర్కురీని మెర్క్యురస్ ఆక్సైడ్గా ఆక్సీకరిస్తుంది. (ఈ చర్యను ‘టెయిలింగ్ ఆఫ్ మెర్క్యురీ’ అని కూడా అంటారు)
2Hg + O3 → Hg2O + O2
d) ఓజోన్ నల్లని లెడ్సల్ఫైడ్ను తెల్లని లెడ్సల్ఫేట్గా ఆక్సీకరిస్తుంది.
PbS + 4O3 → PbSO4 + 4O2