Students get through AP Inter 2nd Year Chemistry Important Questions 5th Lesson లోహనిష్కర్షణలో సాధారణ సూత్రాలు which are most likely to be asked in the exam.
AP Inter 2nd Year Chemistry Important Questions 5th Lesson లోహనిష్కర్షణలో సాధారణ సూత్రాలు
Very Short Answer Questions (అతిస్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
ప్లవన ప్రక్రియలో నిమ్నకారుల పాత్ర ఏమిటి?
జవాబు:
ప్లవన ప్రక్రియలో నిమ్నకారులను వాడుట వలన గాలి బుడగలలో కొన్ని రకాల కణాలు నురుగును ఏర్పర్చకుండా నివారించవచ్చు.
ఉదా: జింక్ సల్ఫైడ్ ముడి ఖనిజాన్ని (ZnS)నుండి లెడ్సల్ఫైడ్ను వేరుపరుచటకు NaCN ను నిమ్నకారిగా వాడతారు. NaCN, ZnS ఉపరితలంపై జింక్ సంక్లిష్టం Na2[Zn(CN)4] ను ఏర్పర్చి నురగను ఏర్పరచకుండా నిరోధిస్తుంది. PbS మాత్రమే నురగను ఏర్పరుస్తుంది. కావున ZnS ముడి ఖనిజాన్ని వేరుపరుస్తారు.
ప్రశ్న 2.
C మరియు CO లలో ఏది 673 K వద్ద మంచి క్షయకరణి?
జవాబు:
ఎల్లింగ్ హోమ్ పటంను గమనించగా 983K వద్ద CO నుండి CO2 ఏర్పడే ప్రమాణస్వేచ్ఛశక్తి మరియు C నుండి CO2 ఏర్పడే వక్రము ∆G° వద్ద ఖండించు కొంటాయి.
అనగా ఈ ఉష్ణోగ్రత వద్ద లేదా దీని కంటే తక్కువ ఉష్ణోగ్రత వద్ద C కంటే మంచిCO క్షయకరణి. ఏది ఏమైన దీని కంటే ఎక్కువ ఉష్ణోగ్రత వద్ద వ్యతిరేక ప్రక్రియ జరుగును.
ప్రశ్న 3.
కాపర్ విద్యుత్ శోధన ప్రక్రియలో ఏర్పడే ఆనోడ్ బురదలో ఉన్న సాధారణమూలకాల పేర్లను వ్రాయుము.
జవాబు:
కాపర్ ధాతువు విద్యుత్ శోధన ప్రక్రియలో ఆనోడ్ బురదలో సాధారణ మూలకాలు ఆంటిమోని, సెలీనియమ్, టెలూరియమ్, వెండి, బంగారం మరియు ప్లాటినమ్ లోహాలు ఉంటాయి.
ఈ మూలకాలను చర్యాశీలత తక్కువ కనుక CuSO4 + H2SO4 ద్రావణం ప్రభావానికి గురి కావు. కావున ఆనోడ్ వద్ద ఆనోడ్ బురదలో అడుగుకు చేరుతాయి.
ప్రశ్న 4.
కాపర్ లోహ నిష్కర్షణంలో సిలికా పాత్రను తెలపండి. [IPE ’14]
జవాబు:
కాపర్ లోహనిష్కర్షణంలోఐరన్ఆక్సైడ్ (FeO)ను లోహ మలం(FeSiO3) గా మార్చి తొలగించుటలో సిలికా ఆమ్ల ద్రవకారిగా పనిచేస్తుంది.
![]()
ప్రశ్న 5.
‘పోలింగ్’ ను విశదీకరించండి. [AP 15,16]
జవాబు:
లోహం, లోహ ఆక్సైడ్ను మలినంగా కలిగి ఉన్నప్పుడు ‘పోలింగ్’ శోధన పద్ధతిని వాడతారు. ఈ పద్ధతిలో గలన స్థితిలో ఉండే లోహాన్ని పచ్చి కర్రలలో కలియ బెడతారు.మాలిన్యాలు వాయువుగా వేరు పడుతాయి లేదా ఆక్సీకరణం చెంది గలన లోహ ఉపరితలం మీద తెట్టుగా (లోహమలం)గా ఏర్పడతాయి. బ్లిస్టర్ కాపర్ను ఈ పద్ధతిలో శుద్ధిచేస్తారు. కర్రల నుండి వెలువడిన క్షయకరణ వాయువులు కాపర్ ఆక్సీకరణను అడ్డుకుంటాయి.
![]()
ప్రశ్న 6.
నికెల్ శోధనానికి ఒక పద్ధతిని వివరించండి.
జవాబు:
మలిన నికెల్ను CO ప్రవాహంసమక్షంలో 330-350K వద్ద వేడి చేసిన ఇది మలినాలను వదిలేసి బాష్పశీల నికెల్టెట్రాకార్బోనైల్ అనే సంక్లిష్ట సమ్మేళనాన్ని ఏర్పరుస్తుంది.
![]()
పైన వచ్చిన బాష్పశీల నికెల్ టెట్రా కార్బోనైల్ను అధిక ఉష్ణోగ్రత (450–470K)వద్ద వేడి చేసిన అది ఉష్ట్రీయ విఘటనం చెంది శుద్ధ నికెల్ లోహాన్ని ఇస్తుంది
![]()
ప్రశ్న 7.
పోత ఇనుము దుక్క ఇనుము నుండి ఏ విధంగా విభేదిస్తుంది?
జవాబు:
బ్లాస్ట్ కొలిమి నుండి వచ్చిన ఐరన్ దుక్క ఇనుము అంటారు. ఇది దాదాపు 4% కార్బన్ మరియు తక్కువ మొత్తంలో మిగిలిన మలినాలను (ఉదా: S, P, Si, Mn). లను కలిగి ఉంటుంది.
దుక్క ఇనుమును బొగ్గుతో వేడి గాలిని ఉపయోగించి ద్రవీభవనం చేస్తే పోత ఇనుము తయారవుతుంది. ఇది కొంచెం తక్కువ కార్బన్ (దాదాపు 3%) ను కలిగి ఉంటుంది. ఇది చాలా గట్టిగా, పెళుసుగా ఉంటుంది. కావున పోత ఇనుము, దుక్క ఇనుము రెండూ వేరువేరు.
ప్రశ్న 8.
ఖనిజం మరియు ముడిఖనిజాల మధ్య భేదాలు ఏమిటి?
జవాబు:
లోహాలు మలినాలతో భూ పటలంలో సహజంగా రసాయన సంయోగ పదార్థాలుగా లభిస్తాయి. ఇవి గనుల తవ్వకం ద్వారా లభిస్తాయి. వీటిని ఖనిజం అంటారు.
ఖనిజాలలో కొన్నింటిని మాత్రమే రసాయనికంగా, వాణిజ్యపరంగా లోహనిష్కర్షణకు ఉపయోగిస్తారు. అటువంటి ఖనిజాలనుదాతువులు లేదా ముడిఖనిజాలు అంటారు. అన్ని ముడి ఖనిజాలు ఖనిజాలే కాని అన్ని ఖనిజాలు ముడి ఖనిజాలు కాదు.
ఉదా: అల్యూమినియం భూపటలంలో రెండు ఖనిజాల రూపంలో లభిస్తుంది అవి బాక్సైట్ (Al2O3. xH2O) మరియు బంక మట్టి (Al2O3.2SiO2. 2H2O). అల్యూమినియంను రసాయనికంగా, ఆర్థికంగా వాణిజ్యపరంగా బాక్సైట్ నుండి నిష్కర్షణ చేస్తారు. కావున బాక్సైట్ను ముడిఖనిజం (ధాతువు) అంటారు.
ప్రశ్న 9.
సిలికాపూత ఉన్న కన్వర్టర్ లో కాపర్ మాటీని ఎందుకు ఉంచుతారు.
జవాబు:
కాపర్మటీ Cu2S మరియు FeS లను కలిగి ఉంటుంది.సిలికాపూత పూసిన కన్వర్టర్ లోనికి గలన కాపర్ మాటీని తీసుకొని దీని గుండా వేడి గాలిని పంపిస్తారు. మాటీలో ఉన్న Fes. FeOగా ఆక్సీకరణం చెందుతుంది ఇది సిలికా(SiO2)తో కలిసి FeSiO3 లోహ మలంను ఏర్పరుస్తుంది.
2FeS + 3O2 → 2FeO + 2SO2
FeO + SiO2 → FeSiO3
ఇది లోహ మలం రూపంలో మొత్తం ఇనుమును తొలగిస్తుంది. కొంత Cu2S ఆక్సీకరణం చెంది Cu2O ను ఏర్పరుస్తుంది. ఇది ఎక్కువ Cu2S తో చర్య జరిపి కాపర్ లోహాన్ని ఏర్పర్చును.
2Cu2S + 3O2 → 2Cu2O + 2SO2
2Cu2O + Cu2S → 6Cu + SO2
సిలికా పూత ఉన్న కన్వర్టర్ లో కాపర్ మాటీని వేడి చేసినపుడు మాటీలో ఉన్న FeS ను FeSiO3 మలిన లోహ మలం తొలగించవచ్చును.
ప్రశ్న 10.
అల్యూమినియమ్ లోహ నిష్కర్షణలో క్రయోలైట్ పాత్ర ఏమిటి? [AP,TS 15,16,18,20]
జవాబు:
క్రయోలైట్ పాత్ర కింది విధంగా ఉంటుంది.
- క్రయోలైట్ అల్యూమినాను మంచి వాహకంగా చేస్తుంది.
- మిశ్రమం యొక్క ద్రవీభవన స్థానంను 2323K నుండి 1140 K కు తగ్గిస్తుంది.
![]()
ప్రశ్న 11.
తక్కువ శ్రేణి కాపర్ ముడి ఖనిజాల విషయంలో ఏ విధంగా నిక్షాళనం చేస్తారు?
జవాబు:
తక్కువ శ్రేణి కాపర్ ముడి ఖనిజాల నుండి జలలోహ సంగ్రహణం ద్వారా కాపర్ను నిష్కర్షణం చేస్తారు. కాపర్ Cu+2 అయాన్ల రూపంలో ద్రావణంలోనికి పోతుంది.
2Cu(s) + 2H2SO4(aq) + O2(g) → 2CuSO4(aq) + 2H2O(l)
(or) Cu(s) + 2H+(aq) + ½O2(g) → Cu+2(aq) + H2O(l)
ప్రశ్న 12.
CO ను ఉపయోగించి జింక్ ఆక్సైడ్ను క్షయకరణం చేయడం ద్వారా జింకు ఎందువల్ల నిష్కర్షణం చేయరు.
జవాబు:
CO → CO2 ఏర్పడే చర్య యొక్క ప్రమాణ స్వేచ్ఛ శక్తి ZnO → Zn ఏర్పడే చర్య యొక్క స్వేచ్ఛ శక్తి కన్నా అధికం కనుక ZnO ను Zn గా క్షయకరించుటకు CO ను ఉపయోగించలేము.
ప్రశ్న 13.
కింది లోహాల సంఘటనాన్ని ఇవ్వండి. [IPE ’14]
a) ఇత్తడి b) కంచు c) జర్మన్ సిల్వర్ [TS 16,19] [AP 19]
జవాబు:
a) 60–80% Cu; 20-40% Zn – ఇత్తడి
b) 75-90% Cu; 10-25% Sn – కంచు
c) 50–60% Cu; 10–30% Ni, 20-30% Zn – జర్మన్ సిల్వర్
ప్రశ్న 14.
గాంగ్, లోహ మలం పదాలను వివరించండి.
జవాబు:
ధాతువుతో ఉన్న మట్టి మరియు ఇసుక రాళ్ళను గాంగ్ అంటారు. భర్జనం లేదా భస్మీకరణంగావించిన ధాతువుతో కలిసి ఉండి సులువుగా ద్రావకారితో ద్రవంగా మారే పదార్థంను లోహ మలం అంటారు.
ఉదా: ఐరన్ లోహ నిష్కర్షణలో సిలికా మలినాలను తొలగించుటకు CaO ను ద్రవకారిగా ఉపయోగించి, సులువుగా ద్రవంగా మారే కాల్షియం సిలికేట్ (CaSiO3)అనే లోహ మలంగా తొలగిస్తారు.
CaCO3 → CaO + CO2.
CaO + SiO2 → CaSiO3(slag)
ప్రశ్న 15.
వెండి, బంగారం వాటి ముడి ఖనిజాల నిక్షాళనం ద్వారా ఎలా లభ్యం అవుతాయి?
జవాబు:
వెండి మరియు బంగారం నిష్కర్షణలో, ఆ లోహాలను గాలి (O2 కోసం) సమక్షంలో NaCN లేదా KCN విలీన ద్రావణాలతో నిక్షాళనం చెందిస్తారు. నిక్షాళన ద్రావణం నుంచి జింక్ ద్వారా లోహాన్ని స్థానభ్రంశం చెందిస్తే అప్పుడు వెండి మరియు బంగారం లోహాలు లభ్యమవుతాయి.
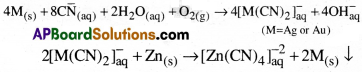
ప్రశ్న 16.
ఎల్లింగ్హామ్ పటాల అవధులు ఏమిటి?
జవాబు:
ఎల్లింగ్హామ్ పటాల అవధులు:
- ఎల్లింగ్హామ్ పటం ఏదైనా చర్య జరుగుతుందో లేదో సూచిస్తుంది. క్షయకరణ ప్రక్రియ గతిజశాస్త్రం గురించి ఏమి తెలియజేయదు. ఇచ్చిన ఉష్ట్రీయ పరిస్థితుల వద్ద చర్య ఎంత వేగంగా జరుగుతుందో తెలియచేయలేదు.
- ∆G° విలువ K మీద ఆధారపడి ఉంది. (∆G° = -RT/K). అంటే క్రియాజనకాలు, క్రియాజన్యాలు సమతాస్థితిలో ఉన్నట్లు భావిస్తే ఇది ఎల్లప్పుడు సరికాదు. ఎందుకంటే క్రియాజనకం, కియాజన్యం ఘన పదార్థంగా ఉండవచ్చు.
![]()
ప్రశ్న 17.
కింది లోహాలకు చెందిన ఏవైన రెండు ముడి ఖనిజాల ఫార్ములాలను a) అల్యూమినియం b) జింక్ c) ఐరన్ d) కాపర్ రాయండి. [AP 20] [IPE ’14][TS-15 19,20]
జవాబు:
a) అల్యూమినియం బాక్సైట్ ……………. Al2O3.2H2O
క్రయోలైట్ ………….. Al2O3.2SiO2.2H2O (or) [Al2(OH)4Si2O5]
b) జింక్ జింక్ బ్లెండ్ ………… ZnS
(లేదా) స్ఫాలరైట్
కాలమైన్ ………….. ZnCO3
c) ఐరన్ హెమటైట్ ………….. Fe2O3
కాసిటరైట్ ………….. FeCO3
d) కాపర్ కాపర్ పైరైటిస్ ………….. CuFeS2
(లేదా) చాల్కో పైరైటిస్
మాలాకైట్ ………….. CuCO3.Cu(OH)2.
ప్రశ్న 18.
మాటీ అంటే ఏమిటి? దాని సంఘటనాన్ని ఇవ్వండి. [AP 15,17]
జవాబు:
ఇది కాపర్ సల్ఫైడ్ మరియు ఐరన్ సల్ఫైడ్ల మిశ్రమం (Cu2S + FeS)
కాపర్ నిష్కర్షణలో భర్జనం చేయబడిన ముడి ఖనిజాన్ని బొగ్గు మరియు ఇసుకతో కలిపి బ్లాస్ట్ కొలిమిలో వేడి చేస్తారు. అప్పుడు కొలిమి అడుగు భాగాన గలన ద్రవ్యం వస్తుంది. దీనినే మాటీ అంటారు.
ప్రశ్న 19.
బ్లిస్టర్ కాపర్ అంటే ఏమిటి? ఎందుకు దానిని అలా పిలుస్తారు? [TS-18]
జవాబు:
97-98 % కాపర్ను బ్లిస్టర్ (బొబ్బర్లు) కాపర్ అంటారు. గలన లోహాన్ని చల్లబర్చినప్పుడు దీనిలో ఉన్న SO2 వాయువులు వెళ్ళిపోతాయి. అందువల్ల కాపర్ లోహతలం పై బుడగలు ఏర్పడుతాయి. ఈ బుడగలు బ్లిస్టర్ (బొబ్బర్లు) రూపంలో ఉంటాయి. కావున దీనిని బ్లిస్టర్ కాపర్ అని పిలుస్తారు.
ప్రశ్న 20.
ముడిఖనిజం నుంచి మలినాల అయస్కాంత వేర్పాటును వివరించండి.
జవాబు:
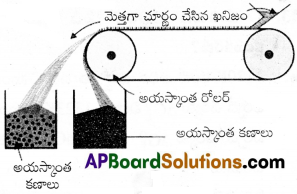
1) ముడి ఖనిజంలోని మలినం గాని లేదా ముడి ఖనిజం గాని అయస్కాంత పదార్థం అయి ఉండవలెను
2) ఈ పద్ధతిలో ముడి ఖనిజాన్ని చూర్ణం చేసి రెండు బలమైన అయస్కాంత రోలర్ మీద తిరిగే బెల్ట్ పై మీద పడేలా పోస్తారు. అయస్కాంత మరియు అనయస్కాంత పదార్థాలు రెండు వేరు వేరు (కుప్పగా) పోగులు గా పడతాయి.
3) అయస్కాంత పదార్థం, అయస్కాంత రోలర్కు సమీపంలో కుప్పగా (పోగుగా) పడుతుంది.
ఉదా:
i) హెమటైట్ ఖనిజా కణాల అయస్కాంత పదార్థాలు, మరియు మలిన పదార్థాలు అనయస్కాంత పదార్థాలు.
ii) కాసిటరైట్ లేదా టిన్ స్టోన్లో లో ముడిఖనిజం అనయస్కాంత పదార్థం మలిన ఉల్రామైట్ అయస్కాంత పదార్థం.
ప్రశ్న 21.
ద్రావకారి అంటే ఏమిటి? [AP 18]
జవాబు:
భర్జనం లేదా భస్మీకరణంగావించిన దాతువు ఇంకా మలినాలను కలిగియున్నచో ఈ మలినాలను సులువుగా ద్రవీకరించి, లోహమలంగా తొలగించే పదార్థాలను ద్రవకారి అంటారు.
ఉదా: సిలికా, లైమ్.
ప్రశ్న 22.
కింది లోహాలలో ప్రతి లోహానికి రెండు ఉపయోగాలను వ్రాయండి.
a) జింక్ b) కాపర్ c) ఐరన్ d) అల్యూమినియం
జవాబు:
a) ఐరన్ను గాల్వనైజ్ చేయడానికి జింక్ను వాడుతారు. దీనిని బ్యాటరీలలో అధిక మొత్తంలో వాడతారు. ఇత్తడి మరియు జర్మన్ సిల్వర్ వంటి మిశ్రమ లోహాలలో ఒక అనుఘటకంగా వాడతారు.
b) కాపర న్నువిద్యుత్ పరిశ్రమలో వాడే తీగలను తయారు చేయడానికి ఉపయోగిస్తారు. దీనిని అనేక మిశ్రమ లోహాలు వాడతారు.
c) పోత ఇనుము చాలా ముఖ్యమైన ఇనుము. దీనిని స్టవ్లు, రైలు బోగీలు, గట్టర్ పైపులులలో వాడుతారు. దీనిని కేబుల్లు, ఆటోమొబైల్, గోలుసులు మరియు వ్యవసాయ పరికరాల తయారీలో వాడతారు.
d) అల్యూమినియంను ఫోటో ఫ్రేమ్ తయారికీ వాడతారు. పలుచని అల్యూమినియం రేకును చాక్లెట్ల మీద చుట్టడానికి వాడతారు.
ప్రశ్న 23.
C మరియు COలలో ఏది ZnOకు మంచి క్షయకరణి?
జవాబు:
1120K కంటే అధిక ఉష్ణోగ్రత వద్ద C నుండి CO ఏర్పడే చర్యకు ∆G°f విలువ, 1323K C నుండి CO2 ఏర్పడే చర్యకు ∆G°f విలువZnO కన్నా తక్కువగా ఉండును.
ఏది ఏమైనప్పటికి CO నుండి CO2 ఏర్పడే చర్యకు ∆G°f విలువ ZnO కన్నా అధికంగా ఉండును. కనుక C మరియు CO లలో C మంచి క్షయకరణి.
![]()
ప్రశ్న 24.
a) పోత ఇనుము
b) చేత. ఇనుము
c) నికెల్ స్టీల్
d) స్టెయిన్లెస్ స్టీల్లు
జవాబు:
a) పోత ఇనుము ఉపయోగాలు :
దీనిని స్టవ్లు, రైలు బోగీలు, గట్టర్ పైపులలో వాడతారు. దీనిని చేత ఇనుము మరియు స్టీల్ల తయారీలో వాడతారు.
b) చేత ఇనుము ఉపయోగాలు :
దీనిని వైర్ల తయారీలో వాడతారు. గొలుసులు మరియు వ్యవసాయ పరికరాల తయారీలో వాడతారు.
c) నికెల్ స్టీల్ ఉపయోగాలు :
దీనిని విమాన భాగాలు మరియు ఆటోమొబైల్ భాగాల తయారీలో వాడతారు. దీనిని కొలత టేపులు, లోలకం తయారీలో వాడతారు.
d) స్టెయిన్లెస్ స్టీల్ ఉపయోగాలు :
దీనిని సైకిళ్ళు, ఆటోమొబైల్ల తయారీలో వాడతారు.
ప్రశ్న 25.
క్రోమియం మాంగనీస్ ను వాటా ఆక్సైడ్ నుంచి నిష్కర్షణం చేయడంలో అల్యూమినియం ఎలా ఉపయోగపడుతుంది.
జవాబు:
అల్యూమినియంకు క్రోమియం మరియు మాంగనీస్ కంటే తక్కువ S.R.P విలువ ఉంటుంది. కావున అల్యూమినియం క్రోమియం మరియు మాంగనీస్ ఆక్సైడ్లను వాటి లోహాలుగా క్షయకరిస్తుంది.
Cr2O3 + 2Al → 2Cr + Al2O3
3Mn3O4 + 8Al → 4Al2O3 + 9Mn
Short Answer Questions (స్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
సార్థ లోహ సంగ్రహణ క్రియ ద్వారా కాపర్ను నిష్కర్షణ చేస్తారు. కానీ జింక్ను కాదు వివరించండి.
జవాబు:
జింక్ యొక్క E° (Zn+2 / Zn = -0.76V) విలువ కాపర్ E° (Cu+2/Cu = + 0.34V) విలువ కన్నా తక్కువ. దీని జింక్ బలమైన క్షయకరణ కారకం మరియు ఇది కాపర్ ద్రావణంలోని Cu+2 అయాన్లను స్థానభ్రంశం చెందించును.
Zn(s) + Cu+2(aq) → Zn+2(aq) + Cu
ఈ క్రమంలో జలలోహ సంగ్రహణ ద్వారా జింక్ . నిష్కర్షణకు కింది బలమైన క్షయకరణలను
ఉపయోగించాలి.
K(E° K+/K = -2.93V) Mg(E°Mg+2/Mg = -2.37V)
Al(E°Al+3/Al = -1.66V) etc.,
అయితే ఈ లోహములు అన్నియు నీటిని H2 వాయువుగా క్షయకరించును. కనుక ఈ లోహములను Zn+2 అయాన్లను కలిగిన ద్రావణం నుండి జింకను స్థాన భ్రంశం చెందించుటకు ఉపయోగించలేము. కనుక కాపర్ను జలలోహ సంగ్రహణలో నిష్కర్షించగలము కాని జింక్ను నిష్కర్షించలేము.
ప్రశ్న 2.
కాపర్ నిష్కర్షణ దాని ఆక్సైడ్ ముడి ఖనిజాన్ని క్షయకరణం చేయడం ద్వారా కంటే పైరైటీస్ నుంచి ఎందుకు ఎక్కువ కష్టం?
జవాబు:
CS2 మరియు H2S ల కంటే Cu2S యొక్క ∆G°f అత్యధిక ఋణాత్మకం. కార్బన్ లేదా హైడ్రోజన్లలో ఏదో ఒకటి Cu2S ను Cuగా క్షయకరణం చేయలేదు.
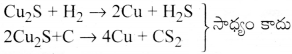
CO కంటే CuzO యొక్క ∆G°f విలువ తక్కువ ఋణాత్మకం. కావున కార్బన్ తేలికగా Cu2O ను Cu.గా క్షయకరిస్తుంది.
Cu2O + C → 2Cu + CO
ఈ కారణంగా కాపర్ నిష్కర్షణ దాని ఆక్సైడ్ ముడి ఖనిజాన్ని క్షయకరణం చేయడం కంటే పైరైటీస్ నుండి క్షయకరణం చేయడం చాల కష్టం.
![]()
ప్రశ్న 3.
మండల శోధనను వివరించండి?
జవాబు:
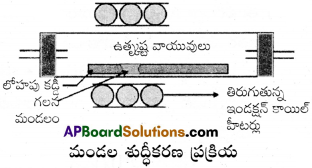
మండల శోధనం :
మలినాలు ఘనస్థితిలో ఉన్న లోహంలో కంటే గలన స్థితిలో ఉండే లోహంలో ఎక్కువ కరిగి ఉంటాయనే నియమం మీద ఈ పద్దతి ఆధారపడి ఉంది. అపరిశుద్ధ లోహపు కడ్డీకి ఒక చివర తిరిగే వృత్తాకార తాపకం బిగించబడి ఉంటుంది. ముందుకు తిరిగే తాపకంతో పాటు గలన మండలం తిరుగుతుంది.
తాపకం ముందుకు జరగుతున్న కొద్దీ, గలనం నుండి శుద్ధ లోహం స్ఫటికీకరణం చెందుతుంది. మలినాలు ప్రక్కనున్న గలన మండలంలోనికి వెళ్తాయి.
ఈ ప్రక్రియను అనేక సార్లు పునరావృతం చేస్తారు. తాపకం ఒకే దిశలో ఒక చివర నుంచి ఇంకొక చివరకు తిరుగుతూ ప్రయాణిస్తుంది. ఒక చివర మలినాలు సాంద్రీకరణం చెందుతాయి. ఈ చివరే
ప్రశ్న 4.
జింక్ బెండ్ నుంచి జింక న్ను నిష్కర్షణం చేయడంలో జరిగే రసాయన చర్యలను రాయండి.
జవాబు:
ఇమిడి ఉన్న వివిధ దశలు:
i) సాంద్రీకరణ :
ధాతువును పొడి (ముక్కలుగా) చేసి తరువాత ప్లవన ప్రక్రియ విధానంలో సాంద్రీకరణం చేస్తారు.
ii) భర్జనం :
సాంద్రీకరణం చెందించినధాతువును అధిక గాలి సమక్షంలో దాదాపు1200K వద్ద భర్జనం చేసిన జింక్ ఆక్సైడ్ (ZnO) ఏర్పడుతుంది.
![]()
iii) క్షయకరణం :
పైన లభించిన జింక్ ఆక్సైడ్ను బొగ్గు పొడితో మిశ్రమం చేసి అగ్గి మట్టితో చేసిన రిటార్ట్ 1673K ఉష్ణోగ్రతకు వేడి చేసిన ఇది జింక్ లోహంగా క్షయకరణం చెందును.
![]()
1673K వద్ద జింక్ లోహం బాష్పస్థితిలో ఉంటుంది. స్వేదనం చేసిన ఇది ద్రవంగా మారుతుంది.
iv) విద్యుత్ శోధనం :
అపరిశుద్ధ లోహాన్ని అనోడ్గాను, శుద్ధ జింక్ లోహ రేకును కాథోడ్ గాతీసుకుంటారు. వీలిన H2SO4తో ఆమ్లీకృతం చేయబడిన ZnSO4 ద్రావణంను విద్యుత్ విశ్లేష్యంగా తీసుకొని విద్యుత్ను ప్రవహింప చేసిన శుద్ధ Zn కాథోడ్ వద్దనిక్షిప్తమవుతుంది.
ప్రశ్న 5.
ఐరన్ నిష్కర్షణం జరిగేటప్పుడు, బ్లాస్ట్ కొలిమిలో వివిధ మండలాలలో జరిగే రసాయన చర్యలను రాయండి.
జవాబు:
500-800K వద్ద (తక్కువ ఉష్ణోగ్రత అవధి)
3Fe2O3 + CO → 2Fe3O4 + CO2
Fe3O4 + 4CO → 3Fe + 4CO2
Fe2O3 + CO → 2FeO + CO2
At 900-1500K (ఎక్కువ ఉష్ణోగ్రత అవధి)
C + CO → 2CO
FeO + CO → Fe + CO2
ప్రశ్న 6.
సిలికాతో కలిసి ఉన్న బాక్సైట్ ముడి ఖనిజంలో సిలికా నుంచి అల్యూమినాను ఎలా వేరు చేస్తారు? [TS-15]
జవాబు:
- అల్యూమినియం(Al2O3) యొక్క ప్రధాన ముడి ఖనిజం అయిన బాక్సైట్లో SiO2, ఐరన్ ఆక్సైడ్(Fe2O3)లు మరియు టైటానియమ్ ఆక్సైడ్(TiO2) మలినాలు ఉంటాయి. [TS-17]
- చూర్ణం చేసిన ధాతువుకు గాఢ NaOH ద్రావణం కలిపి 473-523K ఉష్ణోగ్రత మరియు 35-36 బార్ల పీడనం వద్ద చర్య జరిపిస్తారు.
- ఈ విధంగా Al2O3 సోడియం అల్యూమినేట్గా నిక్షాళనం (SiO కూడా సోడియం సిలికేట్గా) చెందుతుంది. ఇతర మలినాలు ఉండి పోతాయి.
Al2O3(s) + 2NaOH(aq) + 3H2O(l) → 2Na[Al(OH)4](aq) - అల్యూమినేట్ క్షార ప్రవృత్తి గలది. దానిలోనికి CO2 వాయువును పంపి తటస్థీకరించి, సార్థ Al2O3 గా అవక్షేపిస్తారు.
2Na[Al(OH)4](aq) + CO2(g) → Al2O3.xH2O(s) + 2NaHCO3(aq) - సోడియం సిలికేట్ ద్రావణంలో ఉండిపోతుంది. అవక్షేపిత సార్థ అల్యూమినాను వడపోత ద్వారా వేరు పరచి, తడి లేకుండా చేసి, వేడి చేస్తే శుద్ధ Al2O3 లభిస్తుంది.
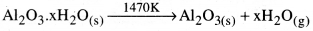
ప్రశ్న 7.
భర్జనం మరియు భస్మీకరణాలను భేదపరిచే ఉదాహరణలను ఇవ్వండి. [TS-18][IPE ’14][AP,TS-16,18]
జవాబు:
| భర్జనం | భస్మీకరణం |
| 1) లోహ ద్రవీభవన స్థానం కంటే తక్కువ ఉష్ణోగ్రత వద్ద అధిక గాలి సరఫరాతో ముడి ఖనిజాన్ని వేడిచేసే విధానాన్ని భర్జనం అంటారు. | 1) గాలిపూర్తిగా లేకుండా ముడి ఖనిజాన్ని దాని గలన ఉష్ణోగ్రత కంటే తక్కువ ఉష్ణోగ్రత వద్ద వేడి చేసే విధానాన్ని భస్మీకరణం అంటారు. |
| 2) సల్ఫైడ్ ధాతువు ఆక్సైడ్గా మారుతుంది. |
2) కార్బోనేట్ ధాతువు ఆక్సైడ్గా మారుతుంది. |
| 3) బాష్పశీల మలినాలను ఆక్సైడ్లుగా తొలగించబడతాయి. SO2, As2O3 etc., | 3) నీరు మరియు కర్బన సమ్మేళనాల మలినాలను తొలగించబడతాయి. |
![]()
ప్రశ్న 8.
Cr2O3 ఏర్పాటుకు ∆G° విలువ -540 kJ mol-1 Al2O3 ఏర్పాటుకు – 847 kJ mol-1. Al తో Cr2O3 క్షయకరణం సాధ్యమా?
జవాబు:
రెండు సమీకరణాలు:

ఆక్సీకరణ, క్షయకరణ చర్యకు ∆G°f విలువ ఋణాత్మకం కనుక అల్యూమినియం తో Cr2O3 యొక్క క్షయకరణం సాధ్యపడును.
ప్రశ్న 9.
అల్యూమినియం విద్యుత్ లోహ సంగ్రహణంలో, గ్రాఫైట్ కడ్డీ పాత్ర ఏమిటి?
జవాబు:
విద్యుత్ లోహ సంగ్రహణలో గలన అల్యూమినా, క్రయోలైట్ మరియు ఫ్లోర్స్పర్ మిశ్రమంను, గ్రాఫైట్ ఆనోడ్గా మరియు గ్రాఫైట్ పూత ఉన్న ఇనుము తొట్టెను కాథోడ్గా తీసుకొని విద్యుత్ విశ్లేషణ చేస్తారు. అల్యూమినియమ్ కాథోడ్ వద్ద CO మరియు CO2 లు ఆనోడ్ వద్ద వెలువడుతాయి.

గ్రాఫైట్కు బదులు కొన్ని ఇతర లోహాలను ఆనోడ్గా వాడినట్లయితే ఆనోడ్ వద్ద విడుదలైన O2 లోహ ఎలక్ట్రోడు ఆక్సీకరించుటయే కాక కాథోడ్ వద్ద విడుదలైన అల్యూమినియమ్ను కూడా Al2O3 గా మార్చును. కనుక విద్యుత్ లోహ సంగ్రహణలో గ్రాఫైట్ యొక్క పాత్ర ఆనోడ్ వద్ద విడుదలై O2 ను నివారించుట లేనట్లయితే విడుదలై అల్యూమినియం తిరిగి Al2O3 గా ఆక్సీకరించబడును.
ప్రశ్న 10.
కింది లోహ శోధణ పద్ధతులలో సూత్రాలను పేర్కొనండి. [TS 19] [AP 19]
a) మండల శోధనం b) విద్యుత్ శోధనం (శుద్ధి చేయడం) c) పోలింగ్ d) బాష్పప్రావస్థ శోధనం
జవాబు:
a) మండల శోధనం :
మలినాలు ఘనస్థితిలో ఉన్న లోహంలో కంటే గలన స్థితిలో ఉండే లోహంలో ఎక్కువ ఉంటాయనే నియమం మీద పద్ధతి ఆధారపడి ఉంది. అపరిశుద్ధ లోహపు కడ్డీకి ఒక చివర తిరిగే వృత్తాకార తాపకం బిగించబడి ఉంటుంది. ముందుకు తిరిగే తాపకంతో పాటు గలన మండలం తిరుగుతుంది. తాపకం ముందుకు జరుగుతున్న కొద్దీ, గలనం నుంచి శుద్ధ లోహం స్ఫటికీకరణం చెందుతుంది. మలినాలు ప్రక్కనున్న గలన మండలంలోనికి వెళ్తాయి. ఈ ప్రక్రియను అనేక సార్లు పునరావృతం చేస్తారు. తాపకం ఒకే దిశలో ఒక చివరి నుంచి ఇంకొక చివరకు తిరుగుతూ ప్రయాణిస్తుంది. ఒక చివరన మలినాలు సాంద్రీకరణం చెందుతాయి. ఈ చివరే సరిహద్దు.
b) విద్యుత్ శోధనం :
ఈ పద్ధతిలో అపరిశుద్ధ లోహాన్ని ఆనోడ్గాను,అదే లోహం యొక్క శుద్ధ లోహ రేకును కాథోడ్గాను ఉపయోగిస్తారు. కరిగే స్వభావం ఉన్న అదే లోహ లవణం కలిగి ఉన్న విద్యుత్ విశ్లేషణం గల తొట్టేలో వాటిని (ఆనోడ్, కాథోడ్లను) ముంచి ఉంచుతారు. అధిక క్షార లోహం ద్రావణంలోనే (ఉండి పోతుంది) మిగిలి ఉండును. తక్కువ క్షారలోహం ఆనోడ్ వద్దకు చేరును మరియు ఆనోడ్ వద్ద బురదగా కిందకు చేరుతాయి.
c) పోలింగ్ :
లోహంలో లోహ ఆక్సైడ్ మలినంగా ఉన్నప్పుడు పోలింగ్ విధానంను ఉపయోగిస్తారు. ఈ పద్ధతిలో గలన స్థితిలో ఉండే లోహాన్ని పచ్చి కర్రలతో కలియబెడతారు. మాలిన్యాలు వాయువులుగా వేరు పడతాయ లేదా ఆక్సీకరణం చెంది, గలన లోహ ఉపరితలం మీద తెట్టుగా (లోహ మలంగా) ఏర్పడతాయి. బ్లిస్టర్ కాఫర్ను ఈ పద్ధతిలో శుద్ధి చేస్తారు. కర్రల నుంచి వెలువడి క్షయకరణ వాయువులు కాపర్ ఆక్సీకరణను అడ్డుకుంటాయి.
d) బాష్పప్రావస్థ శోధనం :
ఈ పద్దతిలో, లోహాన్ని బాష్పశీల సమ్మేళనంగా మార్చి సంగ్రహిస్తారు. తరువాత, దానిని విఘటనం చెందించి శుద్ధ స్థితిలో లోహాన్ని రాబడతారు. కావున దీనిని రెండు అవసరాలు ఉన్నవి.
- లభ్యమయ్యే కారకంతో లోహం భాష్పశీల సమ్మేళనాన్ని ఏర్పరచాలి.
- బాష్పశీల సమ్మేళనం సులభంగా విఘటనం చెందాలి. అప్పుడే సంగ్రహణ సులభమవుతుంది.
ప్రశ్న 11.
Al, MgOను క్షయకరణం చేయడానికి పరిస్థితులను సూచించండి.
జవాబు:
Al, MgOను 1600K కంటే ఎక్కువ ఉష్ణోగ్రత వద్ద క్షయకరణం చేస్తుంది.
![]()
ప్రశ్న 12.
ప్లవన ప్రక్రియ పద్ధతిలో సల్ఫైడ్ ముడి ఖనిజ శుద్ధీకరణను వివరించండి. [AP, TS 15,17,18,19] [TS 20]
జవాబు:
ప్లవన ప్రక్రియ పద్ధతి :
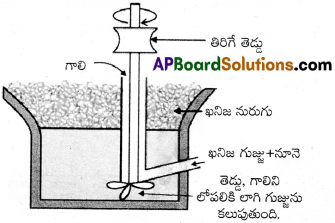
- సల్ఫైడ్ ఖనిజాల నుంచి ఖనిజ మాలిన్యాన్ని తొలగించడానికి ఈ పద్ధతిని ఉపయోగిస్తారు.
- ఈ విధానంలో చూర్ణం చేయబడ్డ ధాతువును నీటితో కలిపి అవలంబనం చేస్తారు. నూనె సమక్షంలో గాలిని పంపి, గుండ్రంగా తిరిగే తెడ్డుతో అవలంబనాన్ని గిలకరిస్తారు.
- ఖనిజ కణాలు గల నురుగు ఏర్పడుతుంది. ఈ అవలంబనానికి బుడగల సేకర్తలను, స్టీరీకరణులను కలుపుతారు.
- బుడగల సేకర్తలు (ఉదా: పైన్ ఆయిల్, కొవ్వు ఆమ్లాలు, గ్జాంథేట్లు మొదలైనవి) ఖనిజ కణాలను నీటితో తడవకుండా అడ్డుకుంటాయి.
- స్థిరీకరణలు(ఉదా: క్రిసాల్లు, ఎనిలీన్) నురుగును స్థిరికరిస్తాయి.
- ఖనిజ కణాలు నూనెతో తడిగా అవుతాయి, ఖనిజ మాలిన్య కణాలు నీటితో తడిగా అవుతాయి నురగు తేలికగా ఉండటం వల్ల, తెట్టులాగా ఏర్పడిన దానిని వేరు చేయవచ్చు.
- అప్పుడు ముడి ఖనిజకణాలు నురుగు నుంచి లభ్యమవుతాయి.
ప్రశ్న 13.
బాక్సైట్ నుంచి అల్యూమినా నిక్షాళన పద్ధతిని వివరించండి.
జవాబు:
- అల్యూమినియం(Al2O3) యొక్క ప్రధాన ముడి ఖనిజం అయిన బాక్సైట్లో SiO2, ఐరన్ ఆక్సైడ్(Fe2O3)లు మరియు టైటానియమ్ ఆక్సైడ్(TiO2) మలినాలు ఉంటాయి. [TS-17]
- చూర్ణం చేసిన ధాతువుకు గాఢ NaOH ద్రావణం కలిపి 473-523K ఉష్ణోగ్రత మరియు 35-36 బార్ల పీడనం వద్ద చర్య జరిపిస్తారు.
- ఈ విధంగా Al2O3 సోడియం అల్యూమినేట్గా నిక్షాళనం (SiO కూడా సోడియం సిలికేట్గా) చెందుతుంది. ఇతర మలినాలు ఉండి పోతాయి.
Al2O3(s) + 2NaOH(aq) + 3H2O(l) → 2Na[Al(OH)4](aq) - అల్యూమినేట్ క్షార ప్రవృత్తి గలది. దానిలోనికి CO2 వాయువును పంపి తటస్థీకరించి, సార్థ Al2O3 గా అవక్షేపిస్తారు.
2Na[Al(OH)4](aq) + CO2(g) → Al2O3.xH2O(s) + 2NaHCO3(aq) - సోడియం సిలికేట్ ద్రావణంలో ఉండిపోతుంది. అవక్షేపిత సార్థ అల్యూమినాను వడపోత ద్వారా వేరు పరచి, తడి లేకుండా చేసి, వేడి చేస్తే శుద్ధ Al2O3 లభిస్తుంది.
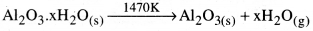
ప్రశ్న 14.
ఎల్లింగ్ హామ్ పటం అంటే ఏమిటి? ఆక్సైడ్ల క్షయకరణంలో ఈ పటాల ద్వారా ఏమి గ్రహించవచ్చు.
జవాబు:
ఆక్సైడ్ క్షయకరణంలో క్షయకరణాల ఎంపికను పరిశీలించడానికి ఇది గట్టి ఆధారాన్ని ఇస్తుంది.
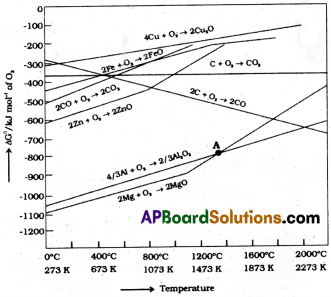
దీనిని ఎల్లింగ్హమ్పటం అంటారు. ముడి ఖనిజం ఉష్ట్రీయ క్షయకరణం ఎంత వరకు జరుగుతుందని చెప్పడానికి ఈ పటాలు ఉపయోగపడతాయి. చర్య జరగాలంటే, నిర్దిష్ట ఉష్ణోగ్రత వద్ద, చర్య గిబ్స్ శక్తి రుణాత్మకంగా ఉండాలి.
i) ఎల్లింగ్హామ్ పటం సాధారణంగా ∆G°fకు మరియు Tకు మధ్య మూలకాల నుండి ఆక్సైడ్లు ఏర్పడే వక్రాలను కలిగి ఉంటుంది.
2xM(s) + O2(g) → 2MxO(s)
ఈ చర్యలో ∆S ఋణాత్మకం దీని వలన ∆G ఉష్ణోగ్రత పెరుగుదలతో అధికవైపుకు జరుగును.
ii) ప్రాపస్థలో ఏదైనా మార్పు జరిగినప్పుడు (ఘ→ద్రా లేదా ద్రా→వా) తప్ప ప్రతి పటం ఒక సరళరేఖ, వాలులో ధనాత్మక దిశలో పెరుగుదల అటువంటి మార్పు జరిగే ఉష్ణోగ్రతను సూచిస్తుంది. (ఉదా: Zn, ZnO పటంలో సరళరేఖలో ఒక్కసారిగా జరిగే మార్పు ద్రవీభవన్నాని సూచిస్తుంది.)
iii) రేఖా పటంలో ఒక స్థానం కింద ∆G ఋణాత్మకం అవుతుంది. (అంటే MxO స్థిరంగా ఉంది) ఈ స్థానం పైన MxO దానంతట అదే విఘటనం చెందుతుంది.
iv) ఒక ఎల్లింగ్హామ్ పటంలో సాధారణ లోహాల ఆక్సీకరణానికి (వాటి సంబంధిత జాతుల క్షయ కరణానికి) కొన్ని క్షయకరణులకు ∆G° పటాలు ఇచ్చారు. వివిధ ఉష్ణోగ్రతల వద్ద ∆G°f విలువలు మొదలైన వాటిని (ఆక్సైడ్ తయారీకి) ఇచ్చారు. కాబట్టి వివరణ సులభతరమవుతుంది.
v) ఇదే విధమైన పటాలు సల్ఫైడ్లు మరియు హాలైడ్లకు కూడా నిర్మించవచ్చు మరియు MxS యొక్క క్షయకరణం ఎందుకు కష్టమైనదో స్పష్టంగా తెలియచున్నది.
ఎల్లింగ్హామ్ పటంను ఉపయోగించి క్షయకరణులు ఐచ్ఛికం.
ఎల్లింగ్హామ్ పటం నందు పైన గల ఆక్సైడ్లు వాటి క్రింద గల ఇతర లోహాలు ఆక్సైడ్లను క్షయకరిస్తాయి. దీనికి కారణం ఒకే ఉష్ణోగ్రత వద్ద గల రెండు గ్రాఫ్ల మధ్య భేదం అదే ప్రమాణంలో ∆G విలువ ఋణాత్మకంలో ఉండును.
ప్రశ్న 15.
కాపర్ పైరైటీస్ నుంచి కాపర్ను. ఎలా నిష్కర్షణ చేస్తారు?
జవాబు:
∆fG° కు మరియు T కు మధ్య గ్రాఫ్ నుందు ఆక్సైడ్ ఏర్పడే Cu2O రేఖ దాదాపు పైన ఉంది కనుక ఆక్సైడ్ ధాతువులను నేరుగా లోహంగా కోక్తో క్షయకరించవచ్చు. ( C→CO మరియు C→CO2 రేఖలు రెండు500– 600K తరువాత చాలా క్రింద స్థానంలో ఉన్నవి). ఎమైనప్పటికీ చాలా ధాతువులు సల్ఫైడ్ మరియు కొన్ని ఐరన్ ను కలిగి ఉంటాయి. సల్ఫైడ్ ధాతువులను భర్జనం లేదా ప్రగలనం చేయగా ఆక్సైడ్లను ఇస్తాయి.
2Cu2S + 3O2 → 2Cu2O + 2SO2
కోకన్ను ఉపయోగించి ఆక్సైడ్ను తేలికగా లోహకాపర్గా క్షయకరించవచ్చును.
Cu2O + C → 2Cu + CO
అసలు విధానంలో సిలికాలతో మిశ్రమం చేసిన తరువాత ధాతువుకు రివర్బరేటరి కొలిమిలో వేడి చేస్తారు. ఈ కొలిమిలో ఐరన్ ఆక్సైడ్ లోహ మలంగా మరియు కాపర్ కాపర్ మాటీగాను ఉత్పత్తి అగును. ఇది Cu2S మరియు FeS లను కలిగి ఉండును.
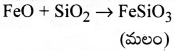
కాపర్ మాటీని సిలికా పూత ఉన్న కన్వర్టర్ లోనికి ప్రవేశపెడతారు. కొంత సిలికాను కలిపి వేడిగాలి ప్రవాహంను కన్వర్టర్లోనికి ప్రవేశపెడతారు. మిగిలిన FeS, FeO మరియు Cu2S/Cu2O లు కాపర్ మార్పుచెందును.
ఈ క్రింది చర్యలు జరుగును:
2FeS + 3O2 → 2FeO + 2SO2
FeO + SiO2 → FeSiO3
2Cu2S + 3O2 → 2Cu2O + 2SO2
2Cu2O + Cu2S → 6Cu + SO2
లభించిన కాపర్ను ఘనస్థితిలోనికి మార్చినప్పుడు SO2 విడుదలవుట వలన బ్లిస్టర్ (బొబ్బర్ల)లను కలిగి ఉండుటచే దీనిని బ్లిస్టర్ కాపర్ అంటారు.
ప్రశ్న 16.
జింక్ బ్లెండ్ నుంచి జింక్ నిష్కర్షణాన్ని క్లుప్తంగా వివరించండి.
జవాబు:
ఇమిడి ఉన్న వివిధ దశలు:
i) సాంద్రీకరణ :
ధాతువును పొడి (ముక్కలుగా) చేసి తరువాత ప్లవన ప్రక్రియ విధానంలో సాంద్రీకరణం చేస్తారు.
ii) భర్జనం :
సాంద్రీకరణం చెందించినధాతువును అధిక గాలి సమక్షంలో దాదాపు1200K వద్ద భర్జనం చేసిన జింక్ ఆక్సైడ్ (ZnO) ఏర్పడుతుంది.
![]()
iii) క్షయకరణం :
పైన లభించిన జింక్ ఆక్సైడ్ను బొగ్గు పొడితో మిశ్రమం చేసి అగ్గి మట్టితో చేసిన రిటార్ట్ 1673K ఉష్ణోగ్రతకు వేడి చేసిన ఇది జింక్ లోహంగా క్షయకరణం చెందును.
![]()
1673K వద్ద జింక్ లోహం బాష్పస్థితిలో ఉంటుంది. స్వేదనం చేసిన ఇది ద్రవంగా మారుతుంది.
iv) విద్యుత్ శోధనం :
అపరిశుద్ధ లోహాన్ని అనోడ్గాను, శుద్ధ జింక్ లోహ రేకును కాథోడ్ గాతీసుకుంటారు. వీలిన H2SO4తో ఆమ్లీకృతం చేయబడిన ZnSO4 ద్రావణంను విద్యుత్ విశ్లేష్యంగా తీసుకొని విద్యుత్ను ప్రవహింప చేసిన శుద్ధ Zn కాథోడ్ వద్దనిక్షిప్తమవుతుంది.
![]()
ప్రశ్న 17.
కాపర్ నిష్కర్షణలో ప్రగలనం పద్ధతిని వివరించండి.
జవాబు:
గలన స్థితిలో లోహాన్ని నిష్కర్షించే విధానాన్ని ప్రగలనం అంటారు.
ప్రగలన ప్రక్రియలో భర్జనం చేసిన ధాతువును సిలికా (ద్రవకారి) మరియు కొంచెం కోక్ మిశ్రమం చేసి బ్లాస్ట్ కొలిమిలో వేడి చేస్తారు. మలనంగా ఉన్న ఐరన్ ఆక్సైడ్ లోహ మలం అయిన (FeSiO3) గా మార్పు చెందును.
![]()
ఉత్పత్తి అయిన కాపర్ ద్రవ కాపర్ మాటీ రూపంలో ఉండును. ఇది ముఖ్యంగా Cu2S మరియు మార్పు చెందని FeS లను కలిగి ఉండును.
ప్రశ్న 18.
విద్యుత్ లోహ సంగ్రహణాన్ని సోదాహరణంగా వివరించండి.
జవాబు:
గలన లోహ లవణాలను విద్యుత్ విశ్లేషణ చేసి లోహాన్ని సంగ్రహించే విధానాన్ని విద్యుత్ లోహ సంగ్రహణం అంటారు.
అల్యూమినా నుండి అల్యూమినియమ్ లోహ నిష్కర్షణ :
అల్యూమినా (Al2O3) దుర్బల విద్యుత్ వాహకం కనుక దీనికి క్రయోలైట్ (Na3AlF6) మరియు ఫ్లోర్స్పర్ CaF2 లను కలుపుతారు. వీటిని కలుపుట వలన అల్యూమినా యొక్క వాహకత పెరుగటయే కాక ఆ మిశ్రమం యొక్క ద్రవీభవన స్థానం దాదాపు 1140K తగ్గుతుంది.
శుద్ధ అల్యూమినా మరియు క్రయోలైట్ మిశ్రమం నుండి అల్యూమినియమ్ లోహంను విద్యుత్ విశ్లేషణ ప్రక్రియ సంగ్రహించే విధానాన్ని హాల్ -హారోల్ట్ విధానం అంటారు.

విద్యుత్ విశ్లేషణ ప్రక్రియను కార్బన్ పూత పూసిన విద్యుత్ ఘట్టం లేదా తొట్టెలో జరుపుతారు. ఇది కాథోడ్ వలె పని చేయును.
గలన విద్యుత్ విశ్లేష్యంలో ఉంచబడిన కార్బన్ కడ్డీలు ఆనోడ్ వలె పని చేయును. గలన విద్యుత్ విశ్లేష్యంను కార్బన్ పొడితో కప్పుతారు ఇది లోహం యొక్క ఆక్సీకరణంను మరియు వికిరణం వలన వేడిని కోల్పోకుండా నివారించును. తొట్టె యొక్క ఉష్ణోగ్రత దాదాపు 1173 వద్ద ఉంచుతారు. విద్యుత్ విశ్లేషణ ప్రక్రియలో క్రింది చర్యలు జరుగును.

ప్రతి కిలో అల్యూమినియమ్ ఉత్పత్తికి ఆనోడ్ నుండి 0.5కిలో కార్బన్ మండుతుంది. దీని కారణంగా ఆనోడ్లను ఎప్పటికప్పుడు మార్చుతూ ఉండవలెను.
ప్రశ్న 19.
బాక్సైట్ నుంచి అల్యూమినియమ్ నిష్కర్షణను క్లుప్తంగా వివరించండి.
జవాబు:
- అల్యూమినియం(Al2O3) యొక్క ప్రధాన ముడి ఖనిజం అయిన బాక్సైట్లో SiO2, ఐరన్ ఆక్సైడ్(Fe2O3)లు మరియు టైటానియమ్ ఆక్సైడ్(TiO2) మలినాలు ఉంటాయి. [TS-17]
- చూర్ణం చేసిన ధాతువుకు గాఢ NaOH ద్రావణం కలిపి 473-523K ఉష్ణోగ్రత మరియు 35-36 బార్ల పీడనం వద్ద చర్య జరిపిస్తారు.
- ఈ విధంగా Al2O3 సోడియం అల్యూమినేట్గా నిక్షాళనం (SiO కూడా సోడియం సిలికేట్గా) చెందుతుంది. ఇతర మలినాలు ఉండి పోతాయి.
Al2O3(s) + 2NaOH(aq) + 3H2O(l) → 2Na[Al(OH)4](aq) - అల్యూమినేట్ క్షార ప్రవృత్తి గలది. దానిలోనికి CO2 వాయువును పంపి తటస్థీకరించి, సార్థ Al2O3 గా అవక్షేపిస్తారు.
2Na[Al(OH)4](aq) + CO2(g) → Al2O3.xH2O(s) + 2NaHCO3(aq) - సోడియం సిలికేట్ ద్రావణంలో ఉండిపోతుంది. అవక్షేపిత సార్థ అల్యూమినాను వడపోత ద్వారా వేరు పరచి, తడి లేకుండా చేసి, వేడి చేస్తే శుద్ధ Al2O3 లభిస్తుంది.
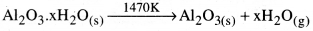
అల్యూమినా నుండి అల్యూమినియమ్ లోహ నిష్కర్షణ :
అల్యూమినా (Al2O3) దుర్బల విద్యుత్ వాహకం కనుక దీనికి క్రయోలైట్ (Na3AlF6) మరియు ఫ్లోర్స్పర్ CaF2 లను కలుపుతారు. వీటిని కలుపుట వలన అల్యూమినా యొక్క వాహకత పెరుగటయే కాక ఆ మిశ్రమం యొక్క ద్రవీభవన స్థానం దాదాపు 1140K తగ్గుతుంది.
శుద్ధ అల్యూమినా మరియు క్రయోలైట్ మిశ్రమం నుండి అల్యూమినియమ్ లోహంను విద్యుత్ విశ్లేషణ ప్రక్రియ సంగ్రహించే విధానాన్ని హాల్ -హారోల్ట్ విధానం అంటారు.

విద్యుత్ విశ్లేషణ ప్రక్రియను కార్బన్ పూత పూసిన విద్యుత్ ఘట్టం లేదా తొట్టెలో జరుపుతారు. ఇది కాథోడ్ వలె పని చేయును.
గలన విద్యుత్ విశ్లేష్యంలో ఉంచబడిన కార్బన్ కడ్డీలు ఆనోడ్ వలె పని చేయును. గలన విద్యుత్ విశ్లేష్యంను కార్బన్ పొడితో కప్పుతారు ఇది లోహం యొక్క ఆక్సీకరణంను మరియు వికిరణం వలన వేడిని కోల్పోకుండా నివారించును. తొట్టె యొక్క ఉష్ణోగ్రత దాదాపు 1173 వద్ద ఉంచుతారు. విద్యుత్ విశ్లేషణ ప్రక్రియలో క్రింది చర్యలు జరుగును.

ప్రతి కిలో అల్యూమినియమ్ ఉత్పత్తికి ఆనోడ్ నుండి 0.5కిలో కార్బన్ మండుతుంది. దీని కారణంగా ఆనోడ్లను ఎప్పటికప్పుడు మార్చుతూ ఉండవలెను.
Long Answer Questions (దీర్ఘ సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
ఒక నిర్దిష్ట విషయంలో క్షయకారిణి ఎంపిక ఉష్ణగతిక ప్రభావకంపై ఆధారపడి ఉంటుంది. రెండు ఉదాహరణలతో వివరించండి.
జవాబు:
ఒక లోహ ఆక్సైడ్ లోహంగా క్షయకరించుటకు క్షయకరణిని ఎంపిక చేయుటకు ఉష్ణగతిక అంశాలు ఉపయోగపడతాయి.
లోహా ఆక్సైడ్ల నుండి లోహం ఏర్పడినప్పుడు ప్రమాణ స్వేచ్ఛ సంశ్లేషణ శక్తి ∆G°f స్వల్ప రుణాత్మకం అని ఎల్లింగ్ హామ్ పటం నుండి స్పష్టంగా తెలియచున్నది.
మరొక విధంగా ఎల్లింగ్ హామ్ పటం నందు పైన గల లోహ ఆక్సైడ్లను వాటి క్రింద గల లోహాలు క్షయకరిస్తాయి. దీనికి కారణం ప్రమాణ స్వేచ్ఛ శక్తి మార్పు ∆G°f ఆక్సీకరణ, క్షయకరణ చర్యకు రుణాత్మకం మరియు ఇది రెండు లోహ ఆక్సైడ్ ∆G°f విలువలు భేదంనకు సమానం.
కనుక అల్యూమినియం మరియు జింక్లు రెండూను FeO ను Feగా క్షయకరించును. కాని Fe Al2O3ని Al గాను, ZnOను Zn గాను క్షయకరించలేదు. అదేవిధంగా C, ZnO ను Zn గా క్షయకరించగలదు. కాని Zn, CO ను C గా క్షయకరించలేదు
![]()
ప్రశ్న 2.
జింక్ బ్లెండ్ నుంచి జింక్ నిష్కర్షణాన్ని వివరించండి.
జవాబు:
ఇమిడి ఉన్న వివిధ దశలు:
i) సాంద్రీకరణ :
ధాతువును పొడి (ముక్కలుగా) చేసి తరువాత ప్లవన ప్రక్రియ విధానంలో సాంద్రీకరణం చేస్తారు.
ii) భర్జనం :
సాంద్రీకరణం చెందించినధాతువును అధిక గాలి సమక్షంలో దాదాపు1200K వద్ద భర్జనం చేసిన జింక్ ఆక్సైడ్ (ZnO) ఏర్పడుతుంది.
![]()
iii) క్షయకరణం :
పైన లభించిన జింక్ ఆక్సైడ్ను బొగ్గు పొడితో మిశ్రమం చేసి అగ్గి మట్టితో చేసిన రిటార్ట్ 1673K ఉష్ణోగ్రతకు వేడి చేసిన ఇది జింక్ లోహంగా క్షయకరణం చెందును.
![]()
1673K వద్ద జింక్ లోహం బాష్పస్థితిలో ఉంటుంది. స్వేదనం చేసిన ఇది ద్రవంగా మారుతుంది.
iv) విద్యుత్ శోధనం :
అపరిశుద్ధ లోహాన్ని అనోడ్గాను, శుద్ధ జింక్ లోహ రేకును కాథోడ్ గాతీసుకుంటారు. వీలిన H2SO4తో ఆమ్లీకృతం చేయబడిన ZnSO4 ద్రావణంను విద్యుత్ విశ్లేష్యంగా తీసుకొని విద్యుత్ను ప్రవహింప చేసిన శుద్ధ Zn కాథోడ్ వద్దనిక్షిప్తమవుతుంది.
ప్రశ్న 3.
బ్లాస్ట్ కొలిమిలో ఐరన్ నిష్కర్షణలో జరిగే చర్యలను వివరించండి.
జవాబు:
500-800K వద్ద (తక్కువ ఉష్ణోగ్రత అవధి)
3Fe2O3 + CO → 2Fe3O4 + CO2
Fe3O4 + 4CO → 3Fe + 4CO2
Fe2O3 + CO → 2FeO + CO2
At 900-1500K (ఎక్కువ ఉష్ణోగ్రత అవధి)
C + CO → 2CO
FeO + CO → Fe + CO2
ప్రశ్న 4.
కాపర్ పైరైటిస్ నుంచి కాపర్ నిష్కర్షణాన్ని విశదీకరించండి.
జవాబు:
∆fG° కు మరియు T కు మధ్య గ్రాఫ్ నుందు ఆక్సైడ్ ఏర్పడే Cu2O రేఖ దాదాపు పైన ఉంది కనుక ఆక్సైడ్ ధాతువులను నేరుగా లోహంగా కోక్తో క్షయకరించవచ్చు. ( C→CO మరియు C→CO2 రేఖలు రెండు500– 600K తరువాత చాలా క్రింద స్థానంలో ఉన్నవి). ఎమైనప్పటికీ చాలా ధాతువులు సల్ఫైడ్ మరియు కొన్ని ఐరన్ ను కలిగి ఉంటాయి. సల్ఫైడ్ ధాతువులను భర్జనం లేదా ప్రగలనం చేయగా ఆక్సైడ్లను ఇస్తాయి.
2Cu2S + 3O2 → 2Cu2O + 2SO2
కోకన్ను ఉపయోగించి ఆక్సైడ్ను తేలికగా లోహకాపర్గా క్షయకరించవచ్చును.
Cu2O + C → 2Cu + CO
అసలు విధానంలో సిలికాలతో మిశ్రమం చేసిన తరువాత ధాతువుకు రివర్బరేటరి కొలిమిలో వేడి చేస్తారు. ఈ కొలిమిలో ఐరన్ ఆక్సైడ్ లోహ మలంగా మరియు కాపర్ కాపర్ మాటీగాను ఉత్పత్తి అగును. ఇది Cu2S మరియు FeS లను కలిగి ఉండును.
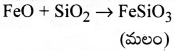
కాపర్ మాటీని సిలికా పూత ఉన్న కన్వర్టర్ లోనికి ప్రవేశపెడతారు. కొంత సిలికాను కలిపి వేడిగాలి ప్రవాహంను కన్వర్టర్లోనికి ప్రవేశపెడతారు. మిగిలిన FeS, FeO మరియు Cu2S/Cu2O లు కాపర్ మార్పుచెందును.
ఈ క్రింది చర్యలు జరుగును:
2FeS + 3O2 → 2FeO + 2SO2
FeO + SiO2 → FeSiO3
2Cu2S + 3O2 → 2Cu2O + 2SO2
2Cu2O + Cu2S → 6Cu + SO2
లభించిన కాపర్ను ఘనస్థితిలోనికి మార్చినప్పుడు SO2 విడుదలవుట వలన బ్లిస్టర్ (బొబ్బర్ల)లను కలిగి ఉండుటచే దీనిని బ్లిస్టర్ కాపర్ అంటారు.
![]()
ప్రశ్న 5.
బాక్సైట్ నుంచి అల్యూమినియమ్ నిష్కర్షణంలో ఉన్న వివిధ అంచెలను వివరించండి.
జవాబు:
- అల్యూమినియం(Al2O3) యొక్క ప్రధాన ముడి ఖనిజం అయిన బాక్సైట్లో SiO2, ఐరన్ ఆక్సైడ్(Fe2O3)లు మరియు టైటానియమ్ ఆక్సైడ్(TiO2) మలినాలు ఉంటాయి. [TS-17]
- చూర్ణం చేసిన ధాతువుకు గాఢ NaOH ద్రావణం కలిపి 473-523K ఉష్ణోగ్రత మరియు 35-36 బార్ల పీడనం వద్ద చర్య జరిపిస్తారు.
- ఈ విధంగా Al2O3 సోడియం అల్యూమినేట్గా నిక్షాళనం (SiO కూడా సోడియం సిలికేట్గా) చెందుతుంది. ఇతర మలినాలు ఉండి పోతాయి.
Al2O3(s) + 2NaOH(aq) + 3H2O(l) → 2Na[Al(OH)4](aq) - అల్యూమినేట్ క్షార ప్రవృత్తి గలది. దానిలోనికి CO2 వాయువును పంపి తటస్థీకరించి, సార్థ Al2O3 గా అవక్షేపిస్తారు.
2Na[Al(OH)4](aq) + CO2(g) → Al2O3.xH2O(s) + 2NaHCO3(aq) - సోడియం సిలికేట్ ద్రావణంలో ఉండిపోతుంది. అవక్షేపిత సార్థ అల్యూమినాను వడపోత ద్వారా వేరు పరచి, తడి లేకుండా చేసి, వేడి చేస్తే శుద్ధ Al2O3 లభిస్తుంది.
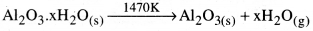
అల్యూమినా నుండి అల్యూమినియమ్ లోహ నిష్కర్షణ :
అల్యూమినా (Al2O3) దుర్బల విద్యుత్ వాహకం కనుక దీనికి క్రయోలైట్ (Na3AlF6) మరియు ఫ్లోర్స్పర్ CaF2 లను కలుపుతారు. వీటిని కలుపుట వలన అల్యూమినా యొక్క వాహకత పెరుగటయే కాక ఆ మిశ్రమం యొక్క ద్రవీభవన స్థానం దాదాపు 1140K తగ్గుతుంది.
శుద్ధ అల్యూమినా మరియు క్రయోలైట్ మిశ్రమం నుండి అల్యూమినియమ్ లోహంను విద్యుత్ విశ్లేషణ ప్రక్రియ సంగ్రహించే విధానాన్ని హాల్ -హారోల్ట్ విధానం అంటారు.

విద్యుత్ విశ్లేషణ ప్రక్రియను కార్బన్ పూత పూసిన విద్యుత్ ఘట్టం లేదా తొట్టెలో జరుపుతారు. ఇది కాథోడ్ వలె పని చేయును.
గలన విద్యుత్ విశ్లేష్యంలో ఉంచబడిన కార్బన్ కడ్డీలు ఆనోడ్ వలె పని చేయును. గలన విద్యుత్ విశ్లేష్యంను కార్బన్ పొడితో కప్పుతారు ఇది లోహం యొక్క ఆక్సీకరణంను మరియు వికిరణం వలన వేడిని కోల్పోకుండా నివారించును. తొట్టె యొక్క ఉష్ణోగ్రత దాదాపు 1173 వద్ద ఉంచుతారు. విద్యుత్ విశ్లేషణ ప్రక్రియలో క్రింది చర్యలు జరుగును.

ప్రతి కిలో అల్యూమినియమ్ ఉత్పత్తికి ఆనోడ్ నుండి 0.5కిలో కార్బన్ మండుతుంది. దీని కారణంగా ఆనోడ్లను ఎప్పటికప్పుడు మార్చుతూ ఉండవలెను.