Students get through AP Inter 2nd Year Chemistry Important Questions Lesson 3(b) రసాయన గతికశాస్త్రం which are most likely to be asked in the exam.
AP Inter 2nd Year Chemistry Important Questions Lesson 3(b) రసాయన గతికశాస్త్రం
Very Short Answer Questions (అతిస్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
ఒక చర్య వేగం లేదా రేటును నిర్వచించండి.
జవాబు:
ఏకాంక కాలములో వచ్చే క్రియాజనకముల లేదా క్రియా ఉత్పన్నముల గాఢతలోని మార్పును చర్యారేటు అంటారు.
ప్రశ్న 2.
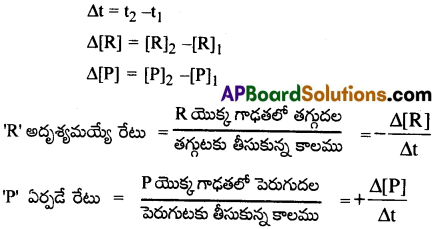
వ్యవస్థ ఘనపరిమాణం స్థిరంగా ఉంది అని ఊహించి, RP వ్యవస్థ సగటు వేగానికి సమీకరణాన్ని R, P. లలో ఉత్పాదించండి. (కాలం =’t’ సెకనులు] [R=క్రియాజనకం, P=క్రియాజన్యం]
జవాబు:
ఘన పరిమాణము స్థిరముగా ఉన్న ఒక ఊహాజనిత చర్య R→P. ఒక మోల్ క్రియాజనకము ‘R’ ఒక మోల్ క్రియా ఉత్పన్నము ‘P’ ను ఏర్పరచినది. [R]1 మరియు [P]1 లు t1 కాలము వద్ద R మరియు P ల యొక్క గాఢతలు. [R]2 మరియు [P]2 లు t2 కాలము వద్ద గాఢతలు.
ప్రశ్న 3.
రసాయన చర్యరేటు యూనిట్లు తెలపండి.
జవాబు:
మోల్. లీటర్-1 సెకన్-1.
ప్రశ్న 4.
రసాయన చర్యలలో క్రియాజనకాల గాఢతలకు (C), చర్యాకాలాలకు (t), క్రియాజన్యాల గాఢతలకు (C) చర్యా కాలాలు(t)కు మధ్య గల సంబంధాలను సూచించే రేఖా పటాలను వ్రాయండి.
జవాబు:
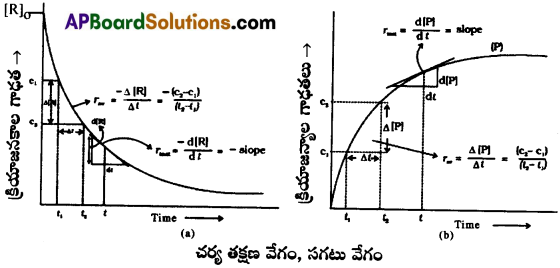
ప్రశ్న 5.
క్రింది చర్యరేటుకు సమీకరణం వ్రాయండి.
5Br–(aq) + BrO–3(aq) + 6H+(aq) → 3Br2(aq) + 3H2O(1)
జవాబు:
![]()
ప్రశ్న 6.
రేటు నియమం అంటే ఏమిటి? ఒక ఉదాహరణ ఇవ్వండి.
జవాబు:
రేటు నియమము :
ఇది ప్రయోగ పూర్వకముగా నిర్ణయించబడిన సమీకరణము. ఇది చర్యారేటుకు మరియు క్రియాజనకముల యొక్క గాఢతకు మధ్య సంబంధమును తెలియజేయును.
ఉదాహరణకు aA+bB → ఉత్పన్నములు అనే పరికల్పనాత్మక రసాయన చర్యలో రేటు ∝ [A]m [B]n, ఇచ్చట ‘m’ మరియు ‘n’ లు తుల్యం చేయబడిన సమీకరణములోని స్థాయికియోమెట్రిక్ పదాలకు సమానము కావచ్చు, కాకపోవచ్చు.
![]()
ప్రశ్న 7.
రేటు నియమంలోని గాఢత పదాల ఘాతాంకాలు, చర్య స్థాయికియోమెట్రిక్ సమీకరణంలోని గుణకాలు సమానంగా లేని ఒక చర్యను తెలపండి.
జవాబు:
చర్య: CHCl3 + Cl2 → CCl4 + HCl
రేటు సమీకరణము: రేటు = K[CHCl3][Cl2]1/2.
గాఢతల యొక్క ఘాతాంకాల పదాలు, మరియు స్థాయికియోమెట్రిక్ పదాలు ఒక్కటి కాదు.
ప్రశ్న 8.
ఒక చర్య, చర్యాక్రమాంకాన్ని నిర్వచించండి. నీ జవాబును ఒక ఉదాహరణలతో తెలపండి. [TS-15,22]
జవాబు:
రేటు నియమ సమీకరణములోని వివిధ క్రియాజనకాల గాఢత పదాల ఘాతాంకాల మొత్తాన్ని రసాయన చర్యాక్రమాంకము అంటారు.
2NO(వా) + O2(వా) → 2NO2(వా) చర్యా సమీకరణము రేటు = k[NO]²[O2]¹
కనుక మొత్తము చర్యా క్రమాంకము = 2 + 1 = 3.
ప్రశ్న 9.
ప్రాథమిక చర్యలు అంటే ఏమిటి?
జవాబు:
ఒకే సోపానంలో జరిగే రసాయన చర్యను ప్రాథమిక చర్య అంటారు.
ప్రశ్న 10.
సంక్లిష్ట చర్యలు అంటే ఏమిటి? ఒక సంక్లిష్ట చర్యను తెలపండి.
జవాబు:
ఒక రసాయన చర్య అనేక ప్రాథమిక చర్యల శ్రేణిలో జరిగి క్రియాజనకాలు, క్రియాజన్యాలుగా మారే చర్యను సంక్లిష్ట చర్యలు అంటారు.
ఉదా: ఈథేన్ ఆక్సీకరణము చెంది CO2 మరియు H2O గా మారు చర్యలో అనేక మధ్యస్థ అంచెల శ్రేణి చర్యలు జరుగును. ఈ చర్యలో ఆల్కహాల్, ఆల్డిహైడ్, మరియు ఆమ్లాలు ఏర్పడును.
ప్రశ్న 11.
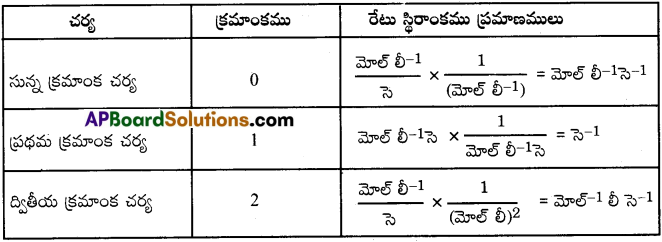
శూన్య, ప్రథమ, ద్వితీయ క్రమాంక చర్యల రేటు స్థిరాంకాలకు యూనిట్లు తెలపండి. [TS 18]
జవాబు:
రేటు స్థిరాంకము ప్రమాణములు :
ఒక సాధారణ చర్యకు aA+ bB → cC + dD
రేటు = K[A]X.[B]Y.
అయితే x + y = n= చర్యాక్రమాంకము.
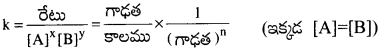
SI ప్రమాణములను తీసుకొనగా గాఢత మోల్. లీ-1 మరియు కాలము సెకన్. వివిధ క్రమాంక చర్యలకు K యొక్క ప్రమాణములు కింద ఇవ్వబడినవి.
ప్రశ్న 12.
చర్య అణుతను నిర్వచించండి. ఒక ఉదాహరణ ఇవ్వండి. [TS 22]
జవాబు:
ఏకకాలంలో తాడనాలు జరిపి రసాయన చర్యను జరపడానికి దోహదం చేసే ప్రాథమిక చర్యలో పాల్గొనే క్రియాజనక పరమాణువులు లేదా అయాన్లు లేదా అణువుల సంఖ్యను ఆ ప్రాథమిక చర్య అణుత అంటారు.
ఉదా : NH4NO2 → N2 + 2H2O (ఏక అణుత చర్య)
2HI(g) → H2(g) + I2(g) (ద్వి అణుత చర్య)
2NO(g) + O2(g) → 2NO2(g) (త్రి అణుత చర్య)
![]()
ప్రశ్న 13.
సంక్లిష్ట చర్యలో రేటు నిర్ధారణ అంచె అంటే ఏమిటి?
జవాబు:
ఒక సంక్లిష్ట చర్యకు మొత్తం చర్యారేటు ఆ చర్యలో నెమ్మదిగా సాగే ప్రాథమిక చర్య మీద ఆధారపడి ఉండును. ఈ ప్రాథమిక చర్యను రేటు నిర్ధారక దశ అంటారు.
ప్రశ్న 14.
క్షార సమక్షంలో, I– అయాన్లచే ఉత్ప్రేరణం చెందే H2O2 వియోగ చర్యా విధానాన్ని తెలపండి.
జవాబు:
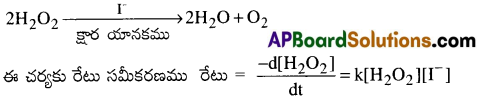
H2O2 మరియు I– ల పరంగా ఇది ప్రథమ క్రమాంక చర్య. పై చర్య ఈ కింది రెండు అంచెలలో జరుగునని తెలియుచున్నది. 1) H2O2 + I– → H2O + IO– (మెల్లగా జరిగే అంచె)
2) H2O2 + IO– → H2O + I– + O2 (వేగంగా జరిగే అంచె)
మొదటి అంచె నెమ్మదిగా జరుగు అంచె కనుక రేటు నిర్ధారక దశ అగును.
ప్రశ్న 15.
శూన్య క్రమాంక చర్యను [R], [R]0 చర్యాకాలం ‘t’ లను సంబంధపరిచే సమీకరణాన్ని వ్రాయండి.
జవాబు:
![]()
ప్రశ్న 16.
శూన్య క్రమాంక చర్యకు, క్రియాజనకం ‘R’ గాఢతకు, చర్యాకాలం ‘t’ కు గల సంబంధాన్ని తెలిపే రేఖాపటాన్ని
జవాబు:
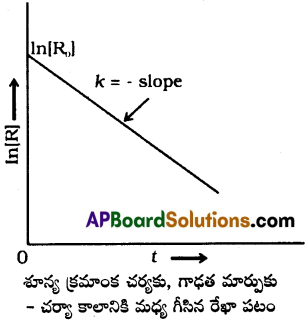

![]()
ప్రశ్న 17.
శూన్య క్రమాంక చర్యలకు రెండు ఉదాహరణలు ఇవ్వండి. [AP 19]
జవాబు:
ప్రశ్న 18.
[R], [R]0 మరియు ‘t’ పదాలలో ప్రథమ క్రమాంక చర్యకు సమాకలన సమీకరణం వ్రాయండి.
జవాబు:
ప్రశ్న 19.
వాయుస్థితిలో ఉండే ప్రథమ క్రమాంక చర్యలకు రెండు ఉదాహరణలు ఇవ్వండి. [IPE ’14][TS 19]
జవాబు:
N2O5(g) → 2NO2(g) + O2(g)
C2H4(g) + H2(g) → C2H6(g)
ప్రశ్న 20.
A(వా) → B(వా) + C(వా), నమాకలన రేటు సమీకరణాన్ని మొత్తం పీడనం ‘P’, పాక్షిక పీడనాలు PAPBPC లలో వ్రాయండి.
జవాబు:
k = \(\frac{1}{2}log\frac{1}{2}\)
pi = ప్రారంభ పీడనము
pt = మొత్తము పీడనము = PA + PB + PC
![]()
ప్రశ్న 21.
రసాయన చర్య ఆర్ధాయువు కాలం అంటే ఏమిటి?
జవాబు:
ఒక ఉదాహరణతో మీ జవాబును వివరించండి. క్రియాజనకాల ఆరంభ గాఢత విలువ సగం తగ్గుటకు అవసరమయ్యే కాలాన్ని అర్థ జీవిత కాలము అంటారు. దీనిని t1/2 తో సూచిస్తారు.
సున్న క్రమాంక చర్యకు రేటు స్థిరాంకం
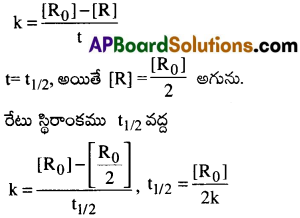
ప్రశ్న 22.
ప్రథమ క్రమాంక రసాయన చర్యలకు అర్ధాయువు కాలం (t1/2)ను, రేటు స్థిరాంకం ‘k’ ను సంబంధపరిచే సమీకరణాన్ని వ్రాయండి.
జవాబు:
ప్రథమ క్రమాంక చర్యకు రేటు స్థిరాంకము

ప్రశ్న 23.
శూన్య, ప్రథమ క్రమాంక రసాయన చర్యలకు అర్ధాయువులను లెక్కించడానికి ఉపయోగపడే సమీకరణాలు వ్రాయండి.
జవాబు:
శూన్య క్రమాంక చర్యకు t1/2 = \(\frac{[R_0]}{2k}\)
ప్రథమ క్రమాంక చర్యకు t1/2 = \(\frac{0.693}{k}\)
ప్రశ్న 24.
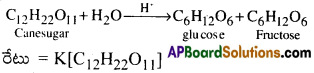
మిథ్యా ప్రథమ క్రమాంక చర్యలు అనగానేమి? ఒక ఉదాహరణ ఇవ్వండి. [AP 16]
జవాబు:
ఒక చర్య నిజానికి ప్రథమ క్రమాంక చర్య కానప్పటికి కొన్ని ఖచ్చితమైన పరిస్థితులలో ప్రథమ క్రమాంక చర్యగా మారు చర్యను మిథ్యా ప్రథమ క్రమాంక చర్య అంటారు. ఉదాహరణకు చక్కర ద్రావణము యొక్క విలోమ విన్యాస చర్య ద్వి అణుక చర్య కాని H2O గాఢత అధికముగా ఉండుటచే గాఢతలో మార్పు గమనించ తగినంతగా ఉండదు. కనుక ప్రథమ క్రమాంక చర్య అగును.
ప్రశ్న 25.
రేటు స్థిరాంకం (k) కు సంబంధించిన ఆర్హీనియస్ సమీకరణం వ్రాయండి. [AP 19]
జవాబు:
k = Ae-Ea/RT
A = అర్హీనియస్కారాణాంశం లేదా పౌనఃపున్యకారాణాంశం.
R = వాయు స్థిరాంకం
Ea = ఉత్తేజిత శక్తి,
K = రేటు స్థిరాంకము
ప్రశ్న 26.
చర్యా ఉష్ణోగ్రతను 10°C పెంచితే, రేటు స్థిరాంకం ఎన్ని రెట్లు అవుతుంది?
జవాబు:
రెండు రెట్లు
ప్రశ్న 27.
ఒక చర్యలో ఉత్తేజిత శక్తిని పటం సహాయంతో వివరించండి.
జవాబు:
ఉత్తేజిత శక్తి :
ఒక మధ్యస్థ ఉత్తేజిత సంక్లిష్టము ఏర్పడుటకు అవసరమయ్యే శక్తిని ఉత్తేజిత శక్తి అంటారు.
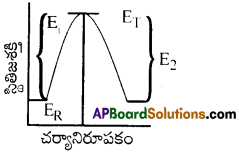
E1 = క్రియాజనకముల ఉత్తేజిత శక్తి
E2 = క్రియాజన్యాల ఉత్తేజిత శక్తి
ER = క్రియాజనకముల సగటు శక్తి
EP = క్రియాజన్యాల సగటు శక్తి
ET = అవరోధ శక్తి
![]()
ప్రశ్న 28.
ఒక రసాయన చర్యరేటు స్థిరాంకాలు k1 మరియు k2 లకు T1 మరియు T2 ఉష్ణోగ్రతల వద్ద ఉండే సంబంధం సూచించే సమీకరణాన్ని వ్రాయండి.
జవాబు:
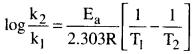
Ea = ఉత్తేజిత శక్తి
R = సార్వత్రిక వాయు స్థిరాంకము.
ప్రశ్న 29.
ఒక చర్య అభిఘాత పౌనఃపున్యం (Z) అంటే ఏమిటి? A + B → క్రియాజన్యాలు అనే చర్యకు దీని రేటుతో ఏవిధంగా సంబంధం ఉంది?
జవాబు:
ఏకాంక కాలంలో ఏకాంక ఘనపరిమాణము వద్ద జరిగే ద్విగుణాత్మక తాడనాల సంఖ్యను తాడన పౌనఃపున్యము అంటారు.
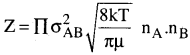
σAB = తాడన వ్యాసం
µ = క్షయీకృత ద్రవ్యరాశి; K = విశిష్టరేటు
nA మరియు nB లు A మరియు B ల అణువుల సంఖ్యలు.
ప్రశ్న 30.
ఉత్ప్రేరణం జరిగిన చర్యకు, ఉత్ప్రేరణం లేని చర్యకు స్థితిజశక్తి-చర్యానిరూపకం వీటి మధ్య రేఖా పటాలను వ్రాయండి.
జవాబు:
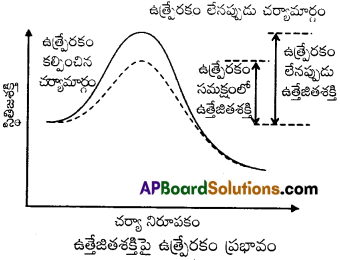
ప్రశ్న 31.
రేటు స్థిరాంకంపై ఉష్ణోగ్రత ప్రభావం తెలపండి.
జవాబు:
ఉష్ణోగ్రత పెరుగుదలతో రేటు స్థిరాంకము కూడా పెరుగును. సాధారణముగా ప్రతి 10°C ఉష్ణోగ్రత పెరుగుదలతో చర్యారేటు దాదాపు రెట్టింపు అగును.
Short Answer Questions (స్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
చర్య సగటు రేటును నిర్వచించండి. క్రింది చర్యలకు క్రియాజనకాల గాఢతలను మార్పు, క్రియాజన్యాల గాఢతల
మార్పు ద్వారా చర్యా రేటులను ఎలా వ్యక్తం చేస్తారు?
1) 2HI(g) → H2(g) + I2(g)
2) Hg(l) + Cl2(g) → HgCl2(s)
3) 5Br–(aq) + BrO–3(aq) +6H+(aq) → 3Br2(aq) +3H2O(l)
జవాబు:
ఏకాంక కాలంలో గాఢతలో జరిగే మార్పురేటును సగటు రేటు అంటారు.

ప్రశ్న 2.
రేటు సమీకరణం అంటే ఏమిటి? దీనిని ఎలా రాబడతారు? క్రింది చర్యలకు రేటు సమీకరణాలు వ్రాయండి.
1) 2NO(g) + O2(g) → 2NO2(g)
2) CHCl3 + Cl2 → CCl4 + HCl
3) CH3COOC2H5(l) + H2O(l) → CH3COOH(aq) + C2H5OH(aq)
జవాబు:
రేటు సమీకరణం లేదా రేటు నియమం :
క్రియాజనకాల గాఢత పదాల మీద చర్య రేటు ఏ విధముగా ఆధారపడి ఉందనే విషయాన్ని తెలిపే గణిత సమీకరణాన్ని రేటు సమీకరణం లేదా రేటు నియమం అంటారు.
రేటు సమీకరణం అనేది ప్రయోగం ద్వారా రాబట్టిన సమీకరణం అగును.
ఉదా :
1) 2NO(g) + O2(g) →2NO2(g) రేటు = k[NO]²[O2]
2) CHCl3 + Cl2 → CCl4 + HCl రేటు = [CHCl3][Cl2]1/2.
3) CH3COOC2H5 + H2O → CH3COOH + C2H5OH రేటు = k[CH3COOC2H5]
![]()
ప్రశ్న 3.
చర్యాక్రమాంకాన్ని నిర్వచించి వివరించండి. దీనిని ప్రయోగాత్మకంగా ఎలా నిర్ణయిస్తారు?
జవాబు:
ఒక చర్య రేటు సమీకరణంలో వివిధ గాఢత పదాల ఘాతాల మొత్తాన్ని, ఆ చర్యకు చెందిన చర్యా క్రమాంకం అంటారు.
aA + bB → ఉత్పన్నాలు అను పరికల్పనాత్మక రసాయన చర్య
రేటు సమీకరణము, రేటు = k[A]m[B]n.
పై చర్యకు చర్యాక్రమాంకము = (m + n).
‘m’ మరియు ‘n’ అను ఘాతాలకు స్థాయికియోమెట్రిక్ సమీకరణములోని పదాలు a మరియు b లకు ఏవిధమైన సంబంధము ఉండదు.
A పరంగా చర్యాక్రమాంకము m మరియు B పరంగా చర్యాక్రమాంకం n. అయితే ఘాతాల మొత్తము ఒకటి అయితే ఆ చర్యను ప్రథమ క్రమాంక చర్య అంటారు. ఘాతాల మొత్తము రెండు, మూడు అయినచో ఆ చర్యను ద్వితీయ క్రమాంక చర్య, తృతీయ క్రమాంక చర్య అంటారు.
చర్యా క్రమాంకమును ప్రయోగ పూర్వక విలువలతో నిర్ణయిస్తారు.
ఉదా : 2NO(వా) + O2(వా) → 2NO2(వా)
క్రియాజనకాలలో ఏదైన ఒకదానిని స్థిరముగా ఉంచి రెండవ క్రియాజనకము ప్రారంభ గాఢతలో మార్పును కాలంతో లెక్కగడతారు. ఇదే విధముగా రెండు క్రియాజనకములలో గాఢతలో మార్పును కూడా లెక్కగడతారు. ఈ విధముగా చేయుటవలన కింది ఫలితాలు లభించినవి.
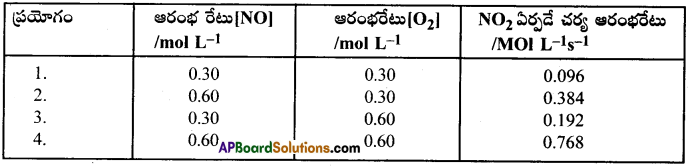
పై ఫలితాలను గమనించగా O2 గాఢతను స్థిరముగా ఉంచి NO గాఢతను రెట్టింపు చేయగా ప్రారంభ రేటు నాలుగు రెట్లు 0.096 నుండి 0.384కు పెరిగినది. ఇది చర్యరేటు. NO యొక్క గాఢత వర్గము పై ఆధారపడి ఉన్నదని తెలియజేయుచున్నది. NO గాఢతను స్థిరముగా ఉంచి O2 గాఢతను రెట్టింపు చేయగా చర్యా రేటు కూడా రెట్టింపు అయినది. అనగా చర్యారేటు O2 గాఢత మొదటి ఘాతము పై ఆధారపడి ఉన్నదని తెలియుచున్నది. కనుక ఈ చర్యకు చర్యారేటు సమీకరణమును
రేటు = k[NO]²[O2] గా సూచిస్తారు.
- రేటు = k[NO]²[O2]; మొత్తం క్రమాంకం = 2 + 1 = 3
- రేటు = [CHCl3][Cl2]1/2 ; మొత్తం క్రమాంకం = 1 + 2 = 3/2
- రేటు = k[CH3COOC2H5]; క్రమాంకం = 1
ప్రశ్న 4.
చర్యఅణుత అంటే ఏమిటి? దీనికి చర్యాక్రమాంకానికి గల భేదం ఏమిటి? ద్విఅణుత, త్రికఅణుత వాయు చర్యలను తెలపండి. [IPE ’14][AP-16,18,19][TS 17]
జవాబు:
ఏక కాలంలో తాడనాలు జరిపి రసాయన చర్యను జరపడానికి దోహదం చేసే, ప్రాథమిక చర్యలో పాల్గొనే క్రియాజనక పరమాణువుల లేదా అయాన్ల లేదా అణువుల సంఖ్యను ఆ ప్రాథమిక చర్య అణుత అంటారు.
చర్యలో ఒక రసాయన కణము పాల్గొన్నచో ఆ చర్యను ఏకాణుక చర్య అంటారు. ఉదా : అమ్మోనియం నైట్రైట్ వియోజన చెంది N2 మరియు H2Oలుగా మారుట.
NH4NO2 → N2 + 2H2O
రెండు కణాలు ఏక కాలంలో తాడనం జరిపి చర్యలో పాల్గొన్నచో దానిని ద్వి అణుక చర్య అంటారు.
ఉదా : HI వియోజనం చెంది H2 మరియు I2 లుగా మారుట.
2HI → H2 + I2
మూడు చర్యా కణాలు ఏక కాలంలో తాడనం జరిపి చర్యలో పాల్గొన్నచో ఆ చర్యను త్రిఅణుక చర్య అంటారు.
ఉదా : 2NO + O2 → 2NO2
- చర్యాక్రమాంకమును ప్రయోగ పూర్వకముగా కనుగొంటారు. దీనికి సున్న, ఇతర పూర్ణాంకాలు, భిన్నాలు కూడా విలువలుగా ఉండవచ్చు. కాని అణుతకు సున్న లేదా భిన్న విలువలుండవు. సాధారణంగా ఈ విలువ ఒకటి,. రెండు లేదా మూడు అవుతుంది.
- చర్యా క్రమాంకమును ప్రాథమిక మరియు సంక్లిష్ట చర్యలకు కూడా అనువర్తింప చేయవచ్చు. కాని అణుతను కేవలం ప్రాథమిక చర్యలకు మాత్రమే అనువర్తింప చేయాలి.
- సంక్లిష్ట చర్యలకు చర్యాక్రమాంకము నెమ్మదిగా సాగే దశ మరియు నెమ్మదిగా సాగే దశలోని అణుతను మొత్తం చర్యాక్రమాంకముగా తీసుకుంటారు.
ప్రశ్న 5.
శూన్య క్రమాంక చర్యకు సమాకలన సమీకరణాన్ని ఉత్పాదించండి.
జవాబు:
ఒక సున్న క్రమాంక చర్య → ఉత్పన్నాలు
రేటు = \(\frac{-d[R]}{dt}\) = k[R]0 = k d[R] = -kdt
ఇరువైపులా సమాకలనం చేయగా [R] =-kt +………..(1) I అనునది సమాకలన స్థిరాంకము t = 0 వద్ద, క్రియాజనకము యొక్క గాఢత R = [R]0,
ఇచట [R]0, క్రియాజనకము ప్రారంభ గాఢత. ఈ విలువలను సమీకరణము (1)లో ప్రతిక్షేపించగా
[R]0 = -k × 0 + I ⇒ [R]0 = I
I విలువను సమీకరణము (1) లో ప్రతిక్షేపించగా
[R] = -kt + [R]0 ⇒ kt= [R]0 – [R] ⇒ k = \(\frac{[R]_0-[R]}{t}\)
ఇది సున్న క్రమాంక చర్య యొక్క సమాకలన సమీకరణం.
ప్రశ్న 6.
ప్రథమ క్రమాంక చర్యకు సమాకలన సమీకరణాన్ని ఉత్పాదించండి. [AP 22]
జవాబు:
ఒక ప్రథమ క్రమాంక చర్య → ఉత్పన్నాలు
రేటు = \(\frac{-d[R]}{dt}\) = k[R] లేదా \(\frac{d[R]}{[R]}\) = -kdt
ఈ సమీకరణమును సమాకలనము చేయగా ln[R] = -kt + I …………….(1) I = సమాకలన స్థిరాంకము
t = 0 అయినపుడు, [R] = [R]0
[R]0 = క్రియాజనకము యొక్క ప్రారంభగాఢత
కనుక సమీకరణము (1) ని కింది విధముగా వ్రాయవచ్చు.
ln[R]0 – k × 0 +I ⇒ ln[R]0
I విలువను సమీకరణము (1) లో ప్రతిక్షేపించగా
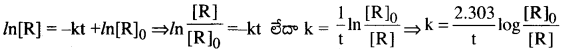
ఇది ప్రథమ క్రమాంక చర్య యొక్క సమాకలన సమీకరణము.
ప్రశ్న 7.
A(వా) → B(వా) + C(వా) వాయు సమీకరణానికి సమాకలన రేటు సమీకరణాన్ని, మొత్తం పీడనం(P), పాక్షిక పీడనాలు PA, PB, PCలలో ఉత్పాదించండి.
జవాబు:
ప్రథమ క్రమాంక వాయు ప్రావస్థ చర్య
A(వా) → B(వా) + C(వా)·
pi ను A యొక్క ప్రారంభ పీడనం, Pt ను ‘t’ కాలం తర్వాత మొత్తం పీడనం అనుకొనుము.
ఈ చర్యకు సమాకలన రేటు సమీకరణమును కింది విధముగా ఉత్పాదిస్తారు.
మొత్తం పీడనము Pt = PA +PB + PC
PA, PB మరియు PC లు వరుసగా A, B మరియు Cల యొక్క పాక్షికపీడనాలు.
t’ కాలము తర్వాత A యొక్క పీడనము x అట్మా తగ్గినది మరియు ఒక మోల్ B, ఒక మోల్ C లు ఏర్పడినవి. B మరియు C యొక్క పీడనాలు ఒక్కొక్క దానికి ‘x’ అట్మా.

ప్రశ్న 8.
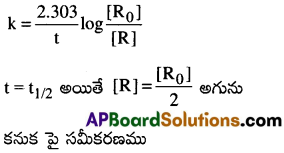
చర్య, ఆర్థాయువు కాలం (t1/2) అంటే ఏమిటి? శూన్య, ప్రథమ క్రమాంక చర్యలకు అర్ధాయువు కాలాలను కనుక్కోనే సమీకరణాలను ఉత్పాదించండి.
జవాబు:
ప్రథమ క్రమాంక చర్యకు రేటు స్థిరాంకము

ప్రశ్న 9.
ఆర్హీనియస్ సమీకరణం అంటే ఏమిటి? రేటు స్థిరాంకం (k) పై, ఉష్ణోగ్రత (T) ను పెంచితే కలిగే ప్రభావాన్ని తెలిపే సమీకరణాన్ని ఉత్పాదించండి. [AP 22]
జవాబు:
రసాయన చర్యా రేటు ఉష్ణోగ్రత పై ఏ విధముగా ఆధారపడి ఉన్నదో ఖచ్చితముగా తెలియజేయు సమీకరణమును అర్హీనియస్ సమీకరణము అంటారు.
k = A e-Ea/RT ……….(1)
ఇచట A పౌనఃపున్య అంశమానం, Ea ఉత్తేజిత శక్తి, మరియు రేటు స్థిరాంకము.
ఇరువైపులా సమీకరణము (1) ని సహజ సంవర్గమానాలను తీసుకొనగా

ప్రశ్న 10.
ఒక రసాయన చర్య గతిక శాస్త్రంపై ఉత్ప్రేరకం ప్రభావాన్ని పటం సహాయంతో వివరించండి.
జవాబు:
ఒక రసాయన చర్యలో శాశ్వత రసాయన మార్పుకు గురి కాకుండా రసాయన చర్యావేగాన్ని పెంచే పదార్థమును ఉత్ప్రేరకము అంటారు.
ఉదాహరణకు, MnO2 కింది చర్య రేటును పెంచుట ద్వారా ఉత్ప్రేరకముగా పని చేయును.
![]()
ఉత్ప్రేరకము పనిచేయు విధానమును మధ్యస్త సంశ్లేషణ సిద్ధాంతంను అనుసరించి వివరించవచ్చు. ఈ సిద్ధాంతము ప్రకారము ఉత్ప్రేరకము రసాయన చర్యలో పాల్గొని క్రియాజనక అణువులతో తాత్కాలిక బంధములను ఏర్పరుచును. ఫలితముగా ఒక మధ్యస్థ సంక్లిష్టము ఏర్పడును. ఇది చాలా అస్థిరమైనది మరియు వియోజనము చెంది ఉత్పన్నమును మరియు ఉత్ప్రేరకమును ఏర్పరుచును.
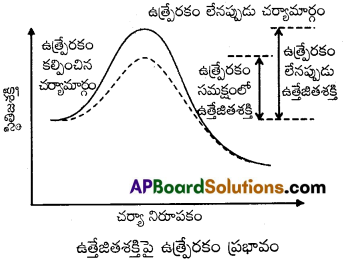
ఉత్ప్రేరకము తక్కువ ఉత్తేజిత శక్తి కలిగిన కొత్త మార్గములో చర్యను తీసుకొనిపోవును. ఉత్తేజిత శక్తి తగ్గేకొలది చర్యారేటు పెరుగును.
![]()
ప్రశ్న 11.
ద్విఅణుత చర్యల రేటులకు సంబంధించిన అభిఘాత సిద్ధాంతంలోని ముఖ్యాంశాలు వర్ణించండి. [TS-15,18,19]
జవాబు:
అణు తాడన సిద్ధాంతమును అర్హీనియస్ ప్రతిపాదించెను. ఇది వాయుస్థితిలో ద్విఅణుక చర్యారేటును వివరించును.
ముఖ్య ప్రతిపాదనలు : [AP 16,17]
- క్రియాజనక అణువులు నిర్థిష్ట దిశలో తాడనము జరుపుట వలన జరుగును.
- అన్ని తాడనములు ఉత్పన్నములను ఏర్పరచవు.
- క్రియాజనకములు, క్రియా ఉత్పన్నములను ఏర్పరుచుటకు కావలసిన కనిష్ట శక్తిని ఆరంభశక్తి (ET) అంటారు.
- సాధారణ STP పరిస్థితులలో కొద్ది అణువులు మాత్రమే ఆరంభ శక్తి (ET) ని కలిగి ఉండును. కాని అధిక సంఖ్యలో అణువులు ఆరంభ శక్తి కన్నా తక్కువ శక్తిని కలిగి ఉండును.
- ఆరంభశక్తి అవరోధాన్ని అధిగమించి రసాయన చర్యలో పాల్గొనుటకు క్రియాజనక అణువులు పొందవలసిన కనీసపు అదనపు శక్తిని ఉత్తేజిత శక్తి (Ea) అంటారు. Ea = ET – ER.
ER = క్రియాజనక అణువుల సగటు శక్తి - ఉత్తేజిత శక్తిని సంపాదించిన అణువులను ఉత్తేజిత అణువులు అంటారు. ఉత్తేజిత అణువుల మధ్య తాడనాలు చర్యకు దారితీయును. కనుక ఈ తాడనాలను ఉత్తేజిత తాడనాలు (లేదా) ఫలప్రదమైన తాడనాలు అంటారు.
- ఏకాంక కాలంలో జరిగే ద్విగుణాత్మక తాడనాల సంఖ్య (Z) తో సూచిస్తారు.
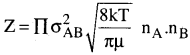
ఇచట σAB = తాడన వ్యాసము,
µ = క్షయీకృత ద్రవ్యరాశి. - విశిష్ట రేటు, k = p.z.e-Ea/RT
(లేదా) k = Ae-Ea/RT
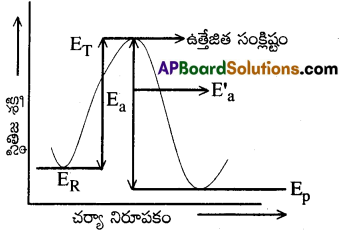
Ea = పురోగామి చర్యకు ఉత్తేజిత శక్తి [ET – ER]
E’a = తిరోగామి చర్యకు ఉత్తేజిత శక్తి [ET – EP]
Ep = క్రియాజన్యాల సగటు శక్తి
ER = క్రియాజనకాల సగటు శక్తి
ET = ఆరంభ శక్తి.
ప్రశ్న 12.
క్రింది పదాలను వివరించండి.
a) ఉత్తేజిత శక్తి(Ea)
b) అభిఘాత పౌనఃపున్యం(Z)
c) ఆర్హీనియస్ సమీకరణంలోని సంభావ్యతా కారణాంశం
జవాబు:
a) ఉత్తేజిత శక్తి :
క్రియాజనక అణువులు ఆరంభ శక్తి అవరోధాన్ని అధిగమించుటకు గ్రహించవలసిన కనీస అదనపు శక్తిని ఉత్తేజిత శక్తి అంటారు. ఆరంభ శక్తికి మరియు క్రియాజనక అణువుల సగటు గతిజశక్తికి మధ్య గల శక్తి బేధమును ఉత్తేజిత శక్తి అంటారు.
Ea = ET – ER
Ea = ఉత్తేజిత శక్తి, ET = ఆరంభ శక్తి
ER = క్రియాజనక అణువుల సగటు శక్తి
b) తాడన పౌనఃపున్యము :
ఏకాంక ఘనపరిమాణంలో ఒక సెకన్ కాలంలో క్రియాజనక అణువుల మధ్య జరిగే తాడనాలను తాడన పౌనఃపున్యము అంటారు.
c) సంభావ్యత అంశమానము :
ఒక తాడనము ఫలప్రదం కావలనంటే తాడన అణువులు కలిగి ఉన్న శక్తి ఆరంభశక్తి కంటే అధికముగా ఉండవలెను మరియు ఒక నిర్థిష్ట దిశను కలిగి ఉండవలెను.
తాడనము ప్రభావవంతం అగుటకు మరియొక అంశమానము (లేదా) సంభావ్యత అంశ మానమును కూడా పరిగణనలోనికి తీసుకొనవలెను. అర్హీనియస్ సమీకరణము కింది విధముగా మార్పు
చెందినది.
k = PZAB e-Ea/RT
P = సంభావ్యత అంశమానము.
Long Answer Questions (దీర్ఘ సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
క్రింది పదాలను, ఉదాహరణలతో వివరించండి.
జవాబు:
a) చర్యా సగటు రేటు
b) నెమ్మదిగా, వేగంగా జరిగే చర్యలు
c) చర్యాక్రమాంకం
d) చర్యఅణుత
e) చర్య ఉత్తేజిత శక్తి
జవాబు:
a) ఏకాంక కాలంలో గాఢతలోని మార్పురేటును చర్యా సగటు రేటు అంటారు.

b) రోజులు (లేదా) నెలలో పూర్తి అయ్యే చర్యలను నెమ్మదిగా సాగే చర్యలు అంటారు.
ఉదా : ఇనుము తుప్పు పట్టుట
అతి తక్కువ కాలంలో పూర్తి అయ్యే చర్యలను వేగవంత చర్యలు అంటారు.
ఉదా : ద్రావణాలలో అయానిక సమ్మేళనాల మధ్య చర్యలు
NaCl + AgNO3 → NaNO3 + AgCl↓
c) చర్యాక్రమాంకము :
రేటు సమీకరణములోని వివిధ పదార్థాల గాఢతల గాతాంకాల మొత్తాన్ని చర్యాక్రమాంకము అంటారు.
కింది ఊహాజనిత చర్యకు
aA + bB → ఉత్పన్నాలు.
ఈ చర్యకు రేటు సమీకరణము
రేటు = k[A]m[B]n.
పై చర్యకు చర్యాక్రమాంకము = (m+n).
d) చర్యా అణుత :
ఏక కాలంలో తాడనాలు జరిపి రసాయన చర్యను జరపడానికి దోహదం చేసే ప్రాథమిక చర్యలో పాల్గొనే క్రియాజనక పరమాణువుల లేదా అయాన్ల లేదా అణువుల సంఖ్యను ప్రాథమిక చర్య అణుత అంటారు.
ఒకే ఒక చర్యాకణము పాల్గొన్న రసాయన చర్యను ఏకాణుక చర్య అంటారు.
ఉదా : అమ్మోనియం నైట్రైట్ వియోజనం చెంది N2 మరియు H2O లు ఏర్పడుట
NH4NO2 → N2 + 2H2O
e) ఉత్తేజిత శక్తి :
క్రియాజనక అణువులు ఆరంభశక్తి అవరోధాన్ని అధిగమించుటకు గ్రహించవలసిన కనీస అదనపు శక్తిని ఉత్తేజిత శక్తి అంటారు.
ఆరంభశక్తికి మరియు క్రియాజనక అణువుల సగటు గతిజశక్తికి మధ్య గల శక్తి బేధమును ఉత్తేజిత శక్తి అంటారు.
![]()
ప్రశ్న 2.
శూన్య, ప్రథమ క్రమాంక చర్యలకు రెండు ఉదాహరణలు ఇవ్వండి. క్రింది చర్యలకు క్రియాజనకాల గాఢతల మార్పు, క్రియాజన్యాల గాఢతల మార్పుపరంగా, రేటులు కనుక్కోనే సమీకరణాలు వ్రాయండి.
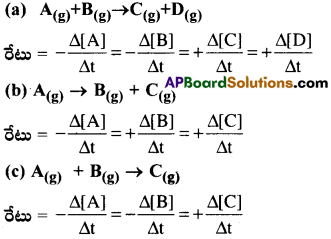
a) A(g) + B(g) → C(g) + D(g)
b) A(g) → B(g) + C(g)
c) A(g) + B(g) → C(g)
జవాబు:
శూన్య క్రమాంక చర్యలకు ఉదాహరణలు
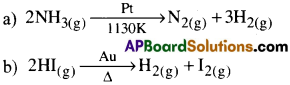
ప్రథమ క్రమాంక చర్యలకు ఉదాహరణలు
a) NH4NO2(g) → N2(g) +2H2O
b) SO2Cl2(g) →SO2(g) +Cl2(g)
చర్యలు:
ప్రశ్న 3.
ఒక చర్యరేటుపై ఉష్ణోగ్రత ప్రదర్శించే ప్రభావం గురించి చర్చించండి. ఈ సందర్భంగా సంబంధిత సమీకరణాలు ఉత్పాదించండి. [TS 15]
జవాబు:
చర్యారేటు పై ఉష్ణోగ్రతా ప్రభావము :
సాధారణముగా 10°C ఉష్ణోగ్రత పెరుగుదలలో చర్యారేటు స్థిరాంకము రెట్టింపు అగును.
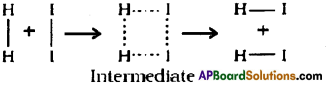
అర్హీనియస్ సిద్దాంతము ప్రకారము ఒక అణువు హైడ్రోజన్ మరియు ఒక అణువు అయోడీన్ తాడనం చెంది ఒక అస్థిరమైన మధ్యస్థ ఉత్తేజిత సంక్లిష్టమును ఏర్పరుచును. ఇది వియోగం చెంది రెండు అణువుల HI ను ఏర్పరుచును.
ఉత్తేజిత సంక్లిష్టమును ఏర్పరుచుటకు అవసరమయ్యే . శక్తిని ఉత్తేజిత శక్తి అంటారు.
అర్హీనియస్ ఇచ్చిన గణిత సమీకరణము
k = A e-Ea/RT
A = అర్హీనియస్ అంశమానము (లేదా) పౌనఃపున్య అంశమానము
E= ఉత్తేజిత శక్తి,
R = వాయు స్థిరాంకము,
T = పరమ ఉష్ణోగ్రత.
క్రియాజనకముల మరియు క్రియాజన్యముల స్వభావము పై ఎంథాల్ఫి మార్పు ఆధారపడి ఉండును.
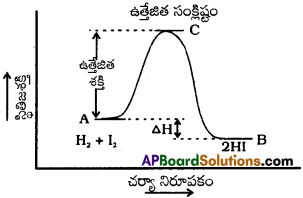
స్థితిజశక్తి-చర్యా నిరూపకాల మధ్య గీసిన రేఖాపటం
క్రియాజనక అణువులు అన్నియూ ఒకే విధమైన గతిజశక్తిని కలిగి ఉండవు. L బోల్ట్మన్ మరియు C మాక్స్వెల్ ప్రకారం గతిజశక్తి వితరణను వివరించుటకు గతిజశక్తికి మరియు అణువుల భాగమునకు (NE/NT) మధ్య గ్రాఫ్ విధానమును అనుసరించెను.
NE = E శక్తి కలిగిన అణువుల సంఖ్య
NT = మొత్తము అణువుల సంఖ్య.
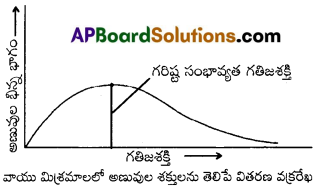
ఉష్ణోగ్రతపై ఆధారపడిన చర్యారేటును వివరించే వక్రము.
అర్హీనియస్ సమీకరణము K = A.e-Ea/RT
ఇరువైపుల సహజ సంవర్గమానములను తీసుకొనగా
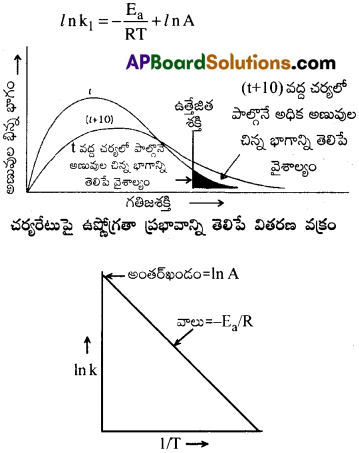
In kకు మరియు 1/T మధ్య గ్రాఫ్ గీయగా అది ఒక సరళరేఖ.
ఈ రేఖ యొక్క వాలు = –\(\frac{E_a}{R}\)
y-అక్షము పై = lnA.
పై విలువల ఆధారముగా E మరియు Aలను లెక్కగట్టవచ్చు.
![]()
ప్రశ్న 4.
ద్విఅణుత వాయు చర్యల అణు తాడన సిద్ధాంతాన్ని వివరంగా తెలపండి. [IPE ’14][AP 18][ TS-16,18]
జవాబు:
అణు తాడన సిద్ధాంతమును అర్హీనియస్ ప్రతిపాదించెను. ఇది వాయుస్థితిలో ద్విఅణుక చర్యారేటును వివరించును.
ముఖ్య ప్రతిపాదనలు :
- క్రియాజనక అణువులు నిర్థిష్ట దిశలో తాడనము జరుపుట వలన జరుగును.
- అన్ని తాడనములు ఉత్పన్నములను ఏర్పరచవు.
- క్రియాజనకములు, క్రియా ఉత్పన్నములను ఏర్పరుచుటకు కావలసిన కనిష్ట శక్తిని ఆరంభశక్తి (ET) అంటారు.
- సాధారణ STP పరిస్థితులలో కొద్ది అణువులు మాత్రమే ఆరంభ శక్తి(ET) ని కలిగి ఉండును. కాని అధిక సంఖ్యలో అణువులు ఆరంభ శక్తి కన్నా తక్కువ శక్తిని కలిగి ఉండును.
- ఆరంభశక్తి అవరోధాన్ని అధిగమించి రసాయన చర్యలో పాల్గొనుటకు క్రియాజనక అణువులు పొందవలసిన కనీసపు అదనపు శక్తిని ఉత్తేజిత శక్తి(Ea) అంటారు. Ea = ET – ER.
ER = క్రియాజనక అణువుల సగటు శక్తి - ఉత్తేజిత శక్తిని సంపాదించిన అణువులను ఉత్తేజిత అణువులు అంటారు. ఉత్తేజిత అణువుల మధ్య తాడనాలు చర్యకు దారితీయును. కనుక ఈ తాడనాలను ఉత్తేజిత తాడనాలు (లేదా) ఫలప్రదమైన తాడనాలు అంటారు.
- ఏకాంక కాలంలో జరిగే ద్విగుణాత్మక తాడనాల సంఖ్య (Z) తో సూచిస్తారు.
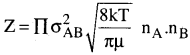
ఇచట σAB = తాడన వ్యాసము, µ = క్షయీకృత ద్రవ్యరాశి. - విశిష్ట రేటు, k = p.z.e-Ea/RT (లేదా) k = Ae-Ea/RT
బ్రోమోమీథేన్ నుండి మిథనోల్ ఏర్పడుట క్రియాజనక అణువుల దృగ్విన్యాసం మీద ఏ విధముగా ఆధారపడి ఉన్నదో కింద ఇవ్వబడినది.
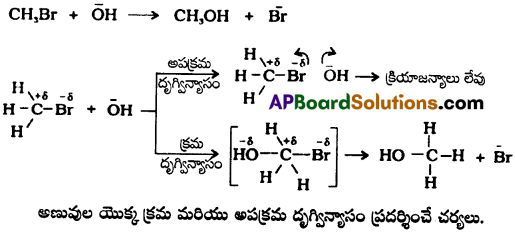
క్రియాజనక అణువులు క్రమ దృగ్విన్యాసంను కలిగి ఉన్నచో బంధములు ఏర్పడును కనుక ఉత్పన్నములు ఏర్పడును. అలాకాక అపక్రమ దృగ్విన్యాసమును కలిగి ఉన్నచో బంధములు ఏర్పడవు. తిరిగి క్రియాజనకాలుగా మారును.
ప్రభావిత తాడనాల కొరకు మరియొక అంశమానము ‘P’ (సంభావ్యతా లేదా ప్రాదేశిక అంశమానము)ను ప్రవేశపెట్టినారు. ఇది తాడనాలలో అణువులు క్రమ దృగ్విన్యాసంను కలిగి ఉండుటను పరిగణించును.
రేటు = PZAB e-Ea/RT
కనుక తాడన సిద్ధాంతము ప్రకారం ఉత్తేజిత శక్తి మరియు అణువుల క్రమ దృగ్విన్యాసం కలసి ప్రభావిత తాడనాలకు కారణమగును. కనుక రసాయన చర్యారేటును ప్రభావితం చేయును.
సంఖ్యాపరమైన దత్తాంశాలు, భావనలు ఆధారిత ప్రశ్నలు
ప్రశ్న 1.
ఒక చర్య 50% 2గంటలలోను, 75% 4 గంటల లోను పూర్తి అయింది. అయితే ఆ చర్య చర్యా క్రమాంకం ఎంత?
సాధన:
As t75% = 2t50%, ఇది ప్రథమ క్రమాంక చర్య.
ప్రశ్న 49.
ఒక చర్య అర్ధాయువు 10 నిమిషాలు. ప్రథమ క్రమాంక చర్యకు రేటు స్థిరాంకాన్ని లెక్కించండి. [TS-16]
సాధన:
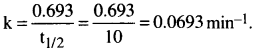
ప్రశ్న 2.
ప్రథమ క్రమాంక చర్యలో క్రియాజనకం గాఢత 0.6 mol/L నుంచి 0.2 mol/L కు 5 నిమిషాలలో తగ్గింది. చర్య రేటు స్థిరాంకం [k] ను లెక్కించండి.
సాధన:

ప్రశ్న 3.
A జరిపే శూన్య క్రమాంక చర్య రేటు స్థిరాంకం 0.0030 mol L-1s-1. A ఆరంభ గాఢత 0.10M నుంచి 0.075Mకు తగ్గడానికి ఎంతకాలం పడుతుంది?
సాధన:

ప్రశ్న 4.
ప్రథమ క్రమాంక వియోగ చర్య 30% వియోగం చెందడానికి 40 నిమిషాలు పట్టింది. దీని అర్ధాయువు కాలం t1/2 ను లెక్కించండి.
సాధన:

![]()
ప్రశ్న 5.
200-1 రేటు స్థిరాంకం గల ప్రథమ క్రమాంక చర్య అర్ధాయువు కాలం లెక్కించండి.
సాధన:
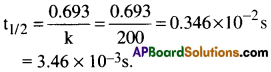
![]()
ప్రశ్న 6.
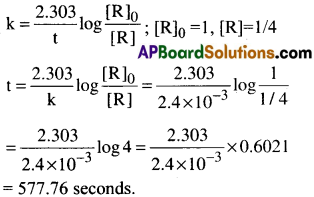
HCOOH ఉష్ట్రీయ వియోగం చర్య, ప్రథమ క్రమాంక చర్య ఒక ఉష్ణోగ్రత వద్ద రేటు స్థిరాంకం 2.4 × 10-2s-1 ఆరంభ పరిమాణంలో3/4 భాగం HCOOH వియోగం చెందడానికి ఎంతకాలం పడుతుంది.
సాధన:
ఆరంభ పరిమాణంలో 3/4 భాగం HCOOH వియోగం చెందగా మిగిలినది 1/4 భాగం.
ప్రశ్న 7.
ఒక సమ్మేళనం ప్రదర్శించే వియోగ చర్య, ప్రథమ క్రమాంక చర్యగా ఉంది. ఆరంభ పరిమాణంలో 20% చర్యలో పాల్గొనడానికి 15 నిమిషాల కాలం పడుతుంది. దీని రేటు స్థిరాంకాన్ని లెక్కించండి.
సాధన:

ప్రశ్న 8.
ఎస్టర్ జరిపే మిథ్యా ప్రథమ క్రమాంక జలవిశ్లేషణ చర్యలో కింది ప్రయోగ ఫలితాలు లభించాయి.
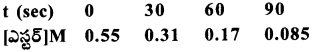
30 సె నుంచి 60 సె చర్యాకాలం వ్యవధిలో చర్య సగటు రేటును లెక్కించండి.
సాధన:
30–60 సెకన్లలో చర్య సగటు రేటు
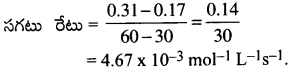
ప్రశ్న 9.
ఒక ప్రథమ క్రమాంక చర్యకు అర్ధాయువు కాలం 5 × 10-6s.రెండు గంటలు చర్యాకాలంలో ఆరంభ, క్రియాజనకం ఎంత శాతం చర్యలో పాల్గొంటుంది.
సాధన:

ప్రశ్న 10.
H2O2 పరంగా,ప్రథమక్రమాంక చర్యగా H2O2(జల) H2O(ద్రవ), O2(వా)గా వియోగం చెందుతుంది. దీని రేటు స్థిరాంక విలువ k = 1.06 × 10-3 min-1.15% నమూనా వియోగం చెందడానికి ఎంత కాలం పడతుంది?
సాధన:
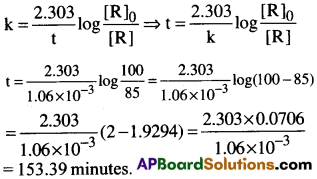
ప్రశ్న 11.
ప్రథమ క్రమాంక చర్యలో 99.9% చర్య పూర్తి కావడానికి పట్టే కాలం 50% చర్య పూర్తి కావడానికి పట్టే కాలం కంటే 10 రెట్లు ఉంటుంది అని చూపండి. (log 2 = 0.3010).
సాధన:
చర్య 99.9% శాతం పూర్తి అయినప్పుడు
[R]0 = 100, [R] = 0.1

ప్రశ్న 12.
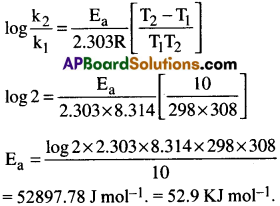
చర్య ఉష్ణోగ్రతను 298K నుంచి 308K కు పెంచినప్పుడు, రేటు స్థిరాంకం రెండు రెట్లు అయింది. చర్య ఉత్తేజిత శక్తి విలువను లెక్కించండి.
సాధన:
T1 = 298K T2 = 308K
ఉష్ణోగ్రతను 10K పెంచినప్పుడు రేటు స్థిరాంకం రెండు రెట్లు అగును.
∴ k1 = k ; k2 = 2k
R = 8.314 Jk-1mol-1
![]()
ప్రశ్న 13.
600K వద్ద ప్రథమ క్రమాంక చర్యలో C2H5I(g) C2H4(g) + HI(g) చర్యకు రేటు స్థిరాంకం ‘k’ విలువ1.60 × 10-5s-1 దీని ఉత్తేజితశక్తి 209kJ/mol 700K వద్ద ‘k’ విలువ ఎంత?
సాధన:
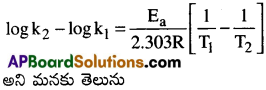
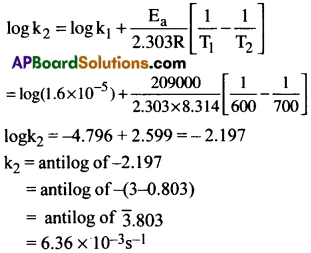
ప్రశ్న 14.
2HI(g) → H2(g) + I2(g) చర్యకు 581K వద్ద ఉత్తేజిత శక్తి 209.5 kJ/mol. ఉత్తేజిత శక్తికి సమానం అయితే, అధికమైన శక్తి గల అణువుల భిన్న భాగాన్ని లెక్కించండి. [R = 8.314 Jk-1mol-1]
సాధన:
ఇచ్చిన సందర్భంలో
Ea = 209.5 KJmol-1.
= 209500 Jmol-1.
T = 581 K,R= 8.314 Jk-1mol-1
ఇప్పుడు, క్రియాజనకాల అణువులు అధికశక్తి
ఉత్తేజితశక్తికి సమానంగా లేక అధికంగా ఉన్నప్పుడు
x = e-Ea/RT
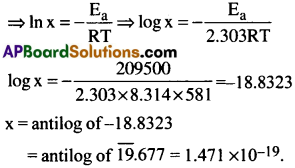
ప్రశ్న 15.
R→P, చర్యకు క్రియాజనకం గాఢత 25 నిమిషాలలో 0.03M నుంచి 0.02Mకు మార్పు చెందింది. ఈ కాల వ్యవధిలో సగటు రేటును నిమిషాలు, సెకన్లు యూనిట్లలో లెక్కించండి.
సాధన:
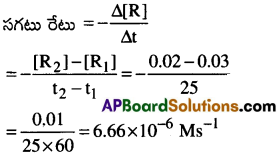
ప్రశ్న 16.
2A → క్రియాజన్యాలు చర్యలో A గాఢత 10 నిమిషాలలో 0.5 mol L-1 నుంచి 0.4 molL-1 కు మార్పు చెందింది. ఈ కాల వ్యవధిలో చర్య రేటును లెక్కించండి.
సాధన:
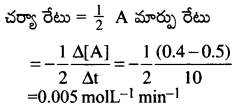
ప్రశ్న 17.
A + B → క్రియాజన్యాలు చర్యకు రేటు నియమం కింది విధంగా ఉంది r = k[A]1/2 [B]². చర్య, చర్యా క్రమాంకం ఎంత?
సాధన:
రేటు = k[A]1/2 [B]²
చర్యా క్రమాంకం = 1/2 + 2 = 2.5
ప్రశ్న 18.
X,Y గా మారే రసాయన చర్య, ద్వితీయ క్రమాంక చర్యగా ఉంది. X గాఢతను 3 రెట్లు పెంచితే, Y ఏర్పాటు రేటును ఇది ఏ విధంగా ప్రభావితం చేస్తుంది.
సాధన:
రేటు = k[X]².
r1 = k[X]²……(1); r2 = k[3X]²….(2)
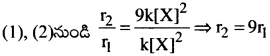
కావున X ఏర్పాటు రేటు 9 రెట్లు పెరుగుతుంది.
![]()
ప్రశ్న 19.
ప్రథమ క్రమాంకచర్య రేటు స్థిరాంకం 1.15 × 10-3s-1. క్రియాజనకం పరిమాణం 5 గ్రా. నుంచి 3 గ్రా. తగ్గడానికి ఎంతకాలం పడుతుంది?
సాధన:
ఇచ్చినది [R]0 = 5g, [R] = 3g; k = 1.15 × 10-3s-1
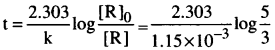
= 2.00 × 10³ (log 1.667)
= 2.00 × 10³ × 0.2219 = 443.8s = 444s.
ప్రశ్న 20.
SO2Cl2 ఆరంభ పరిమాణంలో సగానికి వియోగం చెందడానికి 60 నిమిషాల కాలం పట్టింది. ఈ వియోగ చర్య, ప్రథమ క్రమాంక చర్య, చర్య రేటు స్థిరాంకాన్ని లెక్కించండి.
సాధన:
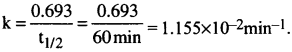
ప్రశ్న 21.
కింది చర్యలకు, వాటి రేటు సమీకరణాల నుంచి చర్యా క్రమాంకాలను లెక్కించండి. రేటు స్థిరాంకాల యూనిట్లు కూడా తెలపండి.
(i) 3NO(g) → N2O(g) Rate = k[NO]²
(ii) H2O2(aq) + 3I–(aq) + 2H+ → 2H2O(l) + I–3
Rate = k[H2O2][I–]
(iii) CH3CHO(g) → CH4(g) + CO(g)
Rate = k[CH3CHO]3/2
(iv) C2H5Cl(g) → C2H4(g) + HCl(g)
Rate = k[C2H5Cl]
సాధన:
(i) రేటు = k[NO]²
చర్య క్రమాంకం = 2

ప్రశ్న 22.
2A + B → A,B, చర్యకు, రేటు = k[A][B]² k = 2.0 × 10-6v mol-2L²s-1.[A] = 0.1mol.L-1, [B] = 0.2mol.L-1. అయితే ఆరంభ రేటును లెక్కించండి. [A] 0.06 mol. L-1కు తగ్గినప్పుడు చర్య రేటును లెక్కించండి.
సాధన:
ప్రారంభ రేటు =k[A][B] 2 = 2.0 × 10-6 × 0.1 × (0.2)²
= 8 × 10-9mol L-1s-1
[A] ను 0.10mol L-1 నుంచి 0.06 mol L-1 కు తగ్గించినప్పుడు
అంటే A 0.04 mol L-1 చర్యలో పాల్గొంది.
B = 1/2 × 0.004 mol L-1
= 0.02 mol L-1
ఇప్పుడు [B] = 0.2 – 0.002 = 0.18 mol L-1
రేటు = 2.0 × 10-6 × 0.06 × (0.18)²
= 3.89 × 10-9 mol L-1s-1
ప్రశ్న 23.
ప్లాటినమ్ ఉపరితలం పై NH3 వియోగ చర్య, శూన్య క్రమాంక చర్య k= 2.5 × 10-4 mol-1s-1 అయితే N2, H2లు ఏర్పడే రేట్లను లెక్కించండి.
సాధన:

ప్రశ్న 24.
డై మిథైల్ ఈథర్ వియోగ చర్యకు రేటు సమీకరణాన్ని పాక్షిక పీడనాలలో కింది విధంగా రాస్తారు. రేటు =k(pCH3OCH)3/2 పీడనాన్ని బార్లలోను, కాలాన్ని నిమిషాలలోను వ్యక్తం చేస్తే రేటు, రేటు స్థిరాంకం యూనిట్లను తెలపండి.
సాధన:
డైమిథైల్ ఈథర్ వియోగ చర్య
CH3-O-CH3 → CH4 + H2 + CO
చర్యా రేటు
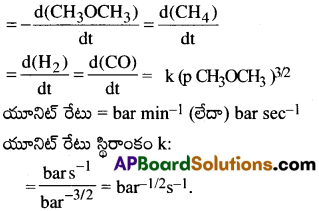
ప్రశ్న 25.
ఒక క్రియాజన్యం పరంగా, ఒక చర్య, ద్వితీయ క్రమాంక చర్యగా ఉంది. క్రియాజనకం గాఢతను కింది విధంగా మార్చినప్పుడు దీని రేటు ఎలా మారుతుంది?
(i) రెండు రెట్లు (ii)సగానికి
సాధన:
రేటు = k[A]² = ka²
i) [A]=2a,అయిన రేటు= k(2a)² = 4ka2 = 4 రెట్లు
ii) [A] = a/2, రేటు = k(a/2)² = 1/4 ka²
= 1/4 times.
![]()
ప్రశ్న 26.
ఒక చర్య A లో ప్రథమ క్రమాంక చర్యగా, Bలో ద్వితీయ క్రమాంక చర్యగా ఉంది.
(i) దీనికి అవకలను రేటు సమీకరణం రాయండి.
(ii) B గాఢతను 3 రెట్లు చేస్తే, రేటు ఎలా మారుతుంది?
(iii) A,B రెండింటి గాఢతలను రెండు రెట్లు చేస్తే రేటు ఎలా మారుతుంది?
సాధన:
(i) రేటు=k[A][B]²
(ii) రేటు = kab²
[B] గాఢతను 3 రెట్లు చేసినప్పుడు
రేటు = ka (3b)² = 9kab² = 9 times.
(iii) [A], [B] లను రెండు రెట్లు చేసినప్పుడు
రేటు = k(2a)(2b)² = 8kab2 =8 times.
ప్రశ్న 27.
A, Bల మధ్య జరిగే చర్యకు కింద ఇచ్చిన విధంగా A, B ల ఆరంభ గాఢత పరంగా చర్య ఆరంభ రేటు (r) ను నిర్ణయించారు.

చర్య క్రమాంకాలను A పరంగా, B పరంగా రాయండి
సాధన:
రేటు నియమం r0 = k[A]m[B]n అనుకొనుము.
(r0)1 = 5.07 × 10-5 = (0.20)m (0.30)n → (1)
(r0)2 = 5.07 × 10-5 = (0.20)m (0.10)n → (2)
(r0)3 = 7.16 × 10-5 = (0.40)m (0.05)n → (3)
(1) ను (2)తో భాగారించగా
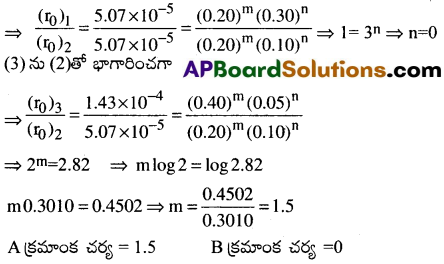
ప్రశ్న 28.
2A + B → C+D చర్య గతికశాస్త్ర అధ్యయనంలో కింది ఫలితాలు లభించాయి.

చర్యకు రేటు నియమాన్ని, రేటు స్థిరాంకాన్ని కనుక్కోండి.
సాధన:
క్రియాజనకం A కు సంబంధించి క్రమాంక చర్య m, మరియు Bకు సంబంధించి క్రమాంక చర్య n అనుకొనుము.
అప్పుడు రేటు నియమం = k[A]m[B]n.
ప్రయోగపు నాలుగు విలువలను ప్రతిక్షేపించగా
(రేటు)ప్రయోగం1 = 6.0 × 10-3 = k(0.1)m(0.1)n
(రేటు)ప్రయోగం2 = 7.2 ×10-2 = k(0.3)m(0.2)n
(రేటు)ప్రయోగం3 = 2.88 × 10-1 = k(0.3)m(0.4)n
(రేటు)ప్రయోగం4 = 2.4 × 10-2 = k(0.3)m(0.1)n

ప్రశ్న 29.
ప్రథమ క్రమాంక చర్య రేటు స్థిరాంకం 60s-1. క్రియాజనకం ఆరంభ గాఢత 1/16 వంతుగా మారడానికి చర్యకు ఎంత కాలం పడుతుంది?
సాధన:

ప్రశ్న 30.
ప్రథమ క్రమాంక చర్యకు 99% చర్య పూర్తికావడానికి పట్టే చర్యా కాలం, 90% చర్య పూర్తి కావడానికి పట్టే కాలానికి రెండు రెట్లు అని రుజువు చేయండి.
సాధన:
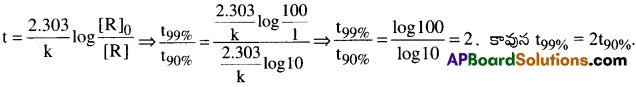
ప్రశ్న 31.
543K వద్ద ఎజోఐసోప్రోపేన్, హెక్సేన్ N2 గా విఘటనం చెందే చర్యలో కింది ఫలితాలు లభించాయి.

రేటు స్థిరాంకాన్ని లెక్కించండి.
సాధన:
(CH3)2CHN = NCH(CH3)2 → N2(g) + C6H14(g)
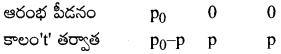
కాలం ‘t’ తర్వాత మొత్తం పీడనం
pt = (p0 – p) + p + p = p0 + p (లేదా) p = pt – p0
[R]0 ∝ p0 and [R] ∝ p0 – p (లేదా) pవిలువను
ప్రతిక్షపించగా [R]0 ∝ 2p0 – pt
ఎజోఐసోప్రోపేన్ విఘటన చర్య ప్రథమ క్రమాంక చర్య కావున

![]()
ప్రశ్న 32.
స్థిర ఘనపరిమాణం వద్ద SO2CI2 ప్రథమ క్రమాంక చర్యగా ఉష్ట్రీయ వియోగం చెందినప్పుడు కింది ఫలితాలు లభించాయి.

ఆరంభ పీడనం 0.65 atm అయినప్పుడు చర్య రేటు లెక్కించండి.
సాధన:
SO2Cl2(g) → SO2(g) + Cl2(g)

Pt = 0.65 atm i.e., P0 + p = 0.65atm
p = 0.65 – P0 = 0.65 – 0.50 = 0.15 atm
కాలం t వద్ద SO2Cl2 పీడనం = P0 – p
= 0.50 – 0.15 atm = 0.35 atm
ఆ సమయంలో రేటు = k × pSO2Cl2
=2.2316 × 10-3 × 0.35
= 7.8 × 10-5 atm s-1.
ప్రశ్న 33.
546K వద్ద హైడ్రోకార్బన్ల వియోగ చర్య రేటు స్థిరాంకం 2.418 × 10-5s-1 ఉత్తేజిత శక్తి 179.9 kJ/mol.పూర్వ ఘాతాంక కారణాంశం విలువ P ఎంత?
సాధన:
8 k = 2.4186 × 10-5s-1,
Ea = 179.9 kJmol-1. T = 546 K.

ప్రశ్న 34.
k = 2.0 × 10-2s-1తో A → క్రియాజన్యాలు చర్యలో A గాఢత 1.0 molL-1 అయితే 100 సెకన్ల తరువాత ఎంత మిగులుతుంది.
సాధన:
k యూనిట్ల ద్వారా ఇది ప్రథమ క్రమాంక చర్య అని

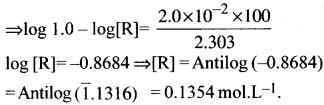
ప్రశ్న 35.
t1/2 = 3.00 గంటలు ఉన్న ప్రథమ క్రమాంకాన్ని ప్రదర్శించే గ్లూకోజ్, ఫ్రక్టోజ్ ఆమ్ల సమక్షంలో వియోగం చెందే సుక్రోజ్ చర్యకు సంబంధించి 8 గంటల తర్వాత ఎంత భాగం సుక్రోజ్ వియోగం చెందకుండా మిగిలి ఉంటుంది?
సాధన:
ప్రథమ క్రమాంక చర్య సమాకలన ఆధారంగా సుక్రోజ్

![]()
ప్రశ్న 36.
హైడ్రోకార్బన్ వియోగం కింది సమీకరణాన్ని ప్రదర్శించింది. k = (4.5 × 1011s-1) e-28000k/T. Ea ను లెక్కించండి.
సాధన:
అర్హీనియస్ సమీకరణం ప్రకారం

ప్రశ్న 37.
HaOa ప్రథమ క్రమాంక చర్యగా వియోగం చెందే చర్యకు రేటు స్థిరాంకాన్ని కింది విధంగా రాస్తాం. logk = 14.34 – 1.25 × 104K/T. ఈ చర్యకు E్నను లెక్కించండి. ఏ ఉష్ణోగ్రత వద్ద దీని అర్ధాయువు కాలం విలువ 256 నిమిషాలుగా ఉంటుంది?
సాధన:
అర్హీనియస్ సమీకరణం ప్రకారం
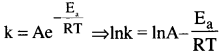

![]()
ప్రశ్న 38.
A క్రియాజన్యాలుగా మారే ఒక చర్య k విలువ 10°C వద్ద 4.5 × 10³s-1. దీని ఉత్తేజిత శక్తి 60 kJ mol-1. ఏ. ఉష్ణోగ్రత వద్ద దీని k విలువ 1.5 × 104 s-1 గా ఉంటుంది?
సాధన:
k1 = 4.5 × 10³s-1
T1 = 10 + 273 = 283K
k2 = 1.5 × 104s-1 = 1; T2 = ?
Ea = 60kJmol-1,

Textual Solved Problems (సాధించిన సమస్యలు)
ప్రశ్న 1.
318K వద్ద CCl4 లో కరిగించిన N2O5 వియోగాన్ని, ద్రావణంలో N2O5 గాఢత 2.33 mol L-1, 184 నిమిషాల చర్యా కాలం తరవాత అది 2.08mol L-1కు తగ్గింది.చర్య కింది సమీకరణం ద్వారా జరుగుతుంది.
2N2O5 → 4NO2(g) + O2(g)
కాబట్టి ఈ చర్య రేటును, గంటలు, నిమిషాలు, సెకన్ల పరంగా లెక్కించండి. ఈ వ్యవధులలో NO2 ఏర్పడే చర్య రేటు ఎంత?
సాధన:

ప్రశ్న 2.
రేటు సమాసాలు కింది విధంగా గల చర్యల మొత్తం చర్యా క్రమాంకాలను లెక్కించండి.
(a) రేటు = k[A]1/2[B]3/2
(b)రేటు = k[A]3/2[B]-1
సాధన:
(a) రేటు = k[A]X[B]Y
చర్యా క్రమాంకం = x + y
కాబట్టి చర్యా క్రమాంకం = 1/2 + 3/2 = 2 చర్యా క్రమాంకం “రెండు”.
(b) dog (šárošo = 3/2 + (−1) = 1/2 అర్థ క్రమాంక చర్య.
ప్రశ్న 3.
ప్రథమ క్రమాంక చర్యలో
N2O5 → 2NO2(వా)+ 1/2O2(వా)
N2O5 ఆరంభ గాఢత 318 K వద్ద 1.24 × 10-2 mol L-160 నిమిషాల చర్యా కాలం తరవాత N2O5 గాఢత 0.20 ×10-2 mol L-1. 318K వద్ద రేటు స్థిరాంకాన్ని లెక్కించండి.
సాధన:
ప్రథమ క్రమాంక చర్యకు

ప్రశ్న 4.
ప్రథమ క్రమాంక చర్యకు రేటు స్థిరాంకం k = 5.5 × 10-14 s-1. చర్య అర్ధాయువు కాలం నిర్ణయించండి. [AP 15]
సాధన:
ప్రథమ క్రమాంక చర్య అర్ధాయువు.
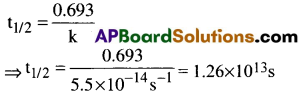
![]()
ప్రశ్న 5.
కింది చర్య సూచించిన ఇథైల్ అయోడైడ్ విఘటనానికి ప్రథమ క్రమాంక చర్య రేటు స్థిరాంకం 600K వద్ద 1.60 × 10-5 s-1 C2H5I(g) → C2H4(g) + HI(g) ఈ చర్య ఉత్తేజిత శక్తి 209 kJ/mol 700K వద్ద రేటు స్థిరాంకాన్ని లెక్కించండి.
సాధన:
