Students get through AP Inter 1st Year Chemistry Important Questions 9th Lesson S బ్లాక్ మూలకాలు which are most likely to be asked in the exam.
AP Inter 1st Year Chemistry Important Questions 9th Lesson S బ్లాక్ మూలకాలు
Very Short Answer Questions (అతిస్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
ఆవర్తన పట్టికలో కర్ణ సంబంధం ఉండటానికి గల కారాణాలను తెలపండి. [Imp.Q]
జవాబు:
ఆవర్తన పట్టికలో కర్ణ సంబంధం ఉండటానికి గల కారాణాలు:
a) సరూప అయానిక మరియు పరమాణు పరిమాణం కలిగి ఉండటం.
b) సమాన ఋణవిద్యుదాత్మకత విలువలు కలిగి ఉండును.
c) సారుప్య మూలకాల ఒకే ధృవణతా సామర్థ్యం కలిగి ఉండటం.
ప్రశ్న 2.
K, Rb. ల ఎలక్ట్రాన్ విన్యాసాలను పూర్తిగా రాయండి. ³
జవాబు:
‘K’ (Z = 19) యొక్క ఎలక్ట్రాన్ విన్యాసం 1s² 2s² 2p6 3s² 3p6 4s¹
‘Rb’ (Z= 37) యొక్క ఎలక్ట్రాన్ విన్యాసం 1s² 2s² 2p6 3s² 3p6 4s² 3d10 4p6 5s¹
ప్రశ్న 3.
లిథియమ్ లవణాలు చాలావరకు ఆర్ద్రీకృతమై ఉంటాయి. ఎందుకు? [TS 18,22][Imp.Q]
జవాబు:
Li+ అయాన్ యొక్క హైడ్రేషన్ ఎంథాల్పీ చాలా ఎక్కువ. దీనికి హైడ్రేషన్ ఎంథాల్పీ అవధి ఎక్కువ. కావున Li+ లవణాలు చాలా ఆర్ద్రీకృతమై ఉంటాయి,
ఉదా: LiCl.2H2O
ప్రశ్న 4.
క్షారలోహాలలో దేనికి అసాధారణ సాంద్రత ఉంటుంది? గ్రూపు 1 మూలకాల సాంద్రతల మార్పుల క్రమం ఏమిటి? [AP 18] [Imp.Q]
జవాబు:
a) పొటాషియం అసాధారణ సాంద్రత కలిగి ఉన్నది.
కారణం: i) ఖాళీ 3d ఆర్బిటాళ్లు ఉండటం.
ii) స్ఫటికజాలకంలో అంతరాణుక పరమాణువుల మధ్య దూరం ఎక్కువ..
b) IA గ్రూపు మూలకాల సాంద్రత క్రమం: LiK<Rb<Cs.
ప్రశ్న 5.
సోడియమ్ కంటే లిథియమ్ నీటితో జరిపే చర్యాతీక్షణత తక్కువ. కారణాలను తెలపండి.
జవాబు:
లిథియంకు పరమాణు పరిమాణం తక్కువ మరియు హైడ్రేషన్ శక్తి ఎక్కువ. అందువలన సోడియం కంటే లిథియమ్ నీటితో చర్య జరిపే తీక్షణత తక్కువ.
![]()
ప్రశ్న 6.
క్షారలోహాల హాలైడ్లలో లిథియమ్ అయొడైడ్ అత్యధిక కోవలెంట్ ధర్మం కలది. కారణాలను తెలపండి.జవాబు:
జవాబు:
క్షారలోహాల హలైడ్లలో లిథియం అయొడైడ్ అత్యధిక కోవలెంట్ ధర్మం కలది.
కారణాలు:
- Li+ అయాన్కు ధుృవణతా సామర్థ్యం ఎక్కువ.
- Li+ కు పరమాణు పరిమాణం ఎక్కువ.
- Li+ అయాన్ ఎలక్ట్రాన్ సమూహంను I– అయాన్ పై విస్తారం చేయు సామర్థ్యం ఎక్కువ.
ప్రశ్న 7.
క్షారలోహ హైడ్రోజన్ కార్బొనేట్ కంటే లిథియమ్ హైడ్రోజన్ కార్బొనేట్ ఏ విధంగా విభేదిస్తుంది? [Imp.Q]
జవాబు:
క్షార లోహాల హైడ్రోజన్ కార్బొనేట్ లు ఘనపదార్థాలు.
లిథియంకు తక్కువ ధనవిద్యుదాత్మకత స్వభావం ఉండటం వలన అది ఘన హైడ్రోజన్ కార్బొనేట్ను ఏర్పరచదు. లిథియం హైడ్రోజన్ కార్బొనేట్ తప్ప మిగిలిన క్షార లోహాల హైడ్రోజన్ కార్బొనేట్లు వేడి చేయగా విఘటనం చెందును.
![]()
ప్రశ్న 8.
ఏవైనా రెండు క్షారమృత్తిక లోహాల ఎలక్ట్రానిక్ విన్యాసాలను పూర్తిగా రాయండి.
జవాబు:
‘Mg’ (Z = 12) యొక్క ఎలక్ట్రాన్ విన్యాసం 1s² 2s² 2p6 3s²
‘Ca’ (Z = 20) యొక్క ఎలక్ట్రాన్ విన్యాసం 1s² 2s² 2p6 3s² 3p6 4s²
ప్రశ్న 9.
క్షారమృత్తిక లోహాల ద్రవీభవన, బాష్పీభవన స్థానాల మార్పుల గురించి చెప్పండి.
జవాబు:
క్షార మృత్తిక లోహాల యొక్క ద్రవీభవన భాష్పీభవన స్థానాలు వాటి సంబంధిత క్షారలోహాల ద్రవీభవన, భాష్పీభవనస్థానాల కంటే ఎక్కువగా ఉంటాయి. దీనికి కారణం వాటి తక్కువ పరిమాణం.
ప్రశ్న 10.
గ్రూపు 2 మూలకాలు జ్వాలకు కలిగించే స్వాభావిక రంగులు ఏమిటి? [Imp.Q][TS 22]
జవాబు:
బెరిలియం, మెగ్నిషియం తప్ప మిగిలిన క్షారమృత్తిక లోహాలన్ని ఉద్రిక్త స్థాయిలోకి ఎలక్ట్రాన్లను పంపించడం ద్వారా వాటి స్వభావిక రంగులను ప్రదర్శించును.
కాల్షియం – ఇటుక ఎరుపు
స్ట్రాన్షియం – కెంపు
బెరియం – రంగులేదు
రెడియం – కెంపు
ప్రశ్న 11.
‘మిల్క్ ఆఫ్ మెగ్నీషియా’ అని దేనిని పిలుస్తారు? ఒక ఉపయోగాన్ని వ్రాయండి. [AP 15]
జవాబు:
మెగ్నీషియమ్ హైడ్రాక్సైడ్ నీటితో ఏర్పర్చే అవలంబనాన్ని “మిల్క్ ఆఫ్ మెగ్నీషియా” అంటారు. (Mg(OH)2.)
ఉపయోగాలు:
- దీనిని వైద్యంలో ఆమ్ల విరోధిగా వాడతారు.
- టూత్పేస్టులలో మెగ్నీషియమ్ కార్బొనేట్ను ఒక ఘటక పదార్థంగా వాడతారు.
![]()
ప్రశ్న 12.
మెగ్నీషియమ్ లోహాన్ని గాలిలో మండిస్తే ఏం జరుగుతుంది? [AP 17,19][TS 15,18]
జవాబు:
మెగ్నీషియం లోహాన్ని గాలిలో మండిస్తే కాంతివంతంగా మండి MgO మరియు Mg, N2 లను ఏర్పరచును.
2 Mg + O2 → 2MgO
3 Mg + N2 → Mg3N2
ప్రశ్న 13.
లిథియమ్ కార్బొనేటికి మిగిలిన క్షారలోహాల కార్బొనేట్లవలె ఉష్ణ స్థిరత్వం లేదు. వివరించండి. [Imp.Q]
జవాబు:
లిథియం కార్బొనేటు మిగిలిన క్షార లోహాల కార్బొనేట్ల వలె ఉష్ణస్థిరత్వం లేదు.
వివరణ:
లిథియం కార్బొనేటు తక్కువ పరమాణు పరిమాణం కలదు. ఇది CO-23 అయానన్ను ధృవణత చెందించి స్థిరమైన Li2O మరియు CO2.లను ఏర్పరచును.
గ్రుపులో కిందికి వెళ్ళే కొలది ధన విద్యుదాత్మకత పెరిగి కార్బొనేట్ల ఉష్ణస్థిరత్వం పెరుగును.
ప్రశ్న 14.
గ్రూపు 2 లోహాలు ద్రవ అమ్మోనియాలో అమ్మోనియేటెడ్ లోహ అయాన్లు ఏర్పడటానికి తుల్య సమీకరణాన్ని రాయండి.
జవాబు:
క్షార మృత్తిక లోహాలు ద్రవ అమ్మోనియాలో కరిగి చిక్కని నీలం నలుపు రంగు గల ద్రావణాలను ఏర్పరచును. ఇందులో అమ్మోనియేటెడ్ అయాన్లు ఏర్పరచును.
M+(x+y)NH3 → [M(NH3)x]+2 + 2[e(NH3)y]–
ప్రశ్న 15.
క్షారమృత్తిక లోహాల ఫ్లోరైడ్లు నీటిలో ఆయా క్లోరైడ్ల కంటే అల్ప ద్రావణీయత ఉన్నవి. ఎందుకు? [Imp.Q]
జవాబు:
క్షారమృత్తిక లోహాల ఫ్లోరైడ్లు నీటిలో ఆయా క్లోరైడ్ల కంటే అల్ప ద్రావణీయత కలిగి ఉన్నవి. దీనికి కారణం ఫ్లోరైడ్లకు అధిక జాలక శక్తి కలిగి ఉండును.
ప్రశ్న 16.
ఆర్ద్ర Mg(NO3)2 ని వేడిచేస్తే ఏమౌతుంది? దానికి తుల్య సమీకరణాన్ని ఇవ్వండి. [AP 22]
జవాబు:
Mg(NO3)2 వేడి చేయగా అది విఘటనం చెంది MgO.ను ఏర్పరుచును.
2Mg(NO3)2 → 2MgO + 4NO2 + O2
ప్రశ్న 17.
క్షారమృత్తిక లోహ హైడ్రాక్సైడ్ల జల ద్రావణీయత గ్రూపులో పై నుంచి కిందికి పెరుగుతుంది. ఎందుకో చెప్పండి. [AP 20][Imp.Q]
జవాబు:
క్షార మృత్తిక లోహాల హైడ్రాక్సైడ్లో ఉమ్మడిగా కనిపించే ఆనయాన్, కాటయాన్ వ్యాసార్థం జాలక ఎంథాల్పీని ప్రభావితం చేయును. హైడ్రేషన్ ఎంథాల్పీ, జాలక ఎంథాల్పీ కంటే ఎక్కువ. అందువల్ల అయానిక పరిమాణం పెరుగును. కావున ద్రావణీయత పెరుగును.
![]()
ప్రశ్న 18.
క్షారమృత్తిక లోహాల కార్బొనేట్ల, సల్ఫేట్ల జలద్రావణీయత గ్రూపులో కిందికి పోయినకొద్దీ ఎందుకు తగ్గుతుంది.
జవాబు:
అనయాన్ పరిమాణం కాటయాన్ కంటే చాలా ఎక్కువ. గ్రూపులో జాలక ఎంథాల్పీ విలువలు దాదాపుగా సమానంగా ఉండును. గ్రూపులో హైడ్రేషన్ ఎంథాల్పీ తగ్గటం వలన క్షారమృత్తిక లోహ కార్బోనేట్లు, సల్ఫేట్ల ద్రావణీయత తగ్గును.
ప్రశ్న 19.
పోర్ట్ లాండ్ సిమెంట్ సగటు సంఘటనాన్ని తెలపండి.
జవాబు:
పోర్ట్లాండ్ సిమెంట్ సగటు సంఘటనం
CaO = 50 – 60%
SiO2 = 20-25%
Al2O3 = 5 – 10% MgO = 2 – 3% Fe2O3 = 1 – 2% మరియు SO2 = 1 – 2%
ప్రశ్న 20.
సిమెంట్కి జిప్సమ్ని ఎందుకు కలుపుతారు? [Imp.Q][TS 15,17,19]
జవాబు:
సిమెంటు జిప్సం కలుపుట వలన సెట్టింగ్ క్రమంగా జరిగి సిమెంట్ తగినంత గట్టిపడుతుంది.
ప్రశ్న 21.
ప్రకృతిలో క్షారలోహాలు స్వేచ్ఛా స్థితిలో ఎందుకు దొరకవు? [Mar’13][AP 17][Imp.Q]
జవాబు:
క్షారలోహాలు చాలా చురుకైనవి. అందుచేత అవి స్వేచ్ఛా స్థితిలో దొరకవు. ఎప్పుడూ సంయోగస్థితిలోనే దొరుకుతాయి. ప్రకృతిలో భూతలంపైన అవి విస్తారంగా వితరణ చెంది ఉంటాయి. పరిమాణు సంఖ్య పెరిగే కొలదీ వాటి విస్తృతి తగ్గుతుంది. Na మరియు K లు అతి విస్తారంగా దొరికే క్షారలోహాలు. అవి వాటి హాలైడ్లుగా ఎక్కువగా దొరుకుతాయి. క్షార లోహాలు త్వరితగతిన ఎలక్ట్రాన్ కోల్పోయి M+ గా మారుతాయి.
ప్రశ్న 22.
సాల్వే పద్ధతిలో పొటాషియమ్ కార్బొనేట్ని తయారుచేయలేం. ఎందుకు? [AP 19]
జవాబు:
పోటాషియం కార్బొనేట్ను సాల్వే పద్ధతిలో తయారు చేయలేము.
వివరణ:
పొటాషియం బై కార్బొనేట్ అధిక ద్రావణీయత కలిగియుండును. అమ్మోనియం బైకార్బొనేట్ను సంతృప్త KClకు కలుపగా అవక్షేపం ఏర్పడును.
ప్రశ్న 23.
కాప్టిక్ సోడా లేదా సోడియం హైడ్రాక్సైడ్ ముఖ్యమైన ఉపయోగాలను వివరించండి. [AP 15][TS 16,18,19]
జవాబు:
- సబ్బు, కాగితం, రేయాన్ పరిశ్రమలలో NaOH ని వాడతారు.
- పెట్రోలియంను శుద్ధి చేయడంలో వాడతారు.
- నూలును మెర్సిరైజ్ చేయడానికి వాడతారు.
- ప్రయోగశాలలో కారకంగాను వాడతారు.
ప్రశ్న 24.
సోడియమ్ కార్బొనేట్ ముఖ్య ఉపయోగాలను వివరించండి. [AP 20][Imp.Q]
జవాబు:
Na2CO3 ఉపయోగాలు:
- నీటిలోని కఠినత్వాన్ని తొలగించుటకు ఉపయోగిస్తారు.
- దీనిని గాజు,కాస్టిక్ సోడా తయారిలో ఉపయోగిస్తారు.
- లాండ్రీలలో ఉపయోగిస్తారు.
- కాగితం, రంగుల, వస్త్ర పరిశ్రమలలో ఉపయోగిస్తారు.
![]()
ప్రశ్న 25.
పొడిసున్నం ముఖ్య ఉపయోగాలను వివరించండి. [AP 19][IPE ’14] [Imp.Q]
జవాబు:
పొడిసున్నం ఉపయోగాలు:
- రంజన ద్రవ్యాలను తయారు చేయుటలో ఉపయోగిస్తారు.
- Na2CO3, NaOH తయారీలో ఉపయోగిస్తారు.
ప్రశ్న 26.
i) BeCl2 (బాష్పం) ii) BeCl2 (ఘనపదార్ధం) ల నిర్మాణాలను గీయండి.
జవాబు:
a) BeCl2 (బాష్పం) నిర్మాణం : BeCl2 భాష్ప స్థితిలో డైమర్గా ప్రవర్తించును.
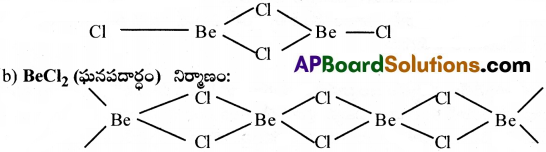
ప్రశ్న 27.
ప్లాస్టర్ ఆఫ్ పారిస్ ప్రాముఖ్యతను వివరించండి. [Imp.Q][AP 17,19]
జవాబు:
ప్లాస్టర్ ఆఫ్ పారిస్ ఉపయోగాలు:
- వైద్య రంగంలో విరిగిన ఎముకలను సరైన స్థానాలలో స్థాపితం చేయడానికి మరియు దంతవైద్యంలో వాడతారు.
- సుద్ద ముక్కలను తయారుచేయుటలో వాడతారు.
- ఆటబొమ్మలను తయారుచేయుటలో వాడతారు.
ప్రశ్న 28.
క్షారమృత్తిక లోహాల కార్బోనేట్లలో దేనికి అధిక ఉష్ణస్థిరత్వం ఉంటుంది? ఎందుకు?
జవాబు:
క్షారమృత్తిక లోహా కార్బోనేట్ అన్నింటిలో BaCO3 అధిక ఉష్ణస్థిరత్వాన్ని కలిగి ఉన్నది.
కారణం:
కాటయాన్ పరిమాణం పెరిగిన కొలది ఉష్ణస్థిరత్వం పెరుగును. కావున BaCO3 అధిక ఉష్ణ స్థిరత్వాన్ని కలిగి ఉన్నది.
ప్రశ్న 29.
(i) Na2O2 నీరు రసాయన చర్య (ii) నీటితో KO చర్య లకు తుల్య సమీకరణాలను రాయండి.
జవాబు:
- Na2O2 + 2H2O → NaOH + H2O2
- K2O + H2O → 2KOH
ప్రశ్న 30.
జీవ శాస్త్రంలో Mg+2 యొక్క ప్రాముఖ్యతను తెలపండి? [May’10]
జవాబు:
- చెట్లలోని ఆకుపచ్చ పదార్థమైన క్లోరోఫిల్లో Mg+2ఒక ఘటక పదార్థం.
- జంతుకణాలలో Mg+2 అయాన్ల గాఢత ఎక్కువగా వుంటుంది.
- ఫాస్ఫో హైడ్రోలేజ్లు, ఫాస్పోట్రాన్స్ఫరేజ్లు లాంటి ఎంజైమ్లలో Mg+2 వుంటుంది. ఈ ఎంజైమ్లు ATP చర్యలలో పాల్గొంటాయి. ఈ ప్రక్రియలో శక్తి విడుదల వుంటుంది. Mg+2, ATP లతో సంక్లిష్టం ఏర్పరుస్తుంది
ప్రశ్న 31.
కణం పనిచేయడంలో Ca+2 ప్రాముఖ్యతను తెలపండి? [May’10]
జవాబు:
- Ca+2 ఎముకలలోను, పళ్ళలోను వుంటుంది.
- రక్తం గడ్డ కట్టడానికి Ca+2 అయాన్లు అవసరం.
- గుండె క్రమంగా కొట్టుకోవడానికి Ca+2 అయాన్లు అవసరం.
- కండరాలు ముడుచుకుపోవడానికి Ca+2 అయాన్లు అవసరం.
ప్రశ్న 32.
ప్లాస్టర్ ఆఫ్ పారిస్ ను ఏ విధంగా తయారుచేస్తారు? [AP 22][TS 16,17]
జవాబు:
120° వద్ద జిప్సమ్ను వేడిచేయుట వల్ల ప్లాస్టర్ ఆఫ్ పారిస్ ఏర్పడుతుంది.
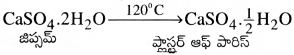
![]()
ప్రశ్న 33.
సోడియం బై కార్బోనేట్ ఉపయోగాలను రాయండి.
జవాబు:
సోడియం బై కార్బొనేట్(NaHCO3) ను బేకింగ్ సోడా అందురు.
సోడియం బై కార్బోనేట్ ఉపయోగాలు :
- దీనిని మందుల తయారీలో యాంటి సెప్టిక్ గా ఉపయోగిస్తారు.
- దీనిని శీతల పానీయాల తయారిలో ఉపయోగిస్తారు.
- దీనిని అగ్నిమాపకాలలో CO2 నివ్వడానికి వాడతారు.
- దీనిని వంటలలో బేకింగ్ పౌడర్గా వాడుతారు.
Short Answer Questions (స్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
కాష్టనర్-కెల్నర్ పద్ధతి గురించి మీకేమి తెలుసు? దానిలో ఉన్న సూత్రాన్ని రాయండి.
జవాబు:
కాష్టనర్ కెల్నర్ పద్ధతి అనునది NaOH ను పారిశ్రామిక పద్ధతిలో ఉత్పత్తిచేయు పద్ధతి.
సూత్రం:
ఈ పద్ధతిలో మెర్కురిని కాథోడ్గా ఉపయోగించి బ్రైన్ ద్రావణాన్ని విద్యుద్విశ్లేషణం చేయుట ద్వారా తయారు చేస్తారు.
ఆనోడ్ వద్ద క్లోరిన్ వాయువు, కాథోడ్ వద్ద సోడియం అమాల్గం ఏర్పడతాయి.
ఈ సోడియం అమాల్గం నీటితో చర్య జరిపి NaOH ద్రావణం మరియు H2 వాయువులను ఇస్తాయి.
ఘట చర్యలు:

దీనిని మెర్కురీ -కాథోడ్ పద్ధతి అని కూడా అంటారు.
ప్రశ్న 2.
ఆక్సీకరణ జ్వాలకు క్షారలోహాలు, వాటి సమ్మేళనాలు స్వాభావిక రంగులను ఇస్తాయి. కారణాలను వివరించండి.
జవాబు:
ఆక్సీకరణ జ్వాలకు క్షారలోహాలు, వాటి సమ్మేళనాలు స్వాభావిక రంగులను ఇస్తాయి.
వివరణ:
జ్వాల నుండి వెలువడే ఉష్ణం బాహ్య కర్పరంలోని ఎలక్ట్రానన్ను అధిక శక్తి స్థాయికి ఉద్రిక్తపరుస్తాయి. అధికశక్తి స్థాయిలోని ఎలక్ట్రాన్ శక్తిని విడుదల చేసి భూస్థాయికి చేరును. ఇది దృగ్గోచర ప్రాంతంలో ఉండును.
ప్రశ్న 3.
సాల్వే పద్దతిలో జరిగే వివిధ చర్యలను చర్చించండి. [AP 16]
జవాబు:
గాఢ సోడియం క్లోరైడ్ ద్రావణాన్ని అమ్మోనియాతో సంతృప్త పరిచి దానిలోకి CO2 వాయువును పంపితే అమ్మోనియం బైకార్బొనేట్ తయారవుతుంది.
2NH3 + H2O + CO2 → (NH4)2CO3
(NH4)2CO3 + H2O + CO2 → 2NH3HCO3
అమ్మోనియం బైకార్బొనేట్ సోడియం క్లోరైడ్ తో చర్య జరిపి సోడియం బైకార్బొనేట్ ఏర్పరుచును.
NH4HCO3 + NaCl → NaHCO3 + NH4Cl
సోడియంబైకార్బొనేట్ స్ఫటికాలను వేడి చేస్తే సోడియం కార్బొనేట్ ఏర్పడును.
![]()
NH4Cl ఉన్న ద్రావణాన్ని Ca(OH)2 తో ప్రతిక్రియను చేసి ఈ పద్ధతిలో NH3 ని పునఃప్రాప్తి చేసుకొంటారు. కాల్షియం క్లోరైడ్ సహజనితంగా వస్తుంది.
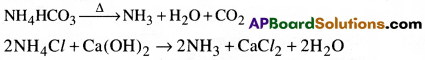
Textual Solved Problems (సాధించిన సమస్యలు)
ప్రశ్న 1.
i) మెగ్నీషియమ్న గాలిలో వేడి చేస్తే
ii) పొడిసున్నాన్ని సిలికాతో వేడిచేస్తే
iii) తడిసున్నంతో క్లోరీనచర్య
iv) కాల్షియమ్ నైట్రైట్ని బాగా వేడిచేస్తే ఏం జరుగుతుంది?
జవాబు:
i) Mg ని గాలిలో మండించినప్పుడు కాంతివంతంగా మండి MgO మరియు Mg3 N2 ఏర్పడును.

ii) పొడిసున్నాన్ని సిలికాతో వేడిచేస్తే కాల్షియం సిలికేట్ ఏర్పడును.
CaO + SiO2 → CaSiO3
iii) తడి సున్నం క్లోరిన్తో చర్య జరిపి బ్లీచింగ్ పౌడర్ను ఏర్పరచును.
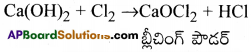
iv) కాల్షియం నైట్రైట్ను బాగా వేడిచేస్తే ఆక్సైడ్ ఏర్పడును.
![]()
ప్రశ్న 2.
జీవశాస్త్ర ప్రవాహికల్లో సోడియమ్, పొటాషియమ్, మెగ్నీషియమ్, కాల్షియమ్లు సార్థకతను వివరించండి. [TS 16,17]
జవాబు:
జీవశాస్త్ర ప్రవాహికల్లో సోడియమ్, పొటాషియమ్ ప్రాముఖ్యత:
- కణాల్లోని కర్బన అణువులతో ఉన్న ఋణావేశాలను లోహ అయాన్ల పై నుండే ఆవేశాలు తుల్యం చేస్తాయి. కణాలలో ద్రవాభిసరణ పీడనాన్ని కూడా నిలకడగా ఉంచడానికి ఈ అయాన్లు సహాయపడతాయి.
- కణాల నుంచి Na+ అయాన్లు బహిష్కృతమవుతాయి. ఈ అయాన్ రవాణా చర్యలను “సోడియం పంప్” అంటారు. అయితే K+ అయాన్లు బహిష్కృతం కావు. Na+ అయాన్లను బయటికి పంపివేయడానికి లేదా K+ అయాన్లను లోపలికి తీసుకోవటానికి జల విశ్లేషణ వల్ల సాధ్యమవుతుంది.
- కణపు పొరకు అటు ఇటు పక్కల Na+, K+ అయాన్లుంటాయి. దీని వల్ల కణంలో విద్యుత్ శక్మం ఏర్పడుతుంది. Na+ అయాన్లుండటం వల్ల గ్లూకోజ్ కణం లోపలికి వెళుతుంది. అధికంగా ఉన్న Na+ అయాన్లు బహిష్కృతమవుతాయి. ఎమినో ఆమ్లాల చలనాలు కూడా ఇదే మాదిరిగా ఉంటాయి.
- పొటాషియమ్ అయాన్లు కణాంతర్భాగంలో గ్లూకోజ్ జీవన క్రియల్లో దోహదపడతాయి. ప్రోటీన్ల సంశ్లేషణలోనూ, కొన్ని నిర్దిష్టమైన ఎంజైమ్లు ఉత్తేజితమవడానికి సహాయపడుతుంది.
జీవశాస్త్రంలో Mg2+ పాత్ర: [May’13, Mar’13]
- జంతు కణాలలో Mg2+ అయాన్ల గాఢత ఎక్కువగా ఉంటుంది.
- ఫాస్ఫోహైడ్రోలేజ్లు, ఫాస్ఫోట్రాన్స్ఫరేజ్లు లాంటి ఎంజైములలో Mg2+ ఉంటుంది. ఈ ఎంజైములు ATP చర్యలలో పాల్గొంటాయి. శక్తి విడుదల ఈ ప్రక్రియలో జరుగుతుంది Mg2+ ATP తో సంక్లిష్టం ఏర్పరుస్తుంది.
- క్లోరోఫిల్లో Mg2+ ఒక ఘటక పదార్థం. కోర్లోఫిల్ చెట్లలోని ఆకుపచ్చ పదార్థం.
జీవశాస్త్రంలోCa2+ పాత్ర:
- మన శరీరంలో 99% కాల్షియం అయాన్లు ఎముకలు మరియు దంతాల తయారీలో ఉపయోగపడుతుంది. రక్త స్కందనములో (గడ్డ కట్టడంలో) మరియు కణ పొర అయాన్ బదిలీ ప్రక్రియలలో ఈ అయాన్ ముఖ్య పాత్ర వహిస్తుంది.
- హార్మోన్లు కాల్షియం గాఢతను ప్లాస్మాలో సుమారుగా 100 మి.గ్రా/లీ. గా వుంచుతాయి. కాల్ఫిటోనిన్ మరియు పెరాథైరాయిడ్ అనే హార్మోన్లు అనేవి కాల్షియం అయాన్ గాఢతను స్థిరీకరించడంలో ప్రముఖంగా తోడ్పడతాయి. పై ప్రక్రియలతో పాటు కాల్షియం అయాన్లు గుండె క్రమంగా కొట్టుకోనే ప్రక్రియలో మరియు కండరాల సంకోచ (ముడుచుకునే) ప్రక్రియలలో కూడా ముఖ్య పాత్రను వహిస్తాయి.
![]()
ప్రశ్న 3.
సిమెంట్ని గురించి కొన్ని వాక్యాలు రాయండి.
జవాబు:
సిమెంట్:
సిమెంట్ భవన నిర్మాణంలో ముఖ్య పదార్థం. దీనినే పోర్ట్ లాండ్ సిమెంట్ అంటారు. సున్నం (CaO) ఎక్కువగా ఉండే పదార్థాన్ని సిలికా (SiO2) ఎక్కువగా ఉండే బంక మట్టితోను Al, Fe మరియు Mg.ఆక్సైడ్లను కలిపితే వచ్చే సంకలిత పదార్థం సిమెంట్.
ముడి పదార్థాలు:
సిమెంట్ తయారిలో ముడిపదార్థాలు (i)సున్నపు రాయి (ii) బంక మన్ను (iii) జిప్సం
బంకమట్టిని సున్నంతో కలిపి బాగావేడి చేస్తే అవి ద్రవీభవించి చర్య జరిపి సిమెంట్ క్లింకర్ను ఏర్పరుచును. ఈ క్లింకర్కు 2-3% జిప్సం కలుపగా సిమెంట్ వస్తుంది. పోర్ట్లాండ్ సిమెంట్లో ఉండే ఘటక పదార్థాలు డైకాల్షియం సిలికేట్ (Ca2SiO4)26%, ట్రైకాల్షియం సిలికేట్ (Ca3SiO4) 51% మరియు ట్రైకాల్షియం అలూమినేట్ (Ca3Al2O6) 11%.
సిమెంట్ గట్టిపడటం:
సిమెంట్కు నీటిని కలిపితే గట్టి పదార్థంగా ఏర్పడుతుంది. ఈ ప్రక్రియను సెట్టింగ్ ఆఫ్ సిమెంట్ అంటారు. సిమెంట్లో ఉండే అణువుల ఆర్ద్రీకరణ చర్య వల్లనూ, వాటి పునర్వ్యవస్థీకరణ జరగడం వల్లనూ పై మార్పు జరుగుతుంది. జిప్సమ్ని వాడటం సెట్టింగ్ ఆఫ్ సిమెంట్ని నెమ్మదిగా జరపడం కోసమే. దీనివల్ల సిమెంట్ తగినంతగా గట్టిపడుతుంది.
ఉపయోగాలు:
- దీనిని కాంక్రీట్ మరియు ప్రబలిత కాంక్రీట్లలో ఉపయోగిస్తారు.
- ప్లాస్టరింగ్లో ఉపయోగిస్తారు.
- వారధులకు, డ్యామ్లను, భవంతుల నిర్మాణంలో ఉపయోగిస్తారు.
ప్రశ్న 4.
Be, Al తో కర్ణ సంబంధం కలిగి ఉంటుంది. చర్చించండి.
జవాబు:
ఈ క్రింది పేర్కొనబడిన అంశాల ఆధారంగా Be తో Al కర్ణ సంబంధం కలిగి ఉండునని చెప్పవచ్చు.
i) Be మరియు Alలు ఒకే ఋణవిద్యుదాత్మకత విలువ (1.50)కలిగి ఉన్నవి.
ii) Be మరియు Al సమ్మేళనాలు రెండు జలవిశ్లేషణ చెందును.
BeCl2 + 2H2O → Be(OH)2 + 2HCl
AlCl3 + 3H2O → Al(OH)3 + 3HCl
iii) Be మరియు Al లు రెండూ, గాఢ HNO3.తో చర్య జరపవు.
iv) Be మరియు Al లు రెండూ, సంక్లిష్ట సమ్మేళనాలను ఏర్పరచును.
v) Be మరియు Al లు రెండూ, క్షారములతో చర్య జరిపి బెరిలేట్లను, అల్యూమినేట్లను ఏర్పరచును.
Be + 2NaOH → Na2BeO2 + H2
2Al + 2 NaOH + 2H2O → 2NaAlO2 + 3H2
vi) Be మరియు Al ల యొక్క కార్బైడ్లు రెండూ, నీటితో చర్య చెంది మీథేన్ వాయువును విడుదల చేయును.
Be2C + 4H2O → 2Be(OH)2 + CH4
Al4Cl3 + 12 H2O → 4Al(OH)3 + 3CH4
![]()
ప్రశ్న 5.
Mg లోహం ముఖ్య ఉపయోగాలను చెప్పండి. [TS 19]
జవాబు:
‘Mg’ ఉపయోగాలు:
- Mg లోహం Al, Zn, Mn మరియు Sn లతో ముఖ్యమైన మిశ్రమ లోహాలను ఏర్పరచును.
- Mgపొడి మరియు రిబ్బన్లను ఫ్లాష్ బల్బులలో, ఇన్సెండియర్ బాంబ్లు మరియు సిగ్నల్లలో ఉపయోగిస్తారు.
- మిల్క్ ఆఫ్ మెగ్నీషియం Mg (OH)2 ను ఆమ్లవిరోధిగా ఉపయోగిస్తారు.
- MgCO3 ను టూత్పేస్ట్లలో ఉపయోగిస్తారు.
ప్రశ్న 6.
కాంతి విద్యుత్ ఘటాల ఎలక్ట్రోడ్లుగా సీసియమ్, పొటాషియమ్ల ఏ ధర్మాలు ఉపయోగపడతాయి?
జవాబు:
క్షారలోహాలు వాటి జ్వాల పరీక్షల ద్వారా గుర్తించవచ్చు. మరియు జ్వాల ఫోటోమెట్రి ద్వారా కనుగొనవచ్చు. కాంతితో ఈ లోహాలను చర్య జరిపినప్పుడు, ఆ లోహపరమాణువు ఎలక్ట్రాన్ కోల్పోవుటకు సరైన శక్తిని శోషించుకొనును. కావున సీసియమ్, పొటాషియంలను కాంతి విద్యుద్ఘాటాలు ఎలక్ట్రోడ్లుగా ఉపయోగపడతాయి..
ప్రశ్న 7.
వాషింగ్ సోడా ధర్మాలను రాయండి.
జవాబు:
వాషింగ్ సోడా ధర్మాలు:
- Na2CO3 తెల్లటి (రంగులేని) స్ఫటిక ఘనపదార్థం.
- Na2CO3 డెకా హైడ్రేట్గా ఉండును. దీనినే వాషింగ్ సోడా NaCO3.10H2O అంటారు.
- Na2CO3 నీటిలో కరుగును.
- Na2CO310H2O వేడిచేయగా నీటి అణువులను కోల్పోయి మోనోహైడ్రేట్ గా మారును. దీనిని 373K కంటే ఎక్కువగా వేడిచేసినపుడు సోడా యాషన్ను ఏర్పరచును.
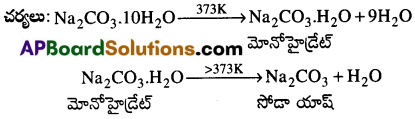
Na2CO3 జలద్రావణం క్షారస్వభావం కలిగియుండును. (PH > 7) ఇది ఆనయానిక్ జలవిశ్లేషణ వలన
CO-23 + H2O → HCO–3 + OH–
ప్రశ్న 8.
ద్రవ అమ్మోనియాలో క్షార లోహాలను కరిగిస్తే, ద్రావణానికి వివిధ రంగులు వస్తాయి. ఈ రకమైన రంగుల్లో మార్పుకు కారణాలను వివరించండి.
జవాబు:
1) క్షార లోహాలు అమ్మోనియా ద్రావణంలో నీలం రంగు ద్రావణంను ఏర్పరుస్తాయి. ఇవి వాహకతను కలిగి ఉంటాయి.
M+(x + y)NH3 →[M(NH3)x]+ +[e(NH3)y]–
2) ఈ నీలం రంగు అమ్మోనియేటెడ్ ఎలక్ట్రాన్ల వలన ఏర్పడుతుంది. ఈ ఎలక్ట్రాన్లు శక్తిని దృగ్గోచరశ్రేణిలో శోషించుకుని నీలం రంగును కలిగిస్తాయి.
3) ఈ ద్రావణాలు పార అయస్కాంత స్వభావం కలిగి ఉంటాయి. ఇవి అలానే ఉంచగా H2 వాయువును విడుదల చేస్తాయి.
M+ + e– + NH3 → MNH2 + \(\frac{1}{2}\) H2
4) ఈ గాఢ ద్రావణాన్ని వేడి చేయగా కంచు రంగులోనికి మారును. ఇది డయా అయస్కాంత స్వభావం కలిగియుండును.
ప్రశ్న 9.
(i) సోడియమ్ లోహాన్ని నీటిలో వేస్తే ఏమి జరుగుతుంది?
(ii) సోడియమ్ లోహానికి గాలిని స్వేచ్ఛగా సరఫరా చేస్తే ఏమి జరుగుతుంది.
(iii) సోడియం పెరాక్సైడ్ పై నీటి చర్య
జవాబు:
(i) సోడియం లోహాన్ని నీటిలో వేస్తే H2 వాయువును విడుదల చేస్తాయి.
2Na + 2H2O → 2NaOH + H2
(ii) సోడియం లోహానికి గాలిని స్వేచ్ఛగా సరఫరా చేస్తే సోడియం పెరాక్సైడ్ ఏర్పడును.
![]()
(iii) సోడియం పెరాక్సైడ్ నీటిలో కరిగి సోడియం హైడ్రాక్సైడ్ మరియు హైడ్రోజన్ పెరాక్సైడ్ లను ఏర్పరచును.
Na2O2 + 2H2O → 2NaOH + H2O2
![]()
ప్రశ్న 10.
కింది పరిశీలనలను మీరు ఎట్లా వివరిస్తారు?
i) BeO దాదాపు కరగదు, కానీ BeSO4 నీటిలో కరుగుతుంది.
ii) BaO నీటిలో కరుగుతుంది, కానీ BaSO4 కరగదు.
జవాబు:
i) BeO కు ద్విస్వభావం కలదు. దీని యొక్క సంయోజనీయ స్వభావం వలన BeO కు ద్రావణీయత నీటిలో తక్కువ. Be+2 కు ఎక్కువ హైడ్రేషన్ శక్తి కలిగి ఉండుట వలన BeSO4 నీటిలో కరుగుతుంది.
ii) BaO నీటిలో కరుగును. దీనికి కారణం అధిక అయానిక స్వభావం.
BaSO4 నీటిలో కరుగదు. ఎందువలన అనగా Ba+2 అయాన్కు తక్కువ హైడ్రేషన్ శక్తి కలిగి ఉండును.