Students get through AP Inter 1st Year Chemistry Important Questions 11th Lesson P బ్లాక్ మూలకాలు – 14వ గ్రూప్ which are most likely to be asked in the exam.
AP Inter 1st Year Chemistry Important Questions 11th Lesson P బ్లాక్ మూలకాలు – 14వ గ్రూప్
Very Short Answer Questions (అతిస్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
గ్రూపు 14 మూలకాల ఆక్సీకరణ స్థితులలో మార్పును చర్చించండి.
జవాబు:
- 14వ గ్రూపు మూలకాలు సాధారణంగా +4 మరియు +2 ఆక్సీకరణ స్థితులు ప్రదర్శిస్తాయి.
- గ్రూపులో క్రింది మూలకాలు +2 ఆక్సీకరణ స్థితిని ప్రదర్శిస్తాయి.
- +2 ఆక్సీకరణ స్థితి ప్రదర్శించే స్వభావం Ge < Sn< Pb.
- Pb +2 ఆక్సీకరణ స్థితి ప్రదర్శిస్తుంది. కారణం జడ ఎలక్ట్రాన్ జంట స్వభావం.
ప్రశ్న 2.
ఈ కింది సమ్మేళనాలు నీటితో ఎలా ప్రవర్తిస్తాయి? (a) BCl3 (b) CCl4 [Imp.Q]
జవాబు:
a) BCl3 నీటితో చర్యజరిపి బోరిక్ ఆమ్లం ఏర్పరచును.
![]()
b) CCl4 ను Fe లేదా Cu సమక్షంలో అధిక ఉష్ణోగ్రత గల నీటి ఆవిరితో చర్య చెందించగా ఫాన్ విడుదలగును.
![]()
ప్రశ్న 3.
BCl3, SiCl4 ఎలక్ట్రాన్ కొరత ఉన్న సమ్మేళనాలా? వివరించండి.
జవాబు:
- BCl3 మరియు SiCl4 లు ఎలక్ట్రాన్ కొరత సమ్మేళనాలు.
- ఇవి రెండు కూడా లూయీ ఆమ్లాలుగా పనిచేస్తాయి.
- ఇవి ఎలక్ట్రాన్ జంటలను స్వీకరిస్తాయి.
- ఈ క్రింది చర్యలు ఈ సమ్మేళనాలు ఎలక్ట్రాన్ కొరత సమ్మేళనాలుగా ధృవపరుస్తాయి.
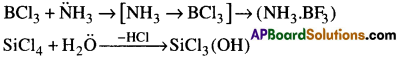
ప్రశ్న 4.
ఈ కింది వాటిలో కార్బన్ సంకరీకరణాన్ని సూచించండి. [Imp.Q] [IPE ’14][AP,TS 16,18]
a) CO-23 b) వజ్రం c) గ్రాఫైట్ d) ఫుల్లరీన్ [Imp.Q]
జవాబు:
a) CO-23 లో ‘C’ పరమాణువు సంకరీకరణం. sp².
b) వజ్రంలో ‘C’ పరమాణువు సంకరీకరణం sp³.
c) గ్రాఫైట్ ‘C’ పరమాణువు సంకరీకరణం sp².
d) ఫుల్లరీన్ లో ‘C’ పరమాణువు సంకరీకరణం sp².
ప్రశ్న 5.
CO ఎందుకు విషపూరితమైంది? [Imp.Q][AP, TS 16,18]
జవాబు:
కార్బన్ మోనాక్సైడు అధిక విష స్వభావం రావడానికి దానికి హెమోగ్లోబిన్తో సంక్లిష్టం ఏర్పరచే సామర్థ్యం ఉండుటయే. అంతేకాక ఆ సంక్లిష్టానికి ఆక్సిజన్ హిమోగ్లోబిన్ సంక్లిష్టం కన్నా 300 రెట్లు ఎక్కువ స్థిరత్వం ఉంటుంది. ఎర్ర రక్త కణాలలోని హెమోగ్లోబిన్ ఆక్సిజన్ ను శరీరమంతా తీసుకొని పోకుండా కార్బన్మైనాక్సైడ్ హెమోగ్లోబిన్ ఏర్పడిన సంక్లిష్టం అడ్డుకొంటుంది, ఫలితంగా చివరకు మరణం సంభవిస్తుంది.
![]()
ప్రశ్న 6.
రూపాంతరత అంటే ఏమిటి? స్ఫటిక రూపంలోని కార్బన్ భిన్న రూపాంతరాలను తెలపండి. [May’13,Mar’13] [TS 22] [AP 16,20]
జవాబు:
ఒకే మూలకం వివిధ భౌతిక రూపాలలో ఉండి ఒకేరకమైన రసాయన ధర్మాలు కలిగి ఉండుటను రూపాంతరత అంటారు. కార్బన్ యొక్క స్ఫటిక రూపాంతరాలు వజ్రం, గ్రాఫైట్.
ప్రశ్న 7.
కింది ఆక్సైడ్లను తటస్థ, ఆమ్ల, క్షార, ద్విస్వభావం గల వాటిగా వర్గీకరించండి.
a) CO
b) B2O3
e) Al2O3
c) SiO2
d) CO2
f) PbO2
g) Tl2O3
జవాబు:
తటస్థ ఆక్సైడ్ : CO
ఆమ్ల ఆక్సైడ్ : O2, SiO2, B2O3
క్షార ఆక్సైడ్ : Tl2O3
ద్విస్వభావ ఆక్సైడ్ : Al2O3, PbO2
ప్రశ్న 8.
మనిషి కృత్రిమంగా తయారు చేసిన ఏవైనా రెండు సిలికేట్ల పేర్లు రాయండి. [TS.17][IPE ’14]
జవాబు:
గాజు మరియు సిమెంట్లు మనిషిచే తయారుచేయబడిన సిలికేట్లు.
ప్రశ్న 9.
గ్రూపు 14 మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసాన్ని రాయండి.
జవాబు:
గ్రూపు 14 మూలకాల బాహ్య ఎలక్ట్రాన్ విన్యాసం ns np2.
1) కార్బన్ – [He]2s²2p²
2) సిలికాన్ – [Ne] 3s²3p²
3) జెర్మేనియం – [Ar] 3d104s²4p²
4) టిన్ – [Kr]4d105s²5p²
5) లెడ్ – [Xe] 4f145d106s²6p²
ప్రశ్న 10.
గ్రాఫైట్ కందెనగా ఎట్లా పనిచేస్తుంది? [Mar’11][TS 15,17,19,20]
జవాబు:
గ్రాఫైట్కి ద్విమితీయ పొరల నిర్మాణం వుంటుంది. మరియు దీనిని తేలికగా విచ్ఛేదనం చేయవచ్చు. కావున గ్రాఫైట్ కందెనగా పనిచేస్తుంది.
ప్రశ్న 11.
గ్రాఫైట్ మంచి విద్యుద్వాహకం. వివరించండి ? [TS 19][AP 17,18,22]
జవాబు:
గ్రాఫైట్లో ప్రతి కార్బన్ పరమాణువు sp² సంకరీకరణం చెందుతుంది. ప్రతి కార్బన్ పరమాణువు ఒక శుద్ధ ‘p’ ఆర్బిటాలు కలిగి వుంటుంది. స్వేచ్ఛా ఎలక్ట్రానులు కలిగి వుండుట వల్ల గ్రాఫైట్ మంచి విద్యుద్వాహకం.
ప్రశ్న 12.
సిలికా నిర్మాణాన్ని వివరించండి.
జవాబు:
- సిలికా త్రిజామితీయ నిర్మాణం కలిగి ఉంటుంది బృహత్ అణువు.
- Si, O పరమాణువులు ఒకదాని తరువాత ఒకటి 8 పరమాణువులున్న వలయాలుగా ఏర్పడతాయి.
- Si చుట్టూ ఆక్సిజన్ పరమాణువులు చతుర్ముఖీయంగా ఏర్పడతాయి.
- SiO2 లో Si పరమాణువు sp³ సంకరీకరణం చెందును.
![]()
ప్రశ్న 13.
“సంశ్లేషణ వాయువు” (synthesis gas). అంటే ఏమిటి? [AP 20][AP,TS 18][Imp.Q]
జవాబు:
- వాటర్గ్యాస్ను సంశ్లేషణ వాయువు అంటారు.
- CO మరియు H2 మిశ్రమాన్ని వాటర్ గ్యాస్ అంటారు.
- నీటి ఆవిరిని వేడి కోక్ ద్వారా పంపి వాటర్గా గ్యాసు తయారు చేస్తారు.
- ఇది మిథనోల్ మరియు అనేక హైడ్రో కార్బన్లను సంశ్లేషణ చేయుటకు ఉపయోగపడును. అందువలన దీనిని సంశ్లేషణ వాయువు అంటారు.
ప్రశ్న 14.
“ప్రొడ్యూసర్ వాయువు” (producer gas) అంటే ఏమిటి? [TS 16]
జవాబు:
CO మరియు N2 ల మిశ్రమాన్ని ప్రొడ్యూసర్ వాయువు అంటారు. దీనిని వేడి కోక్ పై నీటి ఆవిరిని పంపి తయారుచేస్తారు.
ప్రశ్న 15.
వజ్రానికి అధిక ద్రవీభవన ఉష్ణోగ్రత ఉంటుంది-వివరించండి. [AP 18,19,22]
జవాబు:
ధృడమైన C-C బంధాల అల్లికతో ఉన్న త్రిమితీయ నిర్మాణం డైమండు ఉంటుంది. ధృడమైన బంధాలను విచ్ఛిన్నం చేయడానికి చాలా శక్తి కావాలి. అందువల్ల దీని ద్రవీభవన ఉష్ణోగ్రత చాలా అధికం.
ప్రశ్న 16.
కిరణజన్య సంయోగక్రియలో CO2 పాత్ర ఏమిటి? [IPE ’14]
జవాబు:
పచ్చటి మొక్కలు వాతావరణంలోని CO2 ను కార్బోహైడ్రేట్లుగా మార్చుటను కిరణజన్య సంయోగక్రియ అంటారు. కిరణజన్య సంయోగక్రియలో CO2, గ్లూకోజ్ వంటి కార్బోహైడ్రేట్లుగా మారును.
![]()
ప్రశ్న 17.
హరితగృహ ప్రభావాన్ని ఏ విధంగా CO2 పెంచుతుంది. ?
జవాబు:
- పచ్చని మొక్కలు CO2 వాయువును శోషించుకొని O2 వాయువును విడుదల చేయును.
- అడవులను నరికివేయట వలన, సున్నపురాయి వియోగం వలన మరియు ఇంధనాలు మండించుట వలన CO2 గాఢత పెరుగును.
- CO2 గాఢత పెరుగుట వలన O2 – CO2 సమతుల్యత వాతావరణంలో దెబ్బతింటుంది. దీని వలన హరిత గృహప్రభావం పెరుగును.
ప్రశ్న 18.
సిలికోన్లు అంటే ఏమిటి? [AP 15]
జవాబు:
సిలికోన్లు ఆర్గానో సిలికాన్ సమ్మేళనాలు. సిలికోన్లలో సిలికాన్కు ఆక్సిజన్, కార్బన్లు బలంగా బంధింపబడి వుంటాయి.
ఆల్కైల్ క్లోరైడ్ను సిలికాన్ మీద 300°C వద్ద, కాపర్ ఉత్ప్రేరకం సమక్షంలో పంపినపుడు ఆల్కైల్ ప్రతిక్షేపక క్లోరో సిలికోన్లు ఏర్పడతాయి.
![]()
ప్రశ్న 19.
సిలికోన్ల ఉపయోగాలు రాయండి.
జవాబు:
సిలికోన్ ఉపయోగాలు:
- సిలికోస్ రబ్బరు తయారీలో
- వాటర్ ప్రూఫ్ బట్టలు, కాగితాలు తయారు చేయడానికి
- విమానాల్లో కందెనలుగాను, గ్రీజు తయారీలో
- పెయింటింగ్లలోను, పింగాణీలలోను ఉపయోగిస్తారు.
![]()
ప్రశ్న 20.
తగరం (టిన్) మీద నీటి ప్రభావం ఏమిటి? [Imp.Q]
జవాబు:
తగరం లోహం నీటి ఆవిరితో చర్య జరిపి టిన్ డైఆక్సైడ్ మరియు డైహైడ్రోజన్ వాయువును ఏర్పరుచును. ఈ చర్యనీటి ఆవిరి వియోగం చెందును.
![]()
ప్రశ్న 21.
SiCl4 గురించి రాయండి.
జవాబు:
- SiCl4 ను టెట్రాక్లోరోసిలికో మీథేన్ అంటారు.
- ‘Si’.లో 3d ఆర్బిటాల్ ఉండుట వలన SiCl4 లూయీ ఆమ్లంగా పనిచేయును.
- SiCl4 జలవిశ్లేషణం చేసినపుడు నీటి అణువులు Si-పరమాణువులతో సమన్వయ సంయోజనీయ బంధాలను ఏర్పరుచును.
ఉపయోగాలు:
- SiCl4 మరియు NH3 ల మిశ్రమంలను స్మోక్ఇస్క్రీన్ల తయారీలో ఉపయోగిస్తారు.
- ట్రాన్సిస్టర్ తయారీలో ఉపయోగిస్తారు.
- SiCl4 నుండి తయారు చేయబడిన SiO2 పెయింట్లు, రెసిన్ల తయారీలో ఉపయోగిస్తారు.
ప్రశ్న 22.
CO2 వాయువు కానీ SiO2 ఘనపదార్థం వివరించండి. [Imp.Q]
జవాబు:
సిలికా త్రిమితీయ చతుర్ముఖీయ నిర్మాణాన్ని కలిగి వుంటుంది. దీనిలోని అణువులన్నీ బలమైన సమయోజనీయ బంధాలతో బంధింపబడి వుంటాయి. కావున సిలికా నిర్మాణం అత్యంత స్థిరమైనది. మరియు Si-O బంధాలను విడగొట్టడానికి తగినంత శక్తి అవసరం. కనుక, సాధారణ ఉష్ణోగ్రత వద్ద SiO2 ఘనపదార్ధం.
CO2 లోని ప్రతి అణువు, కార్బన్లోని రెండు ఆక్సిజన్ పరమాణువులతో ద్విబంధాన్ని ఏర్పరుస్తుంది. CO2 అణువులు బలహీనమైన అంతరణుక ఆకర్షణ బలాలను కలిగివుంటాయి. వీటికి వాండర్వాల్ ఆకర్షణ బలాలు వుంటాయి. ఆ విధంగా సాధారణ ఉష్ణోగ్రతల వద్ద SiO2 ఘనపదార్ధం కాగా, CO2 వాయువుగా వుంటుంది.
ప్రశ్న 23.
ZSM-5 ఉపయోగం రాయండి. [TS 16,19,20]
జవాబు:
ZSM -5 అనేది ఒక జియోలైట్. దీనిని ఆల్కహాల్ను నేరుగా గాసోలీన్గా మార్చుటకు ఉపయోగిస్తారు.
ప్రశ్న 24.
పొడిమంచు(dry ice) ఉపయోగం ఏమిటి? [Imp.Q][AP 15]
జవాబు:
ఘనరూప CO2 ను పొడిమంచు (dry ice) అంటారు. దీనిని శీతలీకారిణిగా ఉపయోగిస్తారు.
ప్రశ్న 25.
జలవాయువు (water gas) ఎలా తయారుచేస్తారు? [Imp.Q]
జవాబు:
కార్బన్ మోనాక్సైడ్ మరియు హైడ్రోజన్ల మిశ్రమాన్ని వాటర్స్ అంటారు.
వేడికోకు బాగా వేడిచేసిన నీటి ఆవిరితో పంపి జలవాయువును తయారుచేస్తారు.

ప్రశ్న 26.
ప్రొడ్యూసర్ వాయువు (producer gas) ఎలా తయారు చేస్తారు? [TS 19][Imp.Q]
జవాబు:
CO మరియు N2ల మిశ్రమాన్ని ప్రొడ్యూసర్ గాస్ అని కూడా అంటారు.
తెల్లటి వేడికోక్ పై గాలిని పంపి ప్రొడ్యూసర్ వాయువును తయారుచేస్తారు.

ప్రశ్న 27.
గ్రాఫైట్లో C-C బంధదూరం, వజ్రంలో C-C బంధదూరం కంటే తక్కువ – వివరించండి. [Imp.Q]
జవాబు:
- గ్రాఫైట్ నందు ‘C’ పరమాణువు sp² సంకరీకరణం చెందును. బంధదైర్ఘ్యం 1.42A° (లేదా) 141.5 pm.ఉండును.
- గ్రాఫైట్ ద్విజామితీయ నిర్మాణం కలిగియుండును. షట్కోణాకార పొరల వంటి జాలక నిర్మాణం కలిగియుండును.
- వజ్రం నందు ‘C’, పరమాణువు sp³ సంకరీకరణం చెందును. బంధధైర్ఘ్యం 1.54A° (లేదా) 154 pm ఉండును.
- వజ్రం త్రిజామితీయ నిర్మాణం కలిగియుండే టెట్రాహెడ్రల్ బృహత్అణువు.
![]()
ప్రశ్న 28.
వజ్రాన్ని అమూల్యమైన రాయిగా వాడతారు -వివరించండి. [Imp.Q]
జవాబు:
వజ్రమునకు కాంతి పరావర్తన మరియు అత్యధిక వక్రీభవన గుణకం ఉండుట కారణంగా దీనిని ఆభరణాలలో అమ్యూలమైన రత్నంగా వాడతారు.
ప్రశ్న 29.
కార్బన్ సంయోజకత నాలుగు కంటే ఎక్కువ ఎప్పుడు చూపించదు కానీ ఆ కుటుంబంలో మిగతా మూలకాలు సంయోజకత ఆరు వరకు చూపిస్తాయి – వివరించండి.
జవాబు:
- C నందు d- ఆర్బిటాళ్లు లేకపోవుట వలన నాలుగు కంటే ఎక్కువ సంయోజకత చూపదు.
- కార్బన్ కుటుంబంలోని మిగతా మూలకాలలో d – ఆర్బిటాళ్లు గలవు. అందువలన అవి ఆరు వరకు సంయోజకతను చూపుతాయి.
ప్రశ్న 30.
ప్రొడ్యూసర్ వాయువు, జలవాయువు కంటే తక్కువ సామర్థ్యం గల ఇంధనం – వివరించండి. [Imp.Q]
జవాబు:
ప్రొడ్యూసర్ వాయువు కెలోరిఫిక్ విలువ 5439.2 KJ/m³. జలవాయువు కెలోరిఫిక్ విలువ 13,000KJ/m³. జలవాయువుకు అధిక కెలోరిఫిక్ విలువ కలిగి ఉండుటవలన ప్రొడ్యూసర్ వాయువు కంటే ఎక్కువ సామర్థ్యం కలిగి ఉంటుంది.
ప్రశ్న 31.
SiF-26 తెలుసు కాని SiCl-26 తెలియదు వివరించండి. [Imp.Q][AP 16,19]
జవాబు:
ముఖ్య కారాణాలు:
- Si4+ అయాన్ సైజు పరిమితి వల్ల దాని చుట్టూ ఆరు పెద్ద క్లోరైడ్ అయానులకు సరిపడినంత చోటు లేకపోవడం.
- క్లోరైడ్ అయాన్ ఒంటరి జంట Si4+ ల మధ్య అన్యోన్య చర్య అంత బలమైంది కాదు.
ప్రశ్న 32.
వజ్రం మరియు గ్రాఫైట్ యొక్క ఉపయోగాలు వ్రాయుము.
జవాబు:
వజ్రం ఉపయోగాలు:
- ఆభరణాల్లో అమూల్యమైన రత్నంగా ఉపయోగిస్తారు.
- గాజును కోయటానికి మరియు భారీ శిలలకు రంధ్రాలు చేయడానికి
గ్రాఫైట్ ఉపయోగాలు:
- కందెనగా
- ఎలక్ట్రోడ్గా
- లెడ్ పెన్సిల్ తయారిలో
- అణు రియాక్టర్లలో మితకారిగా
ప్రశ్న 33.
వజ్రం కఠినంగా ఎందుకు ఉంటుంది? [May’13][TS 15,22]
జవాబు:
డైమండ్లో ప్రతి కార్బన్ పరమాణువు చుట్టూ నాలుగు కార్బన్ పరమాణువులు చతుర్ముఖీయంగా ఏకబంధాలతో బంధింపబడి ఉండటం వలన అది బృహదణు నిర్మాణం కలిగి ఉంటుంది. అంతే కాకుండా డైమండ్ త్రిజ్యామితీయంగా ఉంటుంది. దీనిలోని C-C బంధాలను విడగొట్టడం చాలా కష్టం. అందువలన డైమండ్ కఠినత్వం కలిగి ఉంటుంది.
Short Answer Questions (స్వల్ప సమాధాన ప్రశ్నలు)
ప్రశ్న 1.
నిర్మాణాల ఆధారంగా వజ్రం, గ్రాఫైట్ల ధర్మాలలో తేడాలను వివరించండి. [AP 17][TS 17]
జవాబు:
| డైమండ్ | గ్రాఫైట్ |
| 1) డైమండ్ చాలా గట్టి పదార్ధం. స్వేచ్ఛా ఎలక్ట్రానులు లేకపోవడం వల్ల డైమండ్లు అవిద్యుద్వాహకాలు. | 1) గ్రాఫైట్ మెత్తనిది. స్వేచ్ఛా ఎలక్ట్రానులు వుండడం వల్ల గ్రాఫైట్లు మంచి విద్యుద్వాహకాలు. |
| 2) ప్రతి కార్బన్ 4 ఇతర కార్బన్లతో చతుర్ముఖీయంగా వుండును. | 2) ప్రతి కార్బన్ 3 ఇతర కార్బన్ పరమాణువులతో హెక్సాగోనల్ వలయాన్ని కలిగి వుండును. |
| 3) ఇది త్రిమితీయ పాలిమర్. | 3) ఇది ద్విమితీయ పొరల నిర్మాణం కలది. |
| 4) C–C బంధ దైర్ఘ్యం 1.54 A॰ మరియు బంధకోణం 109°281. | 4) C-C బంధ దైర్ఘ్యం 1.42 A° మరియు బంధకోణం 120॰. |
| 5) కార్బన్ పరమాణువులు బలమైన కోవలెంట్ బంధాలతో బంధింపబడి వుంటాయి. | 5) కార్బన్లోని హెక్సాగోనల్ పొరలు బలహీనమైన వాండర్వాల్ బలాలను కలిగి వుంటాయి. |
| 6) sp³ సంకరీకరణం | 6) sp² సంకరీకరణం |
![]()
ప్రశ్న 2.
మీరేమి అర్థం చేసుకొన్నారు (a) రూపాంతరత (b) జడజంట ప్రభావం (c) శృంఖలత్వం (Catenation)
జవాబు:
(a) రూపాంతరత:
ఒకే మూలకం వివిధ రూపాల్లో వేరు వేరు భౌతిక ధర్మాలతో ఒకే రసాయన ధర్మాలను కలిగి వుండటాన్ని రూపాంతరత అంటారు.
కార్బన్ యొక్క స్ఫటిక రూపాంతరాలు వజ్రం, గ్రాఫైట్.
(b) జడజంట ప్రభావం:
‘ns’ ఎలక్ట్రాన్ జంట బంధంలో పాల్గొనుటకు విముఖత చూపుటను జడ ఎలక్ట్రాన్ జంట ప్రభావం అంటారు.
ఉదా: లెడ్ +2 స్థిరమైన ఆక్సీకరణ స్థితిని ప్రదర్శించును. దీనికి కారణం జడ ఎలక్ట్రాన్ జంట ప్రభావం.
(c) శృంఖలత్వం:
ఒక మూలక పరమాణువులు ఒకదానితో ఒకటి కలిసి శృంఖలాలను ఏర్పరుచుకునే ప్రక్రియను కాటనేషన్ అంటారు. ఉదా: కార్బన్ [TS 18]
కార్బన్ అత్యధిక శృంఖలత్వం కలిగియుండును. దీనికి కారణం అధిక బంధ శక్తి (348 KJ/mole)
ప్రశ్న 3.
సిలికేట్ల మీద సంక్షిప్తంగా రాయండి.
జవాబు:
సిలికేట్లను ఎక్కువగా నిర్మాణ రంగంలో ఉపయోగిస్తారు.
ఉదా: గ్రానైట్లు, పలకలు, ఇటుకలు, సిమెంట్ మొదలైనవి. పింగాణీలు, గాజు కూడా సిలికేట్లే.
Si-O బంధాలు సిలికేట్లలో చాలా బలమైనవి. సాధారణ ద్రావణులలో దేనిలోనూ అవి కరగవు. ఇతర పదార్థాలతో త్వరగా కలవలేవు. సిలికేట్లను ఆరు రకాలుగా విభజించవచ్చు. అవి.
i) ఆర్థో సిలికేట్లు లేదా నీసో సిలికేట్లు:
వీటి సాధారణ ఫార్ములా M112(SiO4).
ఉదా: విల్లెమైట్ Zn2(SiO4)
ii) పైరో సిలికేట్లు లేదా సోరో సిలికేట్లు లేదా డైసిలికేట్లు:
వీటిలో Si2O-67 యూనిట్లుంటాయి. ఇవి చాలా అరుదు.
ఉదా: ధోర్ట్ ఐటైట్ – Sep (Si2O7)
iii) శృంఖల సిలికేట్లు :
వీటిలో SiO-23 యూనిట్లుంటాయి.
ఉదా: స్పాడ్యుమీన్ – LiAl(SiO3)2
iv) వలయ సిలికేట్లు :
ఈ సిలికేట్లలో వలయ నిర్మాణాలుంటాయి. వీటి సాధారణ ఫార్ములా (SiO3)2n-n, n = 4, 6, 8
ఉదా: బెరైల్ Be3Al2(Si6O18)
v) పలక సిలికేట్లు:
ప్రతి యూనిట్ లోని మూడు మూలలను పంచుకుంటే వచ్చేది అనంతమైన ద్విమితీయ పలక వీటి అనుఘటక ఫార్ములా (Si2O5)2n-n
ఉదా: కయొలిన్ (Al(OH)4Si2O5)
vi) అల్లిక సిలికేట్లు లేదా త్రిమితీయ సిలికేట్లు :
SiO-44 యూనిట్లలోని 4 ఆక్సిజన్లు టెట్రాహెడ్రల్లో నాలుగు మూలలను పంచుకునేటప్పుడు త్రిమితీయ జాలకంగా ఏర్పడుతుంది.
ఉదా: క్వార్ట్జ్, ట్రైడైమైట్, కిప్టో బొలైట్, జియొలైట్, అల్ట్రామెరైన్లు మొదలైనవి.
ప్రశ్న 4.
ఫుల్లరీన్ల గురించి సంక్షిప్తంగా రాయండి.
జవాబు:
- జడవాయువులైన హీలియమ్ లేదా ఆర్గాన్ల సమక్షంలో గ్రాఫైట్ను విద్యుచ్ఛాపంతో వేడిచేసిన ఫుల్లరిన్ తయారవుతుంది.
- ఫుల్లరీన్ మాత్రమే శుద్ధమైన కార్బన్ ఎందుకంటే వాటికి ఊగే. బంధాలు (dangling bonds) లేని మెత్తని నిర్మాణం గలది.
- ఫుల్లరీన్లు పంజరాన్ని పోలిన అణువులు. C60 అణువు సాకర్ బంతిని పోలిన నిర్మాణం ఉంటం వల్ల దీనిని బకిమినిష్టర్ ఫుల్లరిన్ (“Buckminister fullerene”.) అని కూడా అంటారు.
- ఫుల్లరీన్లో కార్బన్ పరమాణువు sp² సంకరీకరణం చెందుతుంది.
- దీనిలో ఆరు కార్బన్లున్న వలయాలు ఇరవై, ఐదు కార్బన్లున్న వలయాలు పన్నెండు ఉంటాయి. ఆరు కార్బన్ల వలయం ఆరు లేదా అయిదు కార్బన్ల వలయాలతో సంలీనం చెందుతుంది. కాని అయిదు కార్బన్ల వలయాలు ఆరు కార్బన్ల వలయాలతో మాత్రమే సంలీనం చెందుతాయి.
- బంతి ఆకృతి గల అణువుకు 60 శీర్షాలు (vertices) ఉన్నాయి. ప్రతి శీర్షంను ఒక కార్బన్ పరమాణువు ఆక్రమించి ఉంటుంది. ఈ కార్బన్లకు ఏక, ద్విబంధాలు ఉంటాయి.
- ఈ గోళాకార ఫుల్లరీన్లను బక్కీబాల్స్ (bucky balls) అని కూడా అంటారు.
![]()
ప్రశ్న 5.
కింది వాటిని వివరించండి.
(a) సిలికాన్ను మిథైల్ క్లోరైడ్తో కాపర్ సమక్షంలో అత్యధిక ఉష్ణోగ్రత వద్ద వేడి చేయబడింది.
(b) SiO2 ను HF తో చర్య జరపడం
(c) గ్రాఫైట్ కందెనగా పనిచేస్తుంది.
(d) వజ్రం అపఘర్షకంగా ఉంటుంది.
జవాబు:
(a) 573K వద్ద కాపర్ ఉత్ప్రేరక సమక్షంలో మిథైల్ క్లోరైడ్ సిలికాన్ పైకి పంపితే డైమిథైల్ సైలెన్ ఏర్పడును.
![]()
(b) సిలికా (SiO2)ను HF తో చర్య జరిపి సిలికాన్ టెట్రా ఫ్లోరైడ్ ఏర్పడుతుంది.
SiO2 + 4HF → SiF4 + 2H2O
(c) గ్రాఫైట్కు పొరల నిర్మాణం ఉంటుంది. పీడనం కలుగచేసినపుడు ఈ పొరలు ఒక దానిపై ఒకటి జారుతాయి. అందువలన గ్రాఫైట్కు జారుడు స్వభావం ఉంటుంది. ఈ స్వభావం వలన గ్రాఫైట్ను కందెనగా వాడుతారు.
(d) వజ్రంలోని సంయోజనీయ బంధాలు చాలా ధృడమైనవి వీటిని విఘటనం చెందింపలేము. కావున వజ్రం అపఘర్షకంగా ఉంటుంది. ఇది భారీ పనిముట్లు, అద్దకాలు వంటి వాటిని తయారుచేయుటకు వాడుతారు.
ప్రశ్న 6.
గ్రాఫైట్ మంచి విద్యుద్వాహకం. కాని డైమండ్ కాదు. వివరించండి? [May’10,09]
జవాబు:
డైమండ్లో ప్రతి కార్బన్ sp సంకరీకరణం చెందుతుంది. ఒక కార్బన్ నాలుగు కార్బన్ పరమాణువులు బలమైన సంయోజనీయ బంధాలతో టెట్రాహెడ్రల్ సౌష్ఠవంలో అమరి వుంటాయి. అందుచేత డైమండ్లో స్వేచ్ఛా ఎలక్ట్రానులు వుండవు. కావున డైమండ్ అవిద్యుద్వాహకం.
గ్రాఫైట్లో కార్బన్ sp² సంకరీకరణం చెందుతుంది. ఒక్కొక్క కార్బన్ పరమాణువు మూడు కోవలెంట్ బంధాలను మూడు వేర్వేరు కార్బన్లను ఉపయోగించుకుని నిర్మిస్తుంది. నాలుగో ఆర్బిటాల్ సంకరీకరణం చెందని ఒంటరి ఎలక్ట్రాన్ వున్న శుద్ధ p-ఆర్బిటాల్. ఈ ఎలక్ట్రాన్ π- బంధ నిర్మాణంలో పాల్గొంటుంది. ఆ విధంగా గ్రాఫైట్లో π-ఎలక్ట్రానులు సంకరీకరణం చెంది వుంటాయి. ఈ π ఎలక్ట్రానులుండటం వల్ల గ్రాఫైట్ మంచి విద్యుద్వాహకాలు.
ప్రశ్న 7.
డైమండ్ మరియు గ్రాఫైట్ల నిర్మాణాలను వివరించండి? [May’11]
జవాబు:
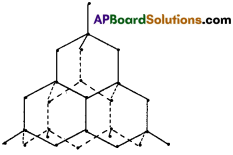
డైమండ్ :
- డైమండ్ అనేది కార్బన్ యొక్క స్పటిక రూపాంతరము.
- డైమండ్ , ప్రతి కార్బన్ సంకరీకరణం చెందుతుంది.
- ఒక కార్బన్ నాలుగు కార్బన్ పరమాణువులకు బంధింపబడి వుంటుంది. ఆ నాలుగు కార్బన్ పరమాణువులు ఏక బంధాలతో చతుర్ముఖీయ ఆకృతిలో అమరి వుంటాయి. చతుర్ముఖీయ నిర్మాణాల త్రిమితీయ అమరిక బృహదణువుగా ఏర్పడుతుంది.
- డైమండ్లో C – C బంధదైర్ఘ్యం = 1.54 A° మరియు బంధకోణం = 109°28′.
గ్రాఫైట్ :
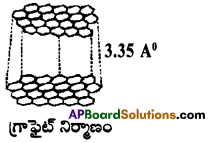
- గ్రాఫైట్ అనేది కార్బన్ యొక్క స్ఫటిక రూపాంతరం.
- గ్రాఫైట్ ద్విమితీయ పొరల నిర్మాణం కలది. గ్రాఫైట్ లోని కార్బన్ పరమాణువులు హెక్సాగోనల్ వలయాలను ఏర్పరుస్తాయి.
- గ్రాఫైట్, ప్రతి కార్బన్ ‘sp²’ సంకరీకరణం చెంది
మూడు వేర్వేరు కార్బన్లతో మూడు కోవలెంట్ బంధాలను ఏర్పరుస్తాయి.
నాలుగో ఆర్బిటాల్ సంకరీకరణం చెందని ఒంటరి ఎలక్ట్రాన్ వున్న శుద్ధ ‘P’ ఆర్బిటాల్ వుంటుంది. - గ్రాఫైట్లోని పొరలు బలహీనమైన వాండర్వాల్ బలాలు కలిగివుంటాయి.
- గ్రాఫైట్లో రెండు పొరల మధ్య దూరం 3.4 A°.
- C – C బంధ దైర్ఘ్యం 1.42 A° మరియు బంధకోణం 120°.
- దీనిని కందెనగా ఉపయోగిస్తారు.
![]()
ప్రశ్న 8.
సిలికా నిర్మాణాన్ని వివరించి, వాటి ఉపయోగాలను తెలపండి?
జవాబు:
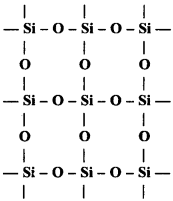
సిలికా నిర్మాణాం:
సిలికాన్ పరమాణువు సమయోజనీయ బంధంతో టెట్రాహైడ్రల్ రీతిలో నాలుగు ఆక్సిజన్ పరమాణువులతో కలిసి ఉంటుంది.
ఉపయోగాలు:
- సిలికాను బిల్డింగ్ నిర్మాణాలలో ఇసుకగా వాడతారు.
- UV వికిరణాలతో ప్రయోగాలు చేసేటప్పుడు క్వార్ట్జ్ గ్లాసిని వాడతారు. గాజు వస్తువులను చేయడానికి కూడా దీన్ని వాడతారు.
- సున్నం, ఇసుక, బంకమట్టిలను కలిపి ఉక్కు తయారీలో కొలిమిల లోపల లైనింగ్ చేయడానికి వాడతారు.
- రంగు క్వార్ట్జ్ ని రత్నాలుగా వాడతారు. పారదర్శక క్వార్ట్జ్ ని, కటకాలను, దృశ్య పరికరాలు చేయడానికి వాడతారు.
- లోహ నిష్కర్షణలో SiO2 ను ఆమ్ల ద్రావకారిగా వాడతారు.